
СПИСОК ПАТЕНТОВ С УПОМИНАНИЕМ ГИАЛУРОНОВОЙ КИСЛОТЫ
-
- 2017751 Способ получения гиалурона
- 2192150 БАД для профилактики йодной недостаточности
- 2112542 Препарат для лечения патологий соединительных тканей
- 2225206 Препарат для лечения рака молочной железы
- 2299733 Лечение опорно-двигательного аппарата
- 2299732 Способ лечения глаукомы
- 2299726 Противоинфекционная губная помада
- 2299725 Косметическое средство для ухода за кожей
- 2198878 Ароматическое соединение
- 2198702 Способ подготовки трофических язв к аутодермапластике
- 2198653 Вагинальные суппозитории
- 2197946 Композиция для ухода за волосами
- 2197923 Фармацевтическая композиция для лечения отеков роговицы
- 2298410 Биотрансплантант и способ лечения ревматических и аутоиммунных заболеваний
- 2197501 Фотоотверженный гель на основе сшитой гиалуроновой кислоты
- 2197228 Твердые лекарственные формы
- 2197222 Водная компазиция для ухода за волосами, лица и тела
- 2297425 Полипептиды
- 2297240 Композиция с гиалуроновой кислотой
- 2297230 Фармацевтическая компазиция с ксантоновой смолой
- 2196588 Глазные капли
- 2195955 Применение биологически активных веществ
- 2195926 Дерматологические композиции
- 2295954 Микрочастицы для доставки нуклеиновых кислот
- 2295951 Косметика для ухода за кожей лица и век
- 2195262 Фармакологическое средство на основе гиалуроновой кислоты
- 2194512 Способ профилактики и коррекции процесса старения кожи
- 2194478 Лечение экземы
- 2294716 Расширяемый стент
- 2194055 Сшитые сополимеры
- 2099350 Ассоциаты депротонированной гиалуроновой кислоты
- 2293557 Средство для лечения кожи и слизистых
- 2292878 Приготовление микроцастиц, содержащих метопропол
- 2292746 БАД
- 2192256 Защита кишечника
- 2191782 Получение модифицированной гиалуроновой кислоты
- 2292219 Паратиреоидный гормон человека
- 2291686 Микроцастицы
- 2191000 Косметическая маска
- 2290921 Фармацевтические и косметические средства против старения кожи
- 2290900 Модифицированный биоматериал для использования в офтальмологии
- 2290899 Получение биоматерьяла
- 2290397 Новые инданилиденовые соединения
- 2290186 Лечение сирингомиелии
- 2288702 Иррингационный раствор для офтальмологии
- 2288699 Гель для лечения стоматологических заболеваний
- 2188011 Активирующая остеогенез фармацевтическая композиция
- 2187327 Средство с антисептиком
- 2187325 Средство с радиопротекторным действием
- 2287330 Композиции миноксидила
- 2186786 Способ получения гиалуроновой кислоты
- 2186593 Лечение раненого процесса кожи
- 2286801 Очищение воды
- 2286781 Лечение ожогов пищевода у детей
- 2286764 Средство лечения воспалений полости рта
- 2185840 Лечение инфекционных заболеваний
- 2286151 Альфа-2-Дельта-Лиганда
- 2185149 Ранозаживляющий гель
- 2285527 Лечение ИЛ-6 заболеваний
- 2184448 Раствор хранения роговицы, включающий гиалуроновую кислоту
- 2090179 Крем для кожи
- 2183961 Способ лечения кожи
- 2284331 Соли алифотических аминов
- 2284187 Производные амида
- 2089191 Снизить внутрение давление
- 2283320 Получение гликозаминогликанов
- 2283129 Лечение опухолей
- 2283098 Косметические средства с Q
- 2182574 Ароматические соединения
- 2088257 Средство с гипохолестеролемическим действием
- 2088218 Состав для гигиенических салфеток
- 2088206 Способ получения препарата, создающего исскуственный загар
- 2282462 Противомикробные средства
- 2182008 Интровагинальная компазиция
- 2181999 Препарат с отсроченным высвобождением
- 2181998 Новые композиции липидов
- 2181995 Лечение болевого синдрома
- 2181295 Вирионная вакцина
- 2087144 Витамин Е
- 2379336 Способ стирки
- 2379052 Вакцинация
- 2180855Композиция в виде ионного комплекса
- 2379025 Противоинфекционный гель
- 2180825 Лечение травм роговицы
- 2281082 Способ коррекции эстетических и возрастных проблем кожи
- 2180576 Биоактивная добавка для косметических средств
- 2280459 Средство для изменения скорости роста или репродукции клеток
- 2179981 Соли переходного металла
- 2378010 Жидкие вакцины
- 2378008 Комбинированные вакцины
- 2378007 Анаболическое средство
- 2377973 Растительные экстракты
- 2280041 Способ получения водорастворимых комплексов гиалурил
- 2280038 Биополимеры
- 2323733 Йодный обмен
- 2377260 Гель
- 2178693 Противовирусное средство на основе гиалуроновой кислоты
- 2178692 Облегчающие зуд косметическое средство
- 2377022 Гемостатические спреи
- 2376982 Увлажняющая сыворотка для лица
- 2376974 Трансдермальный гель для лица
- 2362784 Гипо-и гиперацетилированные менингокковые капсульные сахариды
- 2177789 Устройство для доставки лекарства к шейке матки
- 2277954 Крем для лица омолаживающий
- 2376378 Способ получения метионина
- 2177332 Биоматериал для предотвращения послеоперационных спаек, с производной гиалуроновой кислотой
- 2177310 Способ получения таблеток
- 2376011 Средство для позвоночника
- 2277410 Косметическое средство
- 2323748 Медицинская повязка
- 2276998 Гидрогелевые композиции
- 2082416 Способ получения препарата с коллагенном из животного сырья
- 2375081 Адсорбирующее изделие
- 2375049 Охлаждающий пластырь
- 2346049 Способ получения гиалурона
- 2275913 Фармацевтические средства
- 2174985 Полисахарид с антиоксидантом
- 2373957 Носитель для лекарственных средств и биологически активных веществ
- 2373941 Способ коррекции возрастных и патологических изменений кожных покров
- 2174845 Композиции и способы доставки генетического материала
- 2174830 Средство для укрепления волос
- 2373769 Синбиотическая композиция
- 2274472 Лечение апорно-двигательного аппарата и болевых синдромов
- 2372929 Профилактическая композиция на основе веществ фенольной природы в липосомной форме
- 2173563 Способ нанесения на поверхность предметов покрытия на основе гиалуроновой кислоты, её производных и полусинтетических полимеров
- 2079304 фармацевтическая композиция, обладающая иммуносупрессорной и антимикробной активностью
- 2273645 Полипептид ожирения
- 2173154 Фракция кератансульфатолигосахаридов и содержащий ее фармацевтический препарат
- 2173136 Грязная мазь
- 2173128 Способ хирургического лечения центральных разрывов сечатки
- 2078561 Косметическое средство предотвращающее старение кожи
- 2172490 Способ прогнозирования воспалительных заболеваний молочной железы при эндопластике
- 2272645 Способ лечения ЦМВ-Инфекции у детей раннего возроста
- 2272636 Фармацевтическая композиция для местного лечения воспаления
- 2272635 Фармацевтически активная субстанция для офтальмологии
- 2272599 Биоматерьял для стабилизации прогрессирующей миопии "Коллаплант"
- 2172168 Средство для заживления ран на основе гиалуроновой кислоты
- 2371172 Фармацевтическая композиция для лечения нервной системы на основе стефаглабрина
- 2171470 Способ прогнозирования послеоперационной трансформации доброкачественных опухолей нервной системы
- 2077317 Состав для ванн
- 2271213 Комбинированные композиции, содержащие экстракты из растений и морских животных
- 2076872 Способ получения окрашенной гиалуроновой кислоты
- 2076671 Раствор для защиты роговицы
- 2370281 Конъюгаты гидроксиалкилкрахмал
- 2370275 Способ лечения (коррекции) косметических и возрастных дефектов кожи
- 2370258 Фармацевтическая композиция для парентальной доставки в форме лиофилизата
- 2270023 Способ экстракции и очистки протеогликана хрящего типа (варианты)
- 2369408 Гемостатическая композиция, включающая гиалуроновую кислоту
- 2369387 Фармацевтическая композиция для лечения нервной системы
- 2369379 Нетаблитированные жевательные формы для индивидуального введения
- 2169136 Производное коричной кислоты
- 70792 Медицинский аппликатор
- 20741717 Способ стабилизации аскорбиновой кислоты
- 2074712 Способ получения препарата, препятствующего преждевременной эякуляции
- 2367954 Способ прогнозирования развития кожной патологии у женщин с синдромом склерополикистозных яичников (СПКЯ)
- 2268075 Устройство для электрокинетической доставки
- 2268052 Средство для лечения воспалительных и дегенеративных заболеваний суставов
- 2167649 Способ получения твердой дисперсии умеренного водорастворимого лекарственного вещества
- 2167647 Гель для бритья
- 2073520 Лечение урологических инфекций
- 2367476 Биопластический материал
- 2367475 Мембрана для использования при направленной регенерации тканей
- 2367469 Фармацевтическая композиция на основе лизоамидазы
- 2367456 Фармацевтическая композиция обладающая антибактериальным и некролитическим действием
- 2367455 Фармацевтическая композиция обладающая некролитическим и антибактериальным действием
- 2267324 Применение антиадгезивных углеводов, препарат для уменьшения и /или блокирования адгезии патогенных веществ
- 2166934 Композиции включающие биологический агент
- 2166510 Псевдодипептиды
- 2366460 Композиции, имеющие высокую противовирусную и антибактериальную активность
- 2360901 Производные феноксиуксусной кислоты
- 2165749 Способ восстановления эндотелия роговицы
- 2265441 Способ укрепления склеры
- 2365382 Композиции и способы для регуляции развития сосудов
- 2070879 Соли гликозаминогликанов
- 2164914 Циклические и гетероциклические N - замещенные - иминогидроксамовые карбоновые кислоты
- 2264627 Хламидийный конъюктивит
- 2364399 Фармацевтический препарат на основе стефаглабрина
- 2264230 Препарат с замедленным высвобождением активного вещества
- 2363497 Фармацевтические композиции
- 2363496 Способ увеличения объема мягких тканей
- 2363473 Способ антифлогистической активации в эксперементе
- 2363461 Фармацевтический препарат на основе сигетина
- 2363459 Средства для введения в роговицу глаз для предотвращения офтальмологических нарушений
- 2363448 Фармацевтические композиции
- 2163123 Глазные капли
- 2162687 Усовершенствованнная лекарственная форма индуктора интерферана
- 2162343 Биосовместимый полимерный материал и способ его получения
- 2162327 Лечение рака
- 2067841 Способ получения ароматизатора
- 2161478 Способ консервированого лечения гонартроза
- 2361617 Вольфрамовые частицы в качестве рентгеноконтрастных веществ
- 2361552 Способы и устройства для дренирования жидкостей и понижения внутриглазного давления
- 2066996 Способ изготовления пленочного материала для офтальмохирургии
- 2361417 Корм с глюкозамином и экстрактом ивы для профилактики артроза у животных
- 2161002 Пищевой общеукрепляющий лечебно-профилактический продукт из хрящевой ткани акул
- 2360928 Комплексная матрица для медико-биологического применения
- 2160574 Способ лечения глаукомы
- 2360688 Способ лечения повреждений переферических нервов
- 2360670 Фармацевтическая композиция при климактерических расстройствах
- 2360646 Эндолюминальный протез
- 2260445 Способ усовершенствования транспортировки через легко прспосабливаемый полупроницаемый барьер
- 2260007 Производные амида
- 2359975 Способ получения модифицированных арабиногалактанов
- 2359974 Антигенные Пептиды
- 2159775 Псевдопептидный продукт
- 2259833 Фармацевтическая композиция для лечения роговицы глаза
- 2259816 Ранозаживляющее средство
- 2259815 Способ коррекции возрастных изменений, связанных с процессами старения кожи
- 2359706 Способ сохранения офтальмологических растворов
- 2359704 Антисептическое средство
- 2359662 Микрокапсулы
- 2159253 Катионные полимеры
- 2159111 Средство для ухода за кожей лица
- 2159105 Композиция для защиты кожи от опасных химических веществ Получение
- 2158593 Биосовместимый водный раствор
- 2358728 Способ лечения и предупреждения потери костной ткани
- 2258517 Способ хирургического лечения травмотических повреждений селезенки пленкой на основе гиалуроновой кислоты
- 2357968 Кристалические формы производной имидазола
- 2357957 Ингибиторы P38 и их применение
- 2157647 Пищевая добавка и ее получение
- 2357758 Препараты для чрескожной и чересслизистой добавки
- 2063244 Способ стабилизации растворов
- 2063140 Способ получения препарата для консервирования мяса
- 2157381 Способ получения гиалуроновой кислоты
- 2257198 Композиции микроцастиц
- 2356909 Белковый комплекс
- 2356570 Косметическая композиция
- 2256434 Способ закрытия перфорации барабанной перепонки
- 2356520 Способ лечения постконтузионного повреждения сечатки глаза
- 2156133 Гель
- 2255945 Полимерная композиция
- 2355761 Средства повторной дифференцировки
- 2061043 Способ повышения устойчивости урокиназы к нагреванию
- 2061005 Способ получения красителей для гистологических исследований
- 2355420 Зубная паста
- 2355385 Композиции пролонгированного действия с контролируемым высвобождением
- 2355240 Способ получения пищевого препарата хондропротекторного действия
- 2155057 Пихтово репейный бальзам
- 2354409 Способ производства высвобождающих лекарственные средчтва медицинских устройств
- 2254145 Раневое покрытие на основе коллаген-хитозанового комплекса
- 2254133 Лечение и профилактика ВИЧ-инфекции у человека
- 2253439 Фармацевтическая композиция для защиты и улучшения оптических свойств роговици при проведении эндовитреальных вмешательств
- 2253437 Способ омоложения кожи
- 2153352 Фармацевтическая композиция обладающая ранозаживляющим и противовоспалительным действием
- 2353354 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2252787 Способ получения искусственной матрицы кожи
- 2252767 Способ нормализации иммунобиохимического гомеостаза коров в предродовом и послеродовом периодах
- 2352583 Фармацевтическая композиция содержащая Fc-область иммуноглобулина в качестве носителя
- 2152403 Модифицированные полисахариды
- 2352356 Иммуногенная композиция
- 2352342 Исскусственный физиологический солевый раствор Способ его получения
- 2352330 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2352323 Фармацевтический препарат с модифицированным высвобождением
- 2152027 Способ подготовки ткани мозга для определения гликозаминогликанов
- 2251842 Интектицидный состав для борьбы с личинками оводов
- 2151580 Способ активации пролиферации эндотелия роговицы
- 2351648 Дифференцировка стромальных клеток, полученных из жировой ткани, в эндокринные клетки поджелудочной железы и их использование
- 2351595 N - гидроксиформамидные соединения в качестве ингибиторов металлопротеина
- 2251411 Косметическое средство в лиофилизированной фармацевтической форме
- 2251405 Косметика...ее композиции для косметических препаратов
- 2251367 Средство со сшитой гиалуроновой кислотой для наращивания тканей
- 2351359 Косметика для профилактики и лечения избыточной массы тела
- 2351322 Препарат на основе низкомолекулярного индуктора интерферона
- 2351153 Диета при остеортрите собак
- 2350958 Способ определения групповой принадлежности синовальной жидкости
- 2350625 Производные гиалуроновой кислоты с пониженной биодеградируемостью
- 2150266 Крем после бритья
- 2350354 Фармацевтическое средство содержащие антагонист и фактор некроза
- 2350340 Способ коррекции процессов регенерации
- 2350309 Способ лечения избыточной массы тела с помощью рефлексотерапии
- 2250047 Профилактический продукт из хрящевой ткани гидробионтов
- 2249467 Медицинский матерьял и изделия на его основе
- 2055079 Способ получения препарата гиалуроновой кислоты
- 2349599 Биоадгезив мидии
- 2054903 Способ лечения коллагеноза у бычков на откорме
- 2249210 Способ прогнозирования предрасположенности к развитию и тяжести течения деформирующего остеоартроза коленного сустава у взрослых
- 2349339 Средство для соединительной ткани
- 2148988 Человеческий интерферона
- 2148399 Лечение атеросклероза
- 2148396 Способ определения активного вещества в дифильных мазевых основах
- 2148375 Способ диагностики близорукости
- 2348415 Способ противоспаечной терапии после хирургического вмешательства
- 2348400 Препарат на основе низкомолекулярного индуктора интерферона
- 2348386 Способ непроникающего хирургического лечения первичной открытоугольной глаукомы
- 2248213 Лечение Галактозидальной А недостаточности
- 2347586 Микрофлюидизированные эмульсии типа "масло в воде" и вакцинные средства
- 2147243 Контрастное средство
- 2146526 Лечебный препарат дисбактериоза и урогенитальных инфекций
- 2146148 Терапевтическое применение фактора роста кератиноцитов (ФРК)
- 2146139 Способ повышения активности макрофагов и комбинации для его осуществления
- 2346277 Способ диагностики специфического синовита
- 2345793 Ультразвуковые контрастные вещества и их получение
- 2345782 Терапевтические комбинации на основе PORIFERA для лечения и предотвращения кожных заболеваний
- 2245131 Способ коррекции косметических недостатков кожи
- 2245130 Способ активации восстановительных процессов в коже
- 2144833 Хондроитиназа
- 2344809 Получение твердых дозированных форм с использованием сшитого нетермопластичного носителя
- 2244540 Косметический гель для ухода за кожей лица
- 2244536 Способ лечения дегенеративно-дистрофических заболеваний тазобедренного сустава
- 2344167 Хмелевый экстракт
- 2143884 Агент регулирования дифференциации клеток кожи, культурная среда для клеток или тканей и способ регулирования дифференциации клеток кожи
- 2343932 Способ получения обладающих пониженной растворимостью в воде пленночных материалов
- 2343903 Устройство доставки лекарств для контролируемого введения препаратов
- 2048817 Способ получения материала для лечения ожогов и гнойно - некронических ран
- 2048803 Гидратантный крем
- 2242974 Средства и способы лечения воспалительных заболнваний
- 2142816 Способ получения антигерпетической вакцины
- 2342923 Средство для обработки рук с увлажняющим эффектом
- 2142781 Косметика для макияжа ресниц и бровей и агент ингирирующий рост микроорганизмов в косметических средствах
- 2242251 Трансплантируемые стенты с биоактивными покрытиями
- 2142257 Способ обработки глазных имплантантов и контакных линз
- 2342389 Мононатриевая соль
- 2342107 Способ устранения западения верхнего века при анофтальме
- 2141828 Средство, пролонгирующее эффективность чесночного порошка
- 2241489 Косметическое средство матриксных протеинов для залечивания ран
- 2241443 Средство для лечения герпеса
- 2241414 Способ получения протезов кровеносных сосудов
- 2341539 Гидрогель
- 2141324 Регулятор скорости воздействия препарата для инъекций
- 2141312 Косметическое средство для ухода за кожей лица
- 2341296 Средства и способы покрытия медицинских имплантантов
- 2341272 Средство для неспецифической иммунотерапии
- 2341266 Стенты с нанесенным покрытием содержащим N - (5-(4-(4-
- 2341257 Иммуномодулирующее средство
- 2341255 Средство для лечения климактерических расстройств
- 2240821 Способ лечения урологических инфекций
- 2140786 Способ лечения лишая
- 2140243 Способ хирургического лечения диабетической ретинопатии и отслоек сечатной оболочки
- 2240140 Медицинская многослойная повязка и изделия на ее основе
- 2240135 Культура клеток, содержащая клетки - предшественники остеонегеза, имплантант на ее основе и его использование для восстановления целостности кости
- 2240123 Экзогенные биологически активные коньюгирующие вещества
- 2139886 Фотоотвержаемое производное гликозаминогликата, сшитое производное гликозаминогликата и способы их получения, способ предотвращения клеточной и тканевой адгезии
- 2139729 Вакцина. Способ стимулирования иммунной системы
- 2339386 Средство обладающее радио - и химиозащитным действием
- 2339369 Лечение офтальмологических нарушений с использованием мочевины и ее производных
- 2139041 Гидратантный регенерирующий крем и способ его получения
- 2139039 Косметический суперкрем для ухода за кожей
- 2139017 Способ получения боисовместимого материала
- 2138503 Производные камптотецина, способы их получения, уникальное средство
- 2338556 Средство содержащие антагонист Р2Х - рецептора и нестероидное противоспалительное лекарственное средство
- 2338514 Косметическое средство для профилактики старения кожи
- 2138297 Медицинские устройства, подверженные вызываемому разложению
- 2138295 Покрытие для ран
- 2337906 Ингибиторы цитозольной фосфолипазы А2 Применение физиологически допустимого корпускулярного ферримагнитного или ферромагнитного материала. Способ формирования магнитометрического изображения
- 2137501 Устройство формирования изображения
- 2137477 Способ лечения заболеваний характеризующихся аутоиммунной агрессией
- 2137467 Крем для кожи лица и тела
- 2137449 Способ коррекции дефектов преломления в глазу млекопитающего
- 2137402 Пищевая Добавка БАД
- 2336899 Способ стимуляции миелопоэза
- 2336862 Способ получения раствора для лечения роговицы
- 2336830 Способ восстановления костных структур челюсти
- 2136696 Новый полипептид и средство против ВИЧ - Инфекции
- 2336092 Биоадгезивное средство, по существу свободное от воды
- 2336089 Средство и способ лечения заболеваний периодонтальных и пульпы
- 2336074 Средства и способы лечения заднего сегмента глаза
- 2235548 Ранозаживляющее средство
- 2135186 Способ лечения рефлекторных синдромов при остеохондрозе
- 2234945 Стабилизатор водного раствора и водосодержащего сырья
- 2334762 Растворимая ассоциативная карбоксиметилцеллюлоза
- 2234514 Макропористые хитозановые гранулы и способ их получения. Способ культивирования клеток
- 2133615 Средство для лечения неврологических заболеваний
- 2233164 Способ профилактики развития послеоперационных спаек брюшной полости
- 2133127 Неткатный материал, способ его получения и способ лечения
- 2333223 Альдегидные производные сиаловой кислоты и средства на их основе
- 2333007 Полипептидные вакцины для широкой защиты против рядов поколений менингококов с повышенной вирулентностью
- 2332985 Дозированные формы анестезирующих средств с длительным высвобождением для обезболивания
- 2132677 Косметическая маска
- 38603 Пленочный аппликатор
- 2232594 Средство содержащие ингибирующие остеокластогенез фактор и полисахарид
- 2332238 Средство для прокладок, раневых повязок и других изделий, контактирующих с кожей
- 2331668 Стромальные клетки, получение из жировой ткани, для заживления дефектов роговицы и внутриглазных дефектов и их использование
- 2331438 Альфа - 2 - Дельта Лигант для лечения симптомов нижних мочевыводящих путей
- 2331411Электропряденые аморфные фармоцевтические средства
- 2331367 Способ профилактики образования спаек и их рецидива
- 2130767 Масло в воде для получения косметических и дерматологических средств, способ косметической обработки
- 2230752 Поперечносшитые гиалуроновые кислоты и их применение в медицине
- 2230558 Способ восстановления и сохранения здоровья скмьи
- 2230550 Средства длительного высвобождения, способ их получения и применения
- 2230458 Поддержания здоровья суставов
- 2330290 Способ определения состояния метаболических процессов в ткани суставного хряща
- 2230073 Способ поперечного сшивания карбоксилированных полисахаридов
- 2329059 Способ лечения полипозного риносинусита
- 2329037 Комбинированная терапия для лечения иммуновоспалительных заболеваний
- 2128666 Гиалуроновая кислота и ее соли, способ очистки гиалуроновой кислоты, способ получения гиалуроновой кислоты. Фармацевтический препарат с гиалуроновой кислотой и средства с гиалуроновой кислотой используемые в офтальмологии
- 2328740 Способ экспресс - оценки действия зубных паст
- 2128502 Косметический гель
- 2328272 Суппозитории индуктора интерферона
- 2328268 Косметика содержащая амфолитный сополимер
- 2128057 Композиционная мембрана, способ ее получения и способ направленной регенерации тканей с ее применением
- 2128055 Средство замедленного освобождения и способ его получения
- 2128049 Свечи
- 2227743 Полипептидные варианты с повышенной гепаринсвязывающей способностью
- 2326893 Ковалентное и нековалентное сшивание гидрофильных полимеров
- 2326697 Новый перевязочный материал для быстрого заживления раневой поверхности кожи
- 2126264 Фармацевтическое средство с гиалуроновой кислотой
- 2326137 Способ получения содержащих альгинат пористых формованных изделий
- 2325902 Способ выделения гликозаминогликанов из минерализованной соединительной ткани
- 2225195 Репелленты против насекомых
- 2325193 Сосудистый стент
- 2325184 Улучшенные везикулы наружной мембраны бактерий
- 2325153 Многокомпонентная фармацевтическая дозированная форма
- 2325152 Удерживаемая в желудке система регулируемой доставки лекарственного средства
- 2029955 Способ предоперационного определения помутнения задней капсулы хрусталика при экстракции катаракты
- 2324688 Производные бисбензизоселеназолонила с противоопухолевым, противовоспалительным и антитромбоническим действием
- 2323017 Устройство и способ контролируемый доставки активных веществ в кожу
- 2323011 Содержащий Коллаген I и Коллаген II способный к рассасыванию внеклеточный матрикс, предназначенный для реконструирования хряща
- 2322955 Способ изготовления имплантанта для пластики дефектов хрящевой ткани
- 2322454 Антитело против CCR5
- 2322263 Система продолжительного высвобождения растворимого лекарственного средства
- 2221561 Витамин Е и его сложные эфиры
- 2321634 Гены участвующие в метаболизме углерода и продуцировании энергии
- 2321597 Биоматерьял, способ его приготовления и его применение, медицинское средство, имплантант и вкладыш
- 2121340 Средство для похудения
- 2220737 Средство для улучшения состояния опорно-двигательного аппарата
- 2220729 Гель используемый в стоматологии
- 2320720 Способ культивирования фибропластов для заместительной терапии
- 2320378 Накожный аппликатор
- 2320369 Средства, содержащие Альфа - 2 - Дельта Лиганды и ингибиторы обратного захвата серотонина/норадреналина
- 2320362 Местные фармацевтические средства, содержащие проантоцианидины, для лечения дерматитов
- 2320322 Биоадгезивная доставка лекарств
- 2320318 Чувствительное к температуре изменяющие состояние средство гидрогеля
- 2025120 Способ получения препарата, содержащего Фактор /G-CSF/, стимулирующий рост колоний гранулоцитов
- 2319490 Средство для введения железа при лечении синдрома беспокойных ног
- 25995 Содержащее адгезив приспособление для фиксации зубных протезов в полости рта
- 2218907 Средство для ухода за кожей лица и веками
- 2318830 Способ получения модифицированного дерматансульфата
- 2118153 Косметика - туш для ресниц
- 2217441 Способ получения полимера
- 2317296 Изетионатная соль селективного ингибитора CDK4
- 2217171 Мембрана для использования при направленной регенерации тканей
- 2317095 Экстракты ECHINACEA ANGUSTIFOLIA
- 2216332 Препарат для лечения астроза
- 2216314 Крем - маска для обезвоженной кожи
- 2316333 Средство оздоровительно-восстановительных косметических панто-магниевых ванн
- 2021304 Способ получения биологически активного средства
- 2115662 Способ получения гиалуроновой кислоты
- 2315627 Впрыскиваемые имплантанты на керамической основе для заполнения морщин, кожных впадин, шрамов
- 2315623 Средство получаемое путем лиофилизации препарата
- 2114862 Способ получения гиалуроновой кислоты
- 2314791 Лечебно-Косметическое средство
- 2314791 Косметический крем-бальзам для ухода за кожей лица и шеи
- 2214600 Способ оценки эффективности лечения неврологических проявлений
- 2114602 Способ косметической обработки
- 2114587 Раствор для защиты роговицы
- 2214283 Имплантант для подкожного или внутрикожного введения
- 2313370 Медицинские протезы, имеющие улучшенную биологическую совместимость
- 2313356 Препарат для лечения демодекоза
- 2313338 Средство на основе этиллинолеата и триэтилцитрата для лечения себореи и угрей
- 2313328 Косметика содержащая тонкодисперный и пористый порошок
- 2212880 Способ получения препарата содержащего антибиотик, с замедленным высвобождением активного вещества
- 2312640 Способ лечения Блефароконьюнктивальной формы синдрома сухого глаза
- 2017751 Способ получения гиалуроновой кислоты
- 2312145 Гены CORYNEBACTERIUM GLUTAMICUM, кодирующие белки, участвующие в синтезе мембран и мембранном транспорте
- 2311458 Белки вызывающие измененную иммуногенную реакцию. Способ их получения и использования
- 2311183 Улучшенное разделение с использованием гталуроновой кислоты
- 2311177 Ингибиторы интегрина для лечения заболевания глаз
- 2300069 Косметическая маска
- 2211024 Уход за сухой кожей
- 2310440 Раствор для защиты роговицы от повреждений
- 2309684 Лечение межфалангового остеоатроза узелковой формы
- 2309406 Способ мониторинга фиброза печени у больных хроническим гепатитом с (ХГС)
- 2209088 Опосредованная рецепторами доставка генов с использованием векторов на основе бактериофагов
- 2308967 Уменьшение объема ткани
- 2308962 Средство для опорно-дигательного аппарата
- 2308957 Способ получения препарата для мезотерапии
- 2308954 Средство для лечения ран, содержащее плазму или сыворотку крови
- 2308951 Комплексный способ профилактики вагинальных дисбактериозов
- 2308937 Косметическая биологически активная добавка и косметический литофитокомплекс на ее основе
- 2208638 ДНК (варианты), способ получения белка
- 2207885 Способ подачи небольшого объема лечебного раствора к целевому месту
- 2207858 Лишенные побочных эффектов производные простагландинов для лечения глаукомы
- 2207845 Твердая лекарственная форма пролонгированного действия
- 2207844 Препарат для местного неинвазивного применения
- 2207841 Средства с антиферментативным действием
- 2306335 Стволовые клетки и решетки полученные из жировой ткани
- 2306140 Новые рецепторы для Helicobacter pylori и их применение
- 2205612 Способ эндотелизации IN VITRO протезов кровеносных сосудов
- 2105540 Депигментирующее средство
- 2304960 Косметическое средство для кожи
- 2304616 Гены участвующие в гомеостазе и адаптации
- 2204550Способ получения длинноцепочечной N-Ацилированной кислотой Аминокислот
- 2204415 Способ получения изображения
- 2204394 Средство для лечения грибковых инфекций, желудочных язв
- 2204366 Способ хирургического лечения глаукомы
- 2104034 Вагинальное увлажняющие средство, способ его получения
- 2303991 Биологически активная добавка
- 2303990 БАД
- 2303973 Адсорбирующее изделие
- 2203676 Средство обладающее иммунокорригирующим действием
- 2203672 Способ предупреждения беременности
- 2303635 Гены кодирующие белки резистентности и толерантности к стрессам
- 2303529 Способ фиксации альгинатного геля на твердой фазе, способ получения клеточного чипа на его основе
- 2203078 Способ лечения гнойных ран
- 2302412 Гидразоно-малонитрилы
- 2102400 Способ получения гиалуроновой кислоты
- 2202356 Способ стимуляции репаративных процессов длительно незаживающих ран и трофических язв
- 2202336 Средство для ухода за кожей
- 2302231 Глазные капли
- 2102082 Способ магнитометрического исследования тела человека или животного
- 2301814 Полиакриламидный гидрогель
- 2201765 Гибридные матричные имплантанты и эксплантанты
- 2301677 Биотрансплантант для лечения дегенеративных и трвматических заболеваний хрящевой ткани и способ его получения
- 2301676 Способ лечения ревматизма
- 2301674 Способ лечения больных с переломами нижней челюсти
- 2301661 Средство с регулируемым освобождением и способ его получения
- 2005488 Средство для лечения болезней соединительной ткани
- 2200001 Крем для кожи
|
РОССИЙСКАЯ ФЕДЕРАЦИЯ

ФЕДЕРАЛЬНАЯ СЛУЖБА
ПО ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ
ПАТЕНТАМ И ТОВАРНЫМ ЗНАКАМ
|
Патент №2260007 |
(54) ПРОИЗВОДНЫЕ АМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ
(57) Реферат:
Изобретение относится к новым производным амида формулы (I), их фармацевтически приемлемым солям или in vivo расщепляемым сложным эфирам, обладающим свойствами ингибитора продуцирования цитокинов посредством ингибирования действия фермента р38 киназы, и могут быть использованы при лечении различных заболеваний, например воспалительных или аллергических заболеваний. Изобретение также относится к способам их получения, фармацевтической композиции и способу ингибирования продуцирования цитокинов TNF . Производные амида формулы I соответствуют общей формуле . Производные амида формулы I соответствуют общей формуле
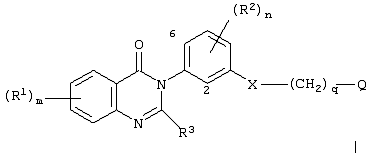
в которой Х является -NHCO- или -CONH-; m равно 0, 1, 2 или 3; R1 является галогеном, (1-6С)алкокси, N-(1-6С)алкил-ди[(1-6C)алкил]амино-(2-6С)-алкиламино или R1 является гетероциклилом, гетероциклил-(1-6C)алкилом, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6С)алкилгетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6C)-алкилгетероциклил-(1-6С)алкиламино, гетероциклилкарбониламино, гетероциклилсульфониламино, N-гетероциклилсульфамоилом, гетероциклил-(2-6С)алканоиламино, гетероциклил-(1-6C)алкокси-(1-6С)алкилом, гетероциклил-(1-6C)алкиламино-(1-6C)алкилом или N-(1-6С)алкилгетероциклил-(1-6C)алкиламино-(1-6C)алкилом, и где любая гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из галогена, (1-6С)алкила и (1-6С)алкокси, и любая гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из оксо или тиоксогруппы; n равно 0, 1 или 2; R2 является галогеном или (1-6С)алкилом; R3 является водородом, галогеном, (1-6С)алкилом или (1-6С)алкокси; q равно 0, 1, 2, 3 или 4; Q является арилом, арилокси, и т.д. 5 н. и 8 з.п. ф-лы, 8 табл.
(56) (продолжение):
CLASS="b560m"PARMAR S. S. ET AL " Synthesis et substituted quinazolone hydrasides: the relation between chemical structure and monoamine oxidase inhybitory activity""CHEMICAL ABSTRACTS,Columbus Ohio ,07.10.1968, v.069, no.15,abstr.no.059182.
HANSON G.J."Ingibitors of p38 kinase" EXPERT OPINION ON THERAPEUTIC PATENTS, GB, ASHLEY PUBLICATIONS, 01.01.1997, v.7,no.7.
WO 95/35304A1, 28.12.1995.
RU 2104276C1, 10.02.1998.
Данное изобретение относится к некоторым производным амида, которые полезны в качестве ингибиторов медиированных цитокином болезней. Данное изобретение также относится к способам получения производных амида данного изобретения, содержащим их фармацевтическим композициям и их применению в терапевтических способах, например, благодаря их способности ингибировать медиированные цитокином болезни.
Производные амида, описанные в данном изобретении, представляют собой ингибиторы продуцирования цитокинов, таких как Фактор Некроза Опухолевых Тканей (далее TNF), например, TNF , и различных представителей семейства интерлейкина (далее IL), например IL-1, IL-6 и IL-8. Соответственно, соединения данного изобретения могут быть полезными при лечении заболеваний или клинических состояний, при которых имеет место избыточное продуцирование цитокинов, например избыточное продуцирование TNF , и различных представителей семейства интерлейкина (далее IL), например IL-1, IL-6 и IL-8. Соответственно, соединения данного изобретения могут быть полезными при лечении заболеваний или клинических состояний, при которых имеет место избыточное продуцирование цитокинов, например избыточное продуцирование TNF или IL-1. Известно, что цитокины продуцируются разнообразными клетками, такими как моноциты и макрофаги, и что они вызывают развитие множества физиологических эффектов, которые, как полагают, играют важную роль при заболевании или медицинских состояниях, таких как воспаление и иммуннорегуляция. Например, TNF или IL-1. Известно, что цитокины продуцируются разнообразными клетками, такими как моноциты и макрофаги, и что они вызывают развитие множества физиологических эффектов, которые, как полагают, играют важную роль при заболевании или медицинских состояниях, таких как воспаление и иммуннорегуляция. Например, TNF и IL-1 вовлечены в сигнальный клеточный каскад, который, как полагают, вносит большой вклад в патологию болезненных состояний, таких как воспаление и аллергические заболевания, и цитокиноиндуцированную токсичность. Также известно, что в некоторых клеточных системах продуцирование TNF и IL-1 вовлечены в сигнальный клеточный каскад, который, как полагают, вносит большой вклад в патологию болезненных состояний, таких как воспаление и аллергические заболевания, и цитокиноиндуцированную токсичность. Также известно, что в некоторых клеточных системах продуцирование TNF предшествует и медиирует продуцирование других цитокинов, таких как IL-1. предшествует и медиирует продуцирование других цитокинов, таких как IL-1.
Аномальные уровни цитокинов также вовлечены, например, в продуцирование физиологически активных эйкозаноидов, таких как простагландины и лейкотриены, стимулирование выделения протеолитических ферментов, таких как коллагеназа, активацию иммунной системы, например, стимулированием Т-хелперных клеток, активацию действия остеокласта, ведущую к ресорбции кальция, стимулирование выделения протеогликанов, например, из хрящей, стимулирование пролиферации клеток и ангиогенез.
Также полагают, что цитокины вовлечены в генерирование и развитие болезненных состояний, таких как воспаление и аллергические заболевания, например воспаление суставов (особенно ревматоидный артрит, остеоартрит и подагра), воспаление желудочно-кишечного тракта (особенно воспаление кишечника, язвенный колит, болезнь Крона и гастриты), кожные заболевания (особенно псориаз, экзема и дерматит) и респираторные заболевания (особенно астма, бронхит, аллергический ринит, респираторный дистресс-синдром у взрослых и хроническое обструктивное заболевание легких), и в порождение и развитие различных сердечно-сосудистых и церебро-сосудистых расстройств, таких как застойная сердечная недостаточность, инфаркт миокарда, образование атеросклеротических бляшек, гипертензия, агрегация тромбоцитов, ангина, удар, болезнь Альцгеймера, нарушения, связанные с реперфузией, повреждения сосудов, включая рестеноз и заболевание периферийных сосудов, и, например, различные нарушения метаболизма костей, такие как остеопороз (включая возрастной и постклимактерический остеопороз), болезнь Педжета, метастазы в костях, гиперкальциемия, гиперпаратиреоз, остеосклероз, остеопороз и периодонтит, и аномальные изменения в метаболизме костей, которые могут сопровождаться ревматоидным артритом и остеоартритом. Избыточное продуцирование цитокина также вовлечено в медиирование некоторых осложнений при бактериальных, грибковых и/или вирусных инфекциях, таких как синдром эндотоксинового бактериально-токсического шока, септического шока и токсического шока, и в медиирование определенных осложнений при хирургическом вмешательстве или повреждении ЦНС, таком как нейротравма или ишемический удар. Избыточное продуцирование цитокина также вовлечено в медиирование или обострение развития заболеваний, включающих резорбцию хрящей или мышц, пневмосклероз, цирроз, почечный фиброз, кахексию, обнаруженную при определенных хронических заболеваниях, таких как злокачественные заболевания и синдром приобретенного иммунодефицита (СПИД), инвазивность опухоли и метастазы опухоли, и рассеянный склероз.
Доказательством того, что TNF играет центральную роль в каскаде сигнальных клеток, который приводит к ревматоидному артриту, является эффективность клинических иследований с антителами TNF играет центральную роль в каскаде сигнальных клеток, который приводит к ревматоидному артриту, является эффективность клинических иследований с антителами TNF (The Lancet, 1994, 344, 1125, и British Journal of Rheumatology, 1995, 34, 334). (The Lancet, 1994, 344, 1125, и British Journal of Rheumatology, 1995, 34, 334).
Таким образом, цитокины, такие как TNF и IL-1 считаются важными медиаторами значительного спектра заболеваний и клинических состояний. Соответственно, полагают, что ингибирование продуцирования и/или действия таких цитокинов будет полезным при профилактике, контроле или лечении таких заболеваний и клинических состояний. и IL-1 считаются важными медиаторами значительного спектра заболеваний и клинических состояний. Соответственно, полагают, что ингибирование продуцирования и/или действия таких цитокинов будет полезным при профилактике, контроле или лечении таких заболеваний и клинических состояний.
Не утверждая, что соединения данного изобретения оказывают фармакологическое действие только благодаря влиянию на единственный биологический процесс, полагают, что соединения ингибируют действие цитокинов посредством ингибирования фермента р38 киназы. р38 Киназа, также известная как связывающий цитокин супрессорный белок (далее CSBP) и реактивирующая киназа (далее RK), являются членом семейства ферментов митогенактивированного белка (далее MAP) киназы, про которые известно, что они активируются при физиологическом стрессе, таком как вызванный ионизирующим излучением, цитотоксичными агентами и токсинами, например эндотоксинами, такими как бактериальный липополисахарид, и рядом агентов, таких как цитокины, например TNF и IL-1. Известно, что р38 киназа фосфорилирует некоторые внутриклеточные белки, которые вовлечены в каскад ферментативных стадий, который ведет к биосинтезу и выделению цитокинов, таких как TNF и IL-1. Известно, что р38 киназа фосфорилирует некоторые внутриклеточные белки, которые вовлечены в каскад ферментативных стадий, который ведет к биосинтезу и выделению цитокинов, таких как TNF и IL-1. Известные ингибиторы р38 киназы описаны у G.J. Hanson в Expert Opinions on Therapeutic Patents, 1997, 7, 729-733. Известно, что р38 киназа существует в виде изоформ, определенных как р38 и IL-1. Известные ингибиторы р38 киназы описаны у G.J. Hanson в Expert Opinions on Therapeutic Patents, 1997, 7, 729-733. Известно, что р38 киназа существует в виде изоформ, определенных как р38 и р38 и р38 . .
Соединения данного изобретения являются ингибиторами продуцирования цитокинов, таких как TNF, в частности TNF , и различных интерлейкинов, в частности IL-1. , и различных интерлейкинов, в частности IL-1.
Некоторые производные 3-(5-бензамидо-2-метилфенил)-3,4-дигидрохиназолин-4-она описаны в Chemical Abstracts, том 77, реферат 19599. Раскрытые соединения включают 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-он, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-он и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-он.
Согласно одному аспекту данного изобретения представлено соединение формулы Ia
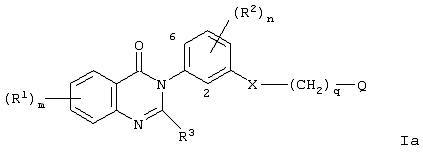
в которой Х является -NHCO- или -CONH-;
m равно 0, 1, 2 или 3;
R1 является гидрокси, галогеном, трифторметилом, циано, меркапто, нитро, амино, карбокси, карбамоилом, формилом, (1-6С)алкилом, (2-6С)алкенилом, (2-6С)алкинилом, (1-6С)алкокси, (1-6С)алкилтио, (1-6С)алкилсульфинилом, (1-6С)алкилсульфонилом, (1-6С)алкиламино, ди[(1-6С)алкил]амино, (1-6С)алкоксикарбонилом, N-(1-6C)алкилкарбамоилом, N,N-ди[(1-6С)алкил]карбамоилом, (2-6С)алканоилом, (2-6С)алканоилокси, (1-6C)алканоиламино, N-(1-6С)алкил-(1-6C)алканоиламино, N-(1-6С)алкилсульфамоилом, N,N-ди[(1-6C)алкил]сульфамоилом, (1-6C)алкансульфониламино, N-(1-6С)алкил-(1-6C)алкансульфониламино, галоген-(1-6C)алкилом, гидрокси-(1-6C)алкилом, (1-6С)алкокси-(1-6С)алкилом, циано-(1-6С)алкилом, амино-(1-6С)алкилом, (1-6С)алкиламино-(1-6С)-алкилом, ди[(1-6С)алкил] амино-(1-6С)алкилом, карбокси-(1-6С)-алкилом, (1-6С)алкоксикарбонил-(1-6С)алкилом, карбамоил-1-6С)алкилом, N-(1-6C)алкилкарбамоил-(1-6С)алкилом, N,N-ди[(1-6С)алкил]карбамоил-(1-6С)алкилом, галоген-(2-6С)алкокси, гидрокси-(2-6С)алкокси, (1-6С)алкокси-(2-6С)алкокси, циано-(1-6С)-алкокси, карбокси-(1-6С)алкокси, (1-6С)алкоксикарбонил-(1-6С)-алкокси, карбамоил-(1-6С)алкокси, N-(1-6С)алкилкарбамоил-(1-6С)-алкокси, N,N-ди[(1-6С)алкил]карбамоил-(1-6С)алкокси, амино-(2-6С)алкокси, (1-6С)алкиламино-(2-6С)алкокси, ди[(1-6С)алкил]-амино-(2-6С)алкокси, галоген-(2-6С)алкиламино, гидрокси-(2-6С)алкиламино, (1-6С)алкокси-(2-6С)алкиламино, циано-(1-6С)-алкиламино, карбокси-(1-6С)алкиламино, (1-6С)алкоксикарбонил-(1-6С)алкиламино, карбамоил-(1-6С)алкиламино, N-(1-6C)алкилкарбамоил-(1-6С)алкиламино, N,N-ди[(1-6C)алкил]карбамоил-(1-6С)алкиламино, амино-(2-6С)алкиламино, (1-6C)-алкиламино-(2-6С)алкиламино, ди-[(1-6C)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкилгалоген-(1-6C)алкиламино, N-(1-6C)алкилгидрокси-(2-6С)алкиламино, N-(1-6C)алкил-(1-6C)алкокси-(2-6С)алкиламино, N-(1-6C)алкилциано-(1-6C)алкиламино, N-(1-6C)алкилкарбокси-(1-6C)алкиламино, N-(1-6C)алкил-(1-6С)-алкоксикарбонил-(1-6C)-алкиламино, N-(1-6C)алкилкарбамоил-(1-6C)алкиламино, N-(1-6С)-алкил-N-(1-6С)алкилкарбамоил-(1-6C)-алкиламино, N-(1-6C)алкил-N,N-ди[(1-6C)алкил]карбамоил-(1-6C)-алкиламино, N-(1-6С)алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-(1-6C)алкиламино-(2-6С) -алкиламино, N-(1-6C)алкил-ди[(1-6C)алкил]амино-(2-6С)алкиламино, галоген-(2-6С)алканоиламино, гидрокси-(2-6С)алканоиламино, (1-6C)алкокси-(2-6С)-алканоиламино, циано-(2-6С)алканоиламино, карбокси-(2-6С)алканоиламино, (1-6C)алкоксикарбонил- (2-6С)-алканоиламино, карбамоил-(2-6С)алканоиламино, N-(1-6C)алкилкарбамоил-(2-6С) алканоиламино, N,N-ди[(1-6C)алкил]карбамоил-(2-6С)алканоиламино, амино-(2-6С)алканоиламино, (1-6С)алкиламино-(2-6С)-алканоиламино или ди-[(1-6C)алкил]амино-(2-6С)алканоиламино,
или R1 является арилом, арил-(1-6C)алкилом, арил-(1-6С)-алкокси, арилокси, ариламино, N-(1-6C)алкилариламино, арил-(1-6C)алкиламино, N-(1-6С)алкиларил-(1-6C)алкиламино, ароиламино, арилсульфониламино, N-арилсульфамоилом, арил-(2-6С)алканоиламино, гетероарилом, гетероарил-(1-6C)алкилом, гетероарилокси, гетероарил-(1-6C)алкокси, гетероариламино, N-(1-6С)алкилгетероариламино, гетероарил-(1-6C)алкиламино, N-(1-6С)алкилгетероарил-(1-6C)алкиламино, гетероарилкарбониламино, гетероарилсульфониламино, N-гетероарилсульфамоилом, гетероарил-(2-6С)алканоиламино, гетероарил-(1-6C)алкокси-(1-6С)алкилом, гетероарил-(1-6C)алкиламино-(1-6C)алкилом, N-(1-6С)алкилгетероарил-(1-6C)алкиламино-(1-6C)алкилом, гетероциклилом, гетероциклил-(1-6C)алкилом, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6С)алкилгетероциклиламино, гетероциклил-(1-6С)алкиламино, N-(1-6С)-алкилгетероциклил-(1-6С)алкиламино, гетероциклилкарбониламино, гетероциклилсульфониламино, N-гетероциклилсульфамоилом, гетероциклил-(2-6С)алканоиламино, гетероциклил-(1-6С)алкокси-(1-6С)алкилом, гетероциклил-(1-6С)алкиламино-(1-6С)алкилом или N-(1-6С)алкилгетероциклил-(1-6С)алкиламино-(1-6С)алкилом,
или (R1)m является (1-3С)алкилендиоксигруппой,
и где любой из заместителей R1, определенный выше, который содержит СН2-группу, которая присоединена к 2 атомам углерода, или СН3-группу, которая присоединена к атому углерода, может необязательно иметь на каждой указанной СН2 или СН3-группе заместитель, выбранный из гидрокси, амино, (1-6С)алкокси, (1-6С)алкиламино, ди-[(1-6С)алкил]амино и гетероциклила,
и где любая арильная, гетероарильная или гетероциклильная группа в заместителе R1 могут необязательно иметь 1 или 2 заместителя, выбранных из гидрокси, галогена, (1-6С)алкила, (1-6С)алкокси, карбокси, (1-6С)алкоксикарбонила, N-(1-6С)алкилкарбамоила, N,N-ди-[(1-6С)алкил]карбамоила, (2-6С)алканоила, амино, (1-6С)алкиламино, ди-[ (1-6С)алкил]амино, галоген-(1-6С)алкила, гидрокси-(1-6С)алкила, (1-6С)алкокси-(1-6С)алкила, циано-(1-6С)алкила, амино-(1-6С)алкила, (1-6С)алкиламино-(1-6С)алкила, ди-[(1-6С)алкил]амино-(1-6С)алкила, арила и арил-(1-6С)алкила,
и где любая гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из оксо- или тиоксогруппы;
n равно 0, 1 или 2;
R2 является гидрокси, галогеном, трифторметилом, циано, меркапто, нитро, амино, карбокси, (1-6С)алкоксикарбонилом, (1-6С)алкилом, (2-6С)алкенилом, (2-6С)алкинилом, (1-6С)алкокси, (1-6С)алкиламино или ди-[(1-6С)алкил]амино;
R3 является водородом, галогеном, (1-6С)алкилом или (1-6С)алкокси;
q равно 0, 1, 2, 3 или 4,
Q является арилом, арилокси, арил-(1-6С)алкокси, ариламино, N-(1-6С)алкилариламино, арил-(1-6С)алкиламино, N-(1-6С)алкиларил-(1-6С)алкиламино, ароиламино, арилсульфониламино, N-арилкарбамоилом, N-арилсульфамоилом, арил-(2-6С}-алканоиламино, (3-7С)циклоалкилом, гетероарилом, гетероарилокси, гетероарил-(1-6С)алкокси, гетероариламино, N-(1-6C)алкилгетероариламино, гетероарил-(1-6С)алкиламино, N-(1-6С)алкилгетероарил-(1-6С)алкиламино, гетероарилкарбониламино, гетероарилсульфониламино, N-гетероарилкарбамоилом, N-гетероарилсульфамоилом, гетероарил-(2-6С)алканоиламино, гетероциклилом, гетероциклилокси, гетероциклил-(1-6С)алкокси, гетероциклиламино, N-(1-6С)алкилгетероциклиламино, гетероциклил- (1-6С)алкиламино, N-(1-6С)алкилгетероциклил-(1-6С)-алкиламино, гетероциклилкарбониламино, гетероциклилсульфониламино, N-гетероциклилкарбамоилом, N-гетероциклилсульфамоилом или гетероциклил- (2-6С)алканоиламино,
и Q необязательно замещен 1, 2 или 3 заместителями, выбранными из гидрокси, галогена, трифторметила, циано, меркапто, нитро, амино, карбокси, карбамоила, формила, (1-6С)алкила, (2-6С)алкенила, (2-6С)алкинила, (1-6С)алкокси, (1-6С)алкилтио, (1-6С)алкилсульфинила, (1-6С)алкилсульфонила, (1-6С)алкиламино, ди-[(1-6С)алкил]амино, (1-6С)алкоксикарбонила, N-(1-6С)алкилкарбамоила, N,N-ди[(1-6С)алкил]карбамоила, (2-6С)алканоила, (2-6С)алканоилокси, (1-6С)алканоиламино, N-(1-6С)алкил-(1-6С)алканоиламино, N-(1-6C)алкилсульфамоила, N,N-ди-[(1-6C)алкил]сульфамоила, (1-6C)алкансульфониламино, N-(1-6C)алкил-(1-6C)алкансульфониламино, галоген-(1-6C)алкила, гидрокси-(1-6С)алкила, (1-6C)алкокси-(1-6C)алкила, циано-(1-6С)алкила, амино-(1-6С)алкила, (1-6C)алкиламино-(1-6C)алкила, ди-[(1-6C)алкил]амино-(1-6С)алкила, карбокси-(1-6C)алкила, (1-6C)алкоксикарбонил-(1-6С)алкила, карбамоил-(1-6С)алкила, N-(1-6С)алкилкарбамоил-(1-6С)алкила, N,N-ди-[(1-6C)алкил]-карбамоил-(1-6C)алкила, галоген-(2-6С)алкокси, гидрокси-(2-6С)алкокси, (1-6C)алкокси-(2-6С)алкокси, циано-(1-6C)алкокси, карбокси-(1-6C)алкокси, (1-6C)алкоксикарбонил-(1-6C)алкокси, карбамоил-(1-6C)алкокси, N-(1-6C)алкилкарбамоил-(1-6C)алкокси, N,N-ди-[(1-6C)алкил]карбамоил-(1-6C)алкокси, амино-(2-6С)-алкокси, (1-6C)алкиламино-(2-6С)алкокси, ди-[(1-6C)алкил]-амино-(2-6С)алкокси, галоген-(2-6С)алкиламино, гидрокси-(2-6С)алкиламино, (1-6C)алкокси-(2-6С)алкиламино, циано-(1-6C)-алкиламино, карбокси-(1-6C)алкиламино, (1-6C)алкоксикарбонил-(1-6C)алкиламино, карбамоил-(1-6C)алкиламино, N-(1-6C)-алкилкарбамоил-(1-6C)алкиламино, N,N-ди-[(1-6C)алкил]карбамоил(1-6C)алкиламино, амино-(2-6С)алкиламино, (1-6С)алкиламино-(2-6С)алкиламино, ди-[(1-6С)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкилгалоген-(1-6С)алкиламино, N-(1-6C)алкил-гидрокси-(2-6С)алкиламино, N-(1-6C)алкил-(1-6С)алкокси-(2-6С)алкиламино, N-(1-6C)алкилциано-(1-6C)алкиламино, N-(1-6С)алкилкарбокси-(1-6С)алкиламино, N-(1-6C)алкил-(1-6C)алкоксикарбонил-(1-6C)-алкиламино, N-(1-6C)алкилкарбамоил-(1-6C)алкиламино, N-(1-6С)алкил-N-(1-6C)алкилкарбамоил-(1-6C)алкиламино, N-(1-6C)-алкил-N,N-ди-[(1-6С)алкил]карбамоил-(1-6C)алкиламино, N-(1-6C)-алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-(1-6C)алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-ди-[(1-6C)алкил]амино-(2-6С)-алкиламино, галоген-(2-6С)алканоиламино, гидрокси-(2-6С)-алканоиламино, (1-6C)алкокси-(2-6С)алканоиламино, циано-(2-6С)алканоиламино, карбокси-(2-6С)алканоиламино, (1-6С)-алкоксикарбонил-(2-6С)алканоиламино, карбамоил-(2-6С)алканоиламино, N-(1-6C)алкилкарбамоил-(2-6С)алканоиламино, N,N-ди[(1-6C)алкил]карбамоил-(2-6С)алканоиламино, амино-(2-6С) -алканоиламино, (1-6C)алкиламино-(2-6С)алканоиламино, ди-[(1-6С)алкил]амино-(2-6С)алканоиламино, арила, арил-(1-6С)алкила, арил-(1 -6С)алкокси, арилокси, ариламино, N-(1-6С)алкил-ариламино, арил-(1-6C)алкиламино, N-(1-6C)алкиларил-(1-6C)-алкиламино, ароиламино, арилсульфониламино, N-арилсульфамоила, арил-(2-6С)алканоиламино, гетероарила, гетероарил-(1-6C)-алкила, гетероарилокси, гетероарил-(1-6C)алкокси, гетероари-ламино, N-(1-6С)алкил-гетероариламино, гетероарил-(1-6C)-алкиламино, N-(1-6C)алкил-гетероарил-(1-6C)алкиламино, гетероарилкарбониламино, гетероарилсульфониламино, N-гетероарил-сульфамоила, гетероарил-(2-6С)алканоиламино, гетероарил-(1-6С)алкокси-(1-6С)алкила, гетероарил-(1-6С)алкиламино-(1-6C) -алкила, N-(1-6C)алкилгетероарил-(1-6С)алкиламино-(1-6С)алкила, гетероциклила, гетероциклил-(1-6C)алкила, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6C)алкил-гетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6С)алкилгетероциклил-(1-6C)алкиламино, гетероциклилкарбонила-мино, гетероциклилсульфониламино, N-гетероциклилсульфамоила, гетероциклил-(2-6С)алканоиламино, гетероциклил-(1-6C)алкокси-(1-6С)алкила, гетероциклил-(1-6C)алкиламино-(1-6C)алкила и N-(1-6С)алкил-гетероциклил-(1-6C)алкиламино-(1-6C)алкила,
или Q замещен (1-3С)алкилендиоксигруппой,
и где любой заместитель радикала Q, определенный выше, который содержит СН2-группу, которая присоединена к 2 атомам углерода, или СН3-группу, которая присоединена к атому углерода, может необязательно иметь на каждой указанной СН2- или СН3-группах заместитель, выбранный из гидрокси, амино, (1-6С)алкокси, (1-6C)алкиламино, ди-[(1-6C)алкил]амино и гетероциклила,
и где любая арильная, гетероарильная или гетероциклильная группа в заместителе радикала Q может необязательно иметь 1 или 2 заместителя, выбранных из гидрокси, галогена, (1-6С)алкила, (1 -6С)алкокси, карбокси, (1 -6С)алкоксикарбонила, N-(1-6С)алкилкарбамоила, N,N-ди-[(1-6C)алкил]карбамоила, (2-6С)алканоила, амино, (1-6C)алкиламино, ди-[(1-6C)алкил]амино, галоген-(1-6С)алкила, гидрокси-(1-6С)алкила, (1-6С)алкокси-(1-6С)алкила, циано-(1-6С)алкила, амино-(1-6С)алкила, (1-6С)алкиламино-(1-6С)алкила, ди-[(1-6С)алкил]амино-(1-6С)алкила, арила и арил-(1-6С)алкила,
и где Q, если он является гетероциклильной группой или содержит гетероциклильную группу или любая гетероциклильная группа в заместителе радикала Q может необязательно иметь 1 или 2 заместителя, выбранных из оксо- или тиоксогруппы;
или его фармацевтически приемлемая соль или in vivo расщепляемый сложный эфир
за исключением 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
Согласно другому аспекту данного изобретения представлено соединение формулы Ib
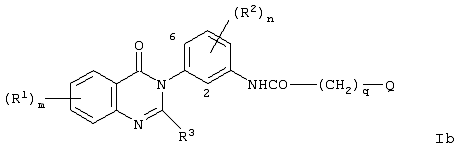
где m равно 0, 1, 2 или 3;
R1 является гидрокси, галогеном, трифторметилом, циано, меркапто, нитро, амино, карбокси, карбамоилом, формилом, (1-6С)алкилом, (2-6С)алкенилом, (2-6С)алкинилом, (1-6С)алкокси, (1-6С)алкилтио, (1-6С)алкилсульфинилом, (1-6С)алкилсульфонилом, (1-6C)алкиламино, ди[(1-6C)алкил]амино, (1-6C)алкоксикарбонилом, N-(1-6С)алкилкарбамоилом, N,N-ди[(1-6C)алкил]карбамоилом, (2-6С)алканоилом, (2-6С)алканоилокси, (1-6С)алканоиламино, N-(1-6C)алкилсульфамоилом, N,N-ди[(1-6C)алкил]сульфамоилом, (1-6С)алкансульфониламино, N-(1-6C) алкил-(1-6С)алкансульфониламино, галоген-(1-6C) алкилом, гидрокси-(1-6C)алкилом, (1-6С)-алкокси-(1-6С)алкилом, циано-(1-6C)алкилом, амино-(1-6С)-алкилом, (1-6C)алкиламино-(1-6C)алкилом, ди-[(1-6C)-алкил]-амино-(1-6C)алкилом, карбокси-(1-6C)алкилом, (1-6C)-алкоксикарбонил-(1-6C)алкилом, карбамоил-(1-6C)алкилом, N-(1-6С)алкилкарбамоил-(1-6C)алкилом, N,N-ди[(1-6C)алкил]карбамоил-(1-6C)-алкилом, галоген-(2-6С)алкокси, гидрокси-(2-6С)алкокси, (1-6С)алкокси-(2-6С)алкокси, циано-(1-6C)алкокси, карбокси-(1-6С)алкокси, (1-6С)алкоксикарбонил-(1-6C)алкокси, карбамоил-(1-6С)алкокси, N-(1-6C)алкилкарбамоил-(1-6C)алкокси, N,N-ди[(1-6C)алкил]карбамоил-(1-6C)алкокси, амино-(2-6C)алкокси, (1-6С)алкиламино-(2-6С)алкокси, ди[(1-6С)алкил]амино-(2-6С)-алкокси, галоген-(2-6С)алкиламино, гидрокси-(2-6С)алкиламино, (1-6С)-алкокси-(2-6С)алкиламино, циано-(1-6C)алкиламино, карбокси-(1-6С)алкиламино, (1-6C)алкоксикарбонил-(1-6C)алкиламино, карбамоил-(1-6С)алкиламино, N-(1-6C)алкилкарбамоил-(1-6C)-алкиламино, N,N-ди[(1-6C)алкил] карбамоил-(1-6C)алкиламино, амино-(2-6С)-алкиламино, (1-6C)алкиламино-(2-6С)алкиламино, ди-[(1-6C)алкил]-амино-(2-6С) алкиламино, N-(1-6C)алкилгалоген-(1-6C)алкиламино, N(1-6С)алкилгидрокси-(2-6С)алкиламино, N-(1-6С)алкил-(1-6С)-алкокси-(2-6С)алкиламино, N-(1-6C)алкилциано-(1-6C)алкиламино, N-(1-6С)алкилкарбокси-(1-6C)алкиламино, N-(1-6С)алкил- (1-6C) -алкоксикарбонил-(1-6C)алкиламино, N-(1-6C)алкилкарбамоил-(1-6С)-алкиламино, N-(1-6С)алкил-N-(1-6С)-алкилкарбамоил-(1-6С)алкиламино, N-(1-6С)алкил-N,N-ди[(1-6C)-алкил]карбамоил-(1-6C)алкиламино, N-(1-6C)алкиламино-(2-6С)-алкиламино, N-(1-6C)алкил-(1-6C)алкиламино-(2-6С)алкиламино, N-(1-6С)алкил-ди[(1-6C)алкил]амино-(2-6С)алкиламино, галоген-(2-6С)алканоиламино, гидрокси-(2-6С)-алканоиламино, (1-6C)-алкокси-(2-6С)алканоиламино, циано-(2-6С)-алканоиламино, карбокси-(2-6С)алканоиламино, (1-6С)алкоксикарбонил-(2-6С)-алканоиламино, карбамоил-(2-6С)алканоиламино, N-(1-6С)-алкилкарбамоил-(2-6С)алканоиламино, N,N-ди[(1-6C)алкил]-карбамоил-(2-6С)алканоиламино, амино-(2-6С)алканоиламино, (1-6С)алкиламино-(2-6С)алканоиламино или ди-[(1-6C)алкил]амино-(2-6С)алканоиламино,
или R1 является арилом, арил-(1-6С)алкилом, арил-(1-6С)-алкокси, арилокси, ариламино, N-(1-6C)алкилариламино, арил-(1-6C)алкиламино, N-(1-6C)алкиларил-(1-6C)алкиламино, ароиламино, арилсульфониламино, N-арилсульфамоилом, арил-(2-6С)-алканоиламино, гетероарилом, гетероарил-(1-6C)алкилом, гетероарилокси, гетероарил-(1-6C)алкокси, гетероариламино, N-(1-6С)алкилгетероариламино, гетероарил-(1-6C)алкиламино, N-(1-6С)алкилгетероарил-(1-6C)алкиламино, гетероарилкарбониламино, гетероарилсульфониламино, N-гетероарилсульфамоилом, гетероарил-(2-6С)алканоиламино, гетероарил-(1-6C)алкокси-(1-6C)-алкилом, гетероарил-(1-6C)алкиламино-(1-6C)алкилом, N-(1-6C)-алкилгетероарил-(1-6C)алкиламино-(1-6C)алкилом, гетероциклилом, гетероциклил-(1-6C)алкилом, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6С)алкилгетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6C)-алкилгетероциклил-(1-6C)алкиламино, гетероциклилкарбониламино, гетероциклилсульфониламино, N-гетероциклилсульфамоилом, гетероциклил-(2-6С)алканоиламино, гетероциклил-(1-6C)алкокси-(1-6C)-алкилом, гетероциклил-(1-6C)алкиламино-(1-6C)алкилом или N-(1-6С)алкилгетероциклил-(1-6C)алкиламино-(1-6C)алкилом,
или (R1)m является (1-3С)алкилендиоксигруппой,
и где любой заместитель R1, определенный выше, который содержит CH2-группу, которая присоединена к 2 атомам углерода, или СН3-группу, которая присоединена к атому углерода, может необязательно иметь на каждой указанной СН2- или СН3-группе заместитель, выбранный из гидрокси, амино, (1-6C)алкокси, (1-6С)алкиламино, ди-[(1-6C)алкил]амино и гетероциклила, и где любая арильная, гетероарильная или гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из гидрокси, галогена, (1-6С)алкила, (1-6C) алкокси, карбокси, (1-6С)алкоксикарбонила, N-(1-6C)-алкилкарбамоила, N,N-ди-[(1-6C)алкил]карбамоила, (2-6C)-алканоила, амино, (1-6C)алкиламино, ди-[(1-6C)алкил]амино, галоген-(1-6C)алкила, гидрокси-(1-6С)алкила, (1-6С)алкокси-(1-6С)алкила, циано-(1-6C)алкила, амино-(1-6C)алкила, (1-6С)-алкиламино-(1-6C)алкила, ди-[(1-6C)алкил]амино-(1-6C)алкила, арила и арил-(1-6C)алкила;
n равно 0, 1 или 2;
R2 является гидрокси, галогеном, трифторметилом, циано, меркапто, нитро, амино, карбокси, (1-6C)алкоксикарбонилом, (1-6С)алкилом, (2-6С)алкенилом, (2-6С)алкинилом, (1-6С)-алкокси, (1-6С)алкиламино или ди-[(1-6С)алкил]амино;
R3 является водородом, галогеном, (1-6С)алкилом или (1-6С)алкокси;
q равно 0, 1, 2, 3 или 4;
Q является арилом, арилокси, арил-(1-6С)алкокси, ариламино, N- (1-6C)алкилариламино, арил-(1-6С)алкиламино, N-(1-6С)алкиларил-(1-6С)алкиламино, ароиламино, арилсульфониламино, N-арилкарбамоилом, N-арилсульфамоилом, арил-(2-6С)-алканоиламино, (3-7С)циклоалкилом, гетероарилом, гетероарилокси, гетероарил-(1-6C)алкокси, гетероариламино, N-(1-6C)-алкилгетероариламино, гетероарил-(1-6C)алкиламино, N-(1-6C)-алкилгетероарил-(1-6C)алкиламино, гетероарилкарбониламино, гетероарилсульфониламино, N-гетероарилкарбамоилом, N-гетероарилсульфамоилом, гетероарил-(2-6С)алканоиламино, гетероциклилом, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6С)алкилгетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6С)алкилгетероциклил-(1-6C)-алкиламино, гетероциклилкарбониламино, гетероциклилсульфони-ламино, N-гетероциклилкарбамоилом, N-гетероциклилсульфамоилом или гетероциклил-(2-6С)алканоиламино,
и Q необязательно замещен 1, 2 или 3 заместителями, выбранными из гидрокси, галогена, трифторметила, циано, меркапто, нитро, амино, карбокси, карбамоила, формила, (1-6С)алкила, (2-6С)алкенила, (2-6С)алкинила, (1-6C)алкокси, (1-6С)алкилтио, (1-6С)алкилсульфинила, (1-6С)алкилсульфонила, (1-6С)алкиламино, ди[(1-6С)алкил]амино, (1-6С)алкоксикарбонила, N-(1-6С)алкилкарбамоила, N,N-ди[(1-6С)алкил]карбамоила, (2-6С)алканоила, (2-6С)алканоилокси, (1-6С)-алканоиламино, N-(1-6С)алкилсульфамоила, N,N-ди-[(1-6С)-алкил]сульфамоила, (1-6С)алкансульфониламино, N-(1-6С)алкил-(1-6С)алкансульфониламино, галоген-(1-6С)алкила, гидрокси-(1-6С)алкила, (1-6С)алкокси-(1-6С)алкила, циано-(1-6С)алкила, амино-(1-6С)алкила, (1-6С)алкиламино-(1-6С)алкила, ди-[(1-6С)алкил]амино-(1-6С)алкила, карбокси-(1-6С)алкила, (1-6С)алкоксикарбонил-(1-6С)алкила, карбамоил-(1-6С)алкила, N-(1-6С)алкилкарбамоил-(1-6С)алкила, N,N-ди-[(1-6С)алкил]-карбамоил-(1-6С)алкила, галоген-(2-6С)алкокси, гидрокси-(2-6С)алкокси, (1-6С)алкокси-(2-6С)алкокси, циано-(1-6С)алкокси, карбокси-(1-6С)алкокси, (1-6С)алкоксикарбонил-(1-6С)алкокси, карбамоил-(1-6С)алкокси, N-(1-6C)алкилкарбамоил-(1-6С)алкокси, N,N-ди-[(1-6C)алкил]карбамоил-(1-6C)алкокси, амино-(2-6С)-алкокси, (1-6С)алкиламино-(2-6С)алкокси, ди-[(1-6C)алкил]-амино-(2-6С)алкокси, галоген-(2-6С)алкиламино, гидрокси-(2-6С)алкиламино, (1-6С)алкокси-(2-6С)алкиламино, циано-(1-6C)-алкиламино, карбокси-(1-6C)алкиламино, (1-6С)алкоксикарбонил-(1-6С)алкиламино, карбамоил-(1-6С)алкиламино, N-(1-6С)алкилкарбамоил-(1-6C)алкиламино, N,N-ди-[(1-6C)алкил]карбамоил-(1-6С)алкиламино, амино-(2-6С)алкиламино, (1-6C)алкиламино-(2-6С)алкиламино, ди-[(1-6C)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкилгалоген-(1-6С)алкиламино, N-(1-6C)алкилгидрокси-(2-6С)алкиламино, N-(1-6C)алкил-(1-6C)алкокси-(2-6С)алкиламино, N-(1-6С)алкилциано-(1-6С)алкиламино, N-(1-6C)алкилкарбокси-(1-6С)алкиламино, N-(1-6С)алкил-(1-6C)алкоксикарбонил-(1-6С)алкиламино, N-(1-6C)алкилкарбамоил-(1-6C)алкиламино, N-(1-6С)алкил-N-(1-6C)алкилкарбамоил-(1-6C)алкиламино, N-(1-6С)алкил-N,N-ди[(1-6C)алкил]карбамоил-(1-6C)алкиламино, N-(1-6C)алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-(1-6C)-алкиламино-(2-6С)алкиламино, N-(1-6С)алкил-ди-[(1-6C)алкил]-амино-(2-6С)алкиламино, галоген-(2-6С)алканоиламино, гидрокси-(2-6С)алканоиламино, (1-6С)алкокси-(2-6С)алканоиламино, циано-(2-6С)алканоиламино, карбокси-(2-6С)алканоиламино, (1-6С)алкоксикарбонил-(2-6С)алканоиламино, карбамоил-(2-6С)-алканоиламино, N-(1-6C)алкилкарбамоил-(2-6С)алканоиламино, N,N-ди-[(1-6C)алкил]карбамоил-(2-6С)алканоиламино, амино-(2-6С)алканоиламино, (1-6С)алкиламино-(2-6С)алканоиламино, ди[(1-6C)алкил]амино-(2-6С)алканоиламино, арила, арил-(1-6С)-алкила, арил-(1-6С)алкокси, арилокси, ариламино, N-(1-6С)алкилариламино, арил-(1-6C)алкиламино, N-(1-6С)алкиларил-(1-6C)алкиламино, ароиламино, арилсульфониламино, N-арилсульфамоила, арил-(2-6С)алканоиламино, гетероарила, гетероарил-(1-6С)алкила, гетероарилокси, гетероарил-(1-6C)-алкокси, гетероариламино, N-(1-6C)алкилгетероариламино, гетероарил-(1-6С)алкиламино, N-(1-6С)алкилгетероарил-(1-6С)-алкиламино, гетероарилкарбониламино, гетероарилсульфониламино, N-гетероарилсульфамоила, гетероарил-(2-6С)алканоиламино, гетероарил-(1-6С)алкокси-(1-6С)алкила, гетероарил-(1-6С)-алкиламино-(1-6C)алкила, N-(1-6С)алкилгетероарил-(1-6С)-алкиламино-(1-6C)алкила, гетероциклила, гетероциклил-(1-6C)-алкила, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6С)алкилгетероциклиламино, гетероциклил-(1-6С)алкиламино, N-(1-6С)алкилгетероциклил-(1-6С)алкиламино, гетероциклилкарбониламино, гетероциклилсульфониламино, N-гетероциклилсульфамоила, гетероциклил-(2-6С)алканоиламино, гетероциклил-(1-6С)алкокси-(1-6С)алкила, гетероциклил-(1-6С)-алкиламино-(1-6С)алкила и N-(1-6C)алкилгетероциклил-(1-6C)-алкиламино-(1-6C)алкила,
или Q замещен (1-3С)алкилендиоксигруппой,
и где любой заместитель радикала Q, определенный выше, который содержит СН2-группу, которая присоединена к 2 атомам углерода, или СН3-группу, которая присоединена к атому углерода, может необязательно иметь на каждой указанной СН2- или СН3-группе заместитель, выбранный из гидрокси, амино, (1-6С)алкокси, (1-6C)алкиламино, ди-[(1-6C)алкил]амино и гетероциклила,
и где любая арильная, гетероарильная или гетероциклильная группа в заместителе радикала Q может необязательно иметь 1 или 2 заместителя, выбранных из гидрокси, галогена, (1-6С)алкила, (1-6C)алкокси, карбокси, (1-6C)алкоксикарбонила, N-(1-6C)алкилкарбамоила, N,N-ди-[(1-6C)алкил]карбамоила, (2-6С)алканоила, амино, (1-6C)алкиламино, ди-[(1-6C)алкил]амино, галоген-(1-6C)алкила, гидрокси-(1-6C)алкила, (1-6С)алкокси-(1-6С)алкила, циано-(1-6С)алкила, амино-(1-6С)алкила, (1-6C)-алкиламино-(1-6С)алкила, ди-[(1-6С)алкил]амино-(1-6С)алкила, арила и арил-(1-6С)алкила;
или его фармацевтически приемлемая соль или in vivo расщепляемый сложный эфир;
за исключением 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В данном описании термин (1-6С)алкил включает алкильные группы с прямой или разветвленной цепью, такие как пропил, изопропил и трет-бутил, и (3-6С)циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил и циклогексил. Однако ссылки на конкретные алкильные группы, такие как «пропил», определены только для соединений с прямой цепью, ссылки на конкретные разветвленные алкильные группы, такие как «изопропил», определены только для соединений с разветвленной цепью и ссылки на конкретные циклоалкильные группы, такие как «циклопентил», определены только для 5-членных колец. Аналогичные условия применяются и для других общих терминов, например, (1-6С)алкокси включает метокси, этокси, циклопропилокси и циклопентилокси, (1-6С)алкиламино включает метиламино, этиламино, циклобутиламино и циклогексиламино и ди-[(1-6С)алкил]амино включает диметиламино, диэтиламино, N-циклобутил-N-метиламино и N-циклогексил-N-этиламино.
Понятно, что поскольку некоторые из соединений формулы I, определенных выше, могут существовать в оптически активных или рацемических формах благодаря одному или более асимметричным атомам углерода, данное изобретение включает любые подобные оптически активные или рацемические формы, которые обладают свойством ингибировать цитокины, в частности TNF. Синтез оптически активных форм может проводиться стандартными методами органической химии, хорошо известными в данной области, например синтезом из оптически активных исходных материалов или разделением рацемических форм. Также ингибирующие свойства в отношении TNF могут быть оценены с помощью стандартных лабораторных методов, представленных в данном описании.
Подходящие значения общих радикалов, описанные выше, включают представленные ниже.
Подходящим значением для R1 или Q, если он является арилом, для заместителя радикала Q, если он является арилом, или для арильной группы в заместителе R1 или Q радикала или в заместителе радикала Q является, например, фенил, инденил, инданил, нафтил, тетрагидронафтил или флуоренил, предпочтительно фенил.
Подходящим значением для R1 или Q, если он является гетероарилом, для гетероарильной группы в заместителе R1 или Q группы, для заместителя радикала Q, если он является гетероарилом или для гетероарильной группы в заместителе радикале Q является, например, ароматическое 5- или 6-членное моноциклическое кольцо, 9- или 10-членное бициклическое кольцо или 13-или 14-членное трициклическое кольцо, каждое из которых имеет вплоть до 5 гетероатомов в кольце, выбранных из кислорода, азота и серы, например фурил, пирролил, тиенил, оксазолил, изоксазолил, имидазолил, пиразолил, тиазолил, изотиазолил, оксадиазолил, тиадиазолил, триазолил, тетразолил, пиридил, пиридазинил, пиримидинил, пиразинил, 1,3,5-триазенил, бензофуранил, индолил, бензотиенил, бензоксазолил, бензимидазолил, бензотиазолил, индазолил, бензофуразанил, хинолил, изохинолил, хиназолинил, хиноксалинил, циннолинил, нафтиридинил, карбазолил, дибензофуранил, дибензотиофенил, S,S-диоксодибензотиофенил, ксантенил, дибензо-1,4-диоксинил, феноксатиинил, феноксазинил, дибензотиинил, фенотиазинил, тиантранил, бензофуропиридил, пиридоиндолил, акридинил или фенантридинил, предпочтительно фурил, тиенил, оксазолил, изоксазолил, имидазолил, пиразолил, тиазолил, изотиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, бензофуранил, индолил, бензотиенил, бензоксазолил, бензимидазолил, бензотиазолил, индазолил, бензофуразанил, хинолил, изохинолил, хиназолинил, хиноксалинил, нафтиридинил, карбазолил, дибензофуранил, дибензотиофенил или ксантенил, более предпочтительно фурил, тиенил, изоксазолил, тиазолил, пиридил, бензотиенил, бензофуразанил, хинолил, карбазолил, дибензофуранил или дибензотиофенил.
Подходящим значением для R1 или Q, если он является гетероциклилом, для заместителя радикала Q, если он является гетероциклилом, или для гетероциклильной группы в заместителе R1 или Q радикале или в заместителе радикала Q является, например, неароматическое насыщенное или частично насыщенное от 3-до 10-членное моноциклическое или бициклическое кольцо, содержащее вплоть до 5 гетероатомов, выбранных из кислорода, азота и серы, например оксиранил, оксетанил, азетидинил, тетрагидрофуранил, тетрагидропиранил, пирролинил, пирролидинил, имидазолинил, имидазолидинил, пиразолинил, пиразолидинил, 1,1-диоксидоизотиазолидинил, морфолинил, тетрагидро-1,4-тиазинил, 1,1-диоксотетрагидро-1,4-тиазинил, пиперидинил, гомопиперидинил, пиперазинил, гомопиперазинил, дигидропиридинил, тетрагидропиридинил, дигидропиримидинил или тетрагидропиримидинил или их бензопроизводные, такие как 2,3-дигидробензофуранил, 2,3-дигидробензотиенил, индолинил, изоиндолинил, хроманил и изохроманил, предпочтительно азетидин-1-ил, 3-пирролин-1-ил, пирролидин-1-ил, пирролидин-2-ил, 1,1-диоксидоизотиазолидин-2-ил, морфолино, 1,1-диоксотетрагидро-4Н-1,4-тиазин-4-ил, пиперидин-3-ил, пиперидин-4-ил, гомопиперидин-1-ил, пиперидино, пиперазин-1-ил или гомопиперазин-1-ил. Подходящим значением для такой группы, которая имеет 1 или 2 заместителя, выбранных из оксо- или тиоксогруппы, является, например, 2-оксопирролидинил, 2-тиоксопирролидинил, 2-оксоимидазолидинил, 2-тиоксоимидазолидинил, 2-оксопиперидинил, 2,5-диоксопирролидинил, 2,5-диоксоимидазолидинил или 2,6-диоксопиперидинил.
Подходящим значением для Q, если он является (3-7С)-циклоалкилом, является, например, неароматическое моно- или бициклическое кольцо, содержащее от 3 до 7 атомов углерода, такое как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или бицикло[2.2.1]гептил, предпочтительно циклобутил, циклопентил, циклогексил или циклогептил, более предпочтительно циклогексил.
Подходящими значениями для R1, R2 или R3 групп, или для различных заместителей радикала Q или на арильной, гетероарильной или гетероциклильной группе в R1 или на арильной, гетероарильной или гетероциклилной группе в составе заместителя на Q являются:
для галогена: фтор, хлор, бром и йод;
для (1-6С)алкила: метил, этил, пропил, изопропил, трет-бутил, циклобутил, циклопентил или циклогексил;
для (2-6С)алкенила: винил и аллил;
для (2-6С)алкинила: этинил и 2-пропинил;
для (1-6С)алкокси: метокси, этокси, пропокси, изопропокси, циклопропилокси, бутокси, циклобутокси и циклопентилокси;
для (1-6С)алкиламино: метиламино, этиламино, пропиламино, циклобутиламино и циклогексиламино;
для ди-[(1-6С)алкил]амино: диметиламино, диэтиламино и N-этил-N-метиламино;
для (1-6С)алкоксикарбонила: метоксикарбонил, этоксикарбонил, пропоксикарбонил и трет-бутоксикарбонил;
для N-(1-6С)алкилкарбамоила: N-метилкарбамоил, N-этилкарбамоил и N-пропилкарбамоил;
для N,N-ди-[(1-6С)алкил]карбамоила: N,N-диметилкарбамоил, N-этил-N-метилкарбамоил и N,N-диэтилкарбамоил;
для (2-6С)алканоила: ацетил и пропионил;
для галоген-(1-6С)алкила: фторметил, хлорметил, бромметил, дифторметил, дихлорметил, дибромметил, 2-фторэтил, 2-хлорэтил и 2-бромэтил;
для гидрокси-(1-6С)алкила: гидроксиметил, 2-гидроксиэтил, 1-гидроксиэтил и 3-гидроксипропил;
для (1-6С)алкокси-(1-6С)алкила: метоксиметил, этоксиметил, 1-метоксиэтил, 2-метоксиэтил, 2-этоксиэтил и 3-метоксипропил;
для циано-(1-6С)алкила: цианометил, 2-цианоэтил, 1-цианоэтил и 3-цианопропил;
для амино-(1-6С)алкила: аминометил, 2-аминоэтил, 1-аминоэтил и 3-аминопропил;
для (1-6С)алкиламино-(1-6С)алкила: метиламинометил, этиламинометил, 1-метиламиноэтил, 2-метиламиноэтил, 2-этиламиноэтил и 3-метиламинопропил;
для ди-[(1-6С)алкил]амино-(1-6С)алкила: диметиламинометил, диэтиламинометил, 1-диметиламиноэтил, 2-диметиламиноэтил и 3-диметиламинопропил.
Подходящими значениями для R1 или Q и подходящими значениями для заместителя на R1 или Q являются:
для арил-(1-6С)алкила: бензил, 2-фенилэтил, 2-фенилпропил и 3-фенилпропил;
для арил-(1-6С)алкокси: бензилокси и 2-фенилэтокси;
для арилокси: фенокси и 2-нафтилокси;
для ариламино: анилино;
для N- (1-6C)алкилариламино: N-метиланилино и N-этиланилино;
для арил-(1-6С)алкиламино: бензиламино, 2-фенетиламино, 2-фенилпропиламино и 3-фенилпропиламино;
для N-(1-6С)алкиларил-(1-6С)алкиламино: N-бензил-N-метиламино;
для ароиламино: бензамидо и 2-нафтоиламино;
для арилсульфониламино: бензолсульфониламидо;
для N-арилкарбамоила: N-фенилкарбамоил;
для N-арилсульфамоила: N-фенилсульфамоил;
для арил-(2-6С)алканоиламино: фенилацетамидо и 3-фенилпропионамидо;
для гетероарил-(1-6С)алкила: гетероарилметил, 2-гетероарилэтил, 2-гетероарилпропил и 3-гетероарилпропил;
для гетероарил-(1-6C)алкокси: гетероарилметокси и 2-гетероарилэтокси;
для N-(1-6С)алкилгетероариламино: N-метилгетероариламино;
для гетероарил-(1-6C)алкиламино: гетероарилметиламино, 2-гетероарилэтиламино и 3-гетероарилпропиламино;
для N-(1-6C)алкилгетероарил-(1-6C)алкиламино: N-метилгетероарилметиламино и N-метил-2-гетероарилэтиламино;
для гетероарил-(2-6С)алканоиламино: гетероарилацетамидо и 3-гетероарилпропионамидо;
для гетероарил-(1-6C)алкокси-(1-6C)алкила: гетероарилметоксиметил, 2-гетероарилэтоксиметил и 3-гетероарилпропоксиметил;
для гетероарил-(1-6С)алкиламино-(1-6С)алкила: гетероарилметиламинометил, 2-гетероарилэтиламинометил и 3-гетероарилпропиламинометил;
для N-(1-6С)алкилгетероарил-(1-6С)алкиламино-(1-6С)алкила: N-гетероарилметил-N-метиламинометил, N-(2-гетероарилэтил)-N-метиламинометил и N-(3-гетероарилпропил)-N-метиламинометил;
для гетероциклил-(1-6С)алкила: гетероциклилметил, 2-гетероциклилэтил, 2-гетероциклилпропил и 3-гетероциклилпропил;
для гетероциклил-(1-6С)алкокси: гетероциклилметокси и 2-гетероциклилэтокси;
для N-(1-6С)алкилгетероциклиламино: N-метилгетероциклиламино;
для гетероциклил-(1-6С)алкиламино: гетероциклилметиламино, 2-гетероциклилэтиламино и 3-гетероциклилпропиламино;
для N-(1-6С)алкилгетероциклил-(1-6С)алкиламино: N-метилгетероциклилметиламино и N-метил-2-гетероциклилэтиламино;
для гетероциклил-(2-6С)алканоиламино: гетероциклилацетамидо и 3-гетероциклилпропионамидо;
для гетероциклил-(1-6С)алкокси-(1-6С)алкила: гетероциклилметоксиметил, 2-гетероциклилэтоксиметил и 3-гетероциклилпропоксиметил;
для гетероциклил-(1-6С)алкиламино-(1-6С)алкила: гетероциклилметиламинометил, 2-гетероциклилэтиламинометил и 3-гетероциклилэтиламинометил;
для N-(1-6C)алкилгетероциклил-(1-6С)алкиламино-(1-6С)-алкила: N-гетероциклилметил-N-метиламинометил, N-(2-гетеро-циклилэтил)-N-метиламинометил и N-(3-гетероциклилпропил)-N-метиламинометил;
для (1-3С)алкилендиокси: метилендиокси, этилендиокси и триметилендиокси;
для (1-6С)алкилтио: метилтио, этилтио и пропилтио;
для (1-6С)алкилсульфинила: метилсульфинил, этилсульфинил и пропилсульфинил;
для (1-6C)алкилсульфонила: метилсульфонил, этилсульфонил и пропилсульфонил;
для (2-6С)алканоилокси: ацетокси и пропионилокси;
для (1-6С)алканоиламино: формамидо, ацетамидо и пропионамидо;
для N- (1-6C)алкил-(1-6C)алканоиламино: N-метилацетамидо и N-метилпропионамидо;
для N-(1-6C)алкилсульфамоила: N-метилсульфамоил и N-этилсульфамоил;
для N,N-ди-[(1-6C)алкил]сульфамоила: N,N-диметилсульфамоил;
для (1-6C)алкансульфониламино: метансульфонамидо и этансульфонамидо;
для N-(1-6C)алкил-(1-6C)алкансульфониламино: N-метилметансульфониламино и N-метилэтансульфониламино;
для карбокси-(1-6C)алкила: карбоксиметил, 1-карбоксиэтил, 2-карбоксиэтил, 3-карбоксипропил и 4-карбоксибутил;
для (1-6С) алкоксикарбонил-(1-6С)алкила: метоксикарбонилметил, этоксикарбонилметил, трет-бутоксикарбонилметил, 1-метоксикарбонилэтил, 1-этоксикарбонилэтил, 2-метоксикарбонилэтил, 2-этоксикарбонилэтил, 3-метоксикарбонилпропил и 3-этоксикарбонилпропил;
для карбамоил-(1-6С)алкила: карбамоилметил, 1-карбамоилэтил, 2-карбамоилэтил и 3-карбамоилпропил;
для N-(1-6С)алкилкарбамоил-(1-6С)алкила: N-метилкарбамоилметил, N-этилкарбамоилметил, N-пропилкарбамоилметил, 1-(N-метилкарбамоил)этил, 1-(N-этилкарбамоил)этил, 2-(N-метилкарбамоил)этил, 2-(N-этилкарбамоил)этил и 3-(N-метилкарбамоил)пропил;
для N,N-ди-[(1-6С)алкил]карбамоил-(1-6С)алкила: N,N-диметилкарбамоилметил, N-этил-N-метилкарбамоилметил, N,N-диэтилкарбамоилметил, 1-(N,N-диметилкарбамоил)этил, 1-(N,N-диэтилкарбамоил)этил, 2-(N,N-диметилкарбамоил)этил, 2-(N,N-диэтилкарбамоил)этил, 3-(N,N-диметилкарбамоил)пропил и 4-(N,N-диметилкарбамоил)бутил;
для галоген-(2-6С)алкокси: 2-хлорэтокси, 2-бромэтокси, 3-хлорпропокси, 1,1,2,2-тетрафторэтокси и 2,2,2-трифторэтокси;
для гидрокси-(2-6С)алкокси: 2-гидроксиэтокси, 3-гидроксипропокси, 2-гидрокси-1-метилэтокси, 2-гидрокси-2-пропокси и 4-гидроксибутокси;
для (1-6С)алкокси-(2-6С)алкокси: 2-метоксиэтокси, 2-этоксиэтокси, 3-метоксипропокси, 2-метокси-1-метилэтокси и 4-этоксибутокси;
для циано-(1-6С)алкокси: цианометокси, 2-цианоэтокси и 3-цианопропокси;
для карбокси-(1-6С)алкокси: карбоксиметокси, 1-карбоксиэтокси, 2-карбоксиэтокси и 3-карбоксипропокси;
для (1-6С)алкоксикарбонил-(1-6С)алкокси: метоксикарбонилметокси, этоксикарбонилметокси, трет-бутоксикарбонилметокси, 2-метоксикарбонилэтокси и 3-этоксикарбонилпропокси;
для карбамоил-(1-6С)алкокси: карбамоилметокси и 2-карбамоилэтокси;
для N-(1-6C)алкилкарбамоил-(1-6С)алкокси: N-метилкарбамоилметокси, 2-(N-этилкарбамоил)этокси и 3-(N-метилкарбамоил)пропокси;
для N,N-ди[((1-6С)алкил]карбамоил-(1-6С)алкокси: N,N-диметилкарбамоилметокси, 2-(N,N-диметилкарбамоил)этокси и 3-(N,N-диэтилкарбамоил)пропокси;
для амино-(2-6С)алкокси: 2-аминоэтокси, 2-амино-1-метилэтокси, 3-аминопропокси, 2-амино-2-метоксипропокси и 4-аминобутокси;
для (1-6С)алкиламино-(2-6С)алкокси: 2-метиламиноэтокси, 2-метиламино-1-метилэтокси и 3-этиламинопропокси;
для ди-[(1-6С)алкил]амино-(2-6С)алкокси: 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 2-диметиламинопропокси, 2-диметиламино-2-метилэтокси, 3-диметиламинопропокси и 4-диметиламинобутокси;
для галоген-(2-6С)алкиламино: 2-фторэтиламино, 2-хлорэтиламино, 2-бромэтиламино, 3-фторпропиламино и 3-хлорпропиламино;
для гидрокси-(2-6С)алкиламино: 2-гидроксиэтиламино, 3-гидроксипропиламино, 2-гидрокси-2-метилпропиламино и 4-гидроксибутиламино;
для (1-6С)алкокси-(2-6С)алкиламино: 2-метоксиэтиламино, 2-этоксиэтиламино, 3-метоксипропиламино и 3-этоксипропиламино;
для циано-(1-6С)алкиламино: цианометиламино, 2-цианоэтиламино и 3-цианопропиламино;
для карбокси-(1-6С)алкиламино: карбоксиметиламино, 1-карбоксиэтиламино, 2-карбоксиэтиламино и 3-карбоксипропиламино;
для (1-6С)алкоксикарбонил-(1-6С)алкиламино: метоксикарбонилметиламино, 2-(этоксикарбонил)этиламино и 3-(трет-бутоксикарбонил)пропиламино;
для карбамоил-(1-6С)алкиламино: карбамоилметиламино и 2-карбамоилэтиламино;
для N-(1-6С)алкилкарбамоил-(1-6С)алкиламино: N-метилкарбамоилметиламино, N-этилкарбамоилметиламино и 2-(N-метилкарбамоил)этиламино;
для N,N-ди-[(1-6С)алкил]карбамоил-(1-6С)алкиламино: N,N-диметилкарбамоилметиламино, N,N-диэтилкарбамоилметиламино и 2-(N,N-диметилкарбамоил)этиламино;
для амино-(2-6С)алкиламино: 2-аминоэтиламино, 3-аминопропиламино, 2-амино-2-метилпропиламино и 4-аминобутиламино;
для (1-6С)алкиламино-(2-6С)алкиламино: 2-метиламиноэтиламино, 2-этиламиноэтиламино, 2-пропиламиноэтиламино, 3-метиламинопропиламино, 3-этиламинопропиламино, 2-метиламино-2-метилпропиламино и 4-метиламинобутиламино;
для ди[(1-6С)алкил]амино-(2-6С)алкиламино: 2-диметиламиноэтиламино, 2-(N-этил-N-метиламино)этиламино, 2-диэтиламиноэтиламино, 2-дипропиламиноэтиламино, 3-диметиламинопропиламино, 3-диэтиламинопропиламино, 2-диметиламино-2-метилпропиламино и 4-диметиламинобутиламино;
для N-(1-6С)алкилгалоген-(2-6С)алкиламино: N-(2-хлорэтил)-N-метиламино, N-(2-бромэтил)-N-метиламино и N-(2-бромэтил)-N-этиламино;
для N-(1-6С)алкилгидрокси-(2-6С)алкиламино: N-(2-гидроксиэтил)-N-метиламино, N-(3-гидроксипропил)-N-метиламино и N-этил-N-(2-гидроксиэтил)амино;
для N-(1-6С)алкил-(1-6С)алкокси-(2-6С)алкиламино: N-метил-N-(2-метоксиэтил)амино, N-метил-N-(3-метоксипропил)амино и N-этил-N-(2-метоксиэтил)амино;
для N-(1-6С)алкилциано-(1-6С)алкиламино: N-(цианометил)-N-метиламино;
для N-(1-6С)алкилкарбокси-(1-6С)алкиламино: N-карбоксиметил-N-метиламино и N-(2-карбоксиэтил)-N-метиламино;
для N-(1-6C)алкил-(1-6С)алкоксикарбонил-(1-6С)алкиламино: N-метоксикарбонилметил-N-метиламино, N-(2-этоксикарбонилэтил)-N-этиламино и N-(2-трет-бутоксикарбонилэтил)-N-метиламино;
для N-(1-6С)алкилкарбамоил-(1-6С)алкиламино: N-карбамоилметил-N-метиламино и N-(2-карбамоилэтил)-N-метиламино;
для N-(1-6С)алкил-N-(1-6С)алкилкарбамоил-(1-6С)алкиламино: N-(N-метилкарбамоилметил)-N-метиламино, N-(N-этилкарбамоилметил)-N-метиламино и N-[2-(N-метилкарбамоил)этил]-N-метиламино;
для N-(1-6С)алкил-N,N-ди-[(1-6С)алкил]карбамоил-(1-6С)-алкиламино: N-(N,N-диметилкарбамоилметил)-N-метиламино и N-[2-(N,N-диметилкарбамоил)этил]-N-метиламино;
для N-(1-6С)алкиламино-(2-6С)алкиламино: N-(2-аминоэтил)-N-метиламино, N-(3-аминопропил)-N-метиламино и N-(4-аминобутил)-N-метиламино;
для N-(1-6С)алкил-(1-6С)алкиламино-(2-6С)алкиламино: N-(2-метиламиноэтил)-N-метиламино, N-(2-метиламиноэтил)-N-метиламино, N-(3-метиламинопропил)-N-метиламино, N-(3-этиламинопропил)-N-этиламино и N-(4-метиламинобутил)-N-метиламино;
для N-(1-6С)алкил-ди((1-6С)алкил]амино-(2-6С)алкиламино:
N-(2-диметиламиноэтил)-N-метиламино, N-(2-диэтиламиноэтил)-N-метиламино, N-(3-диметиламинопропил)-N-метиламино и N-(4-диметиламинобутил)-N-метиламино;
для галоген-(2-6С)алканоиламино: 2-хлорацетамидо и 3-хлорпропионамидо;
для гидрокси-(2-6С)алканоиламино: 2-гидроксиацетамидо и 3-гидроксипропионамидо;
для (1-6С)алкокси-(2-6С)алканоиламино: 2-метоксиацетамидо и 3-метоксипропионамидо;
для циано-(2-6С)алканоиламино: 2-цианоацетамидо и 3-цианопропионамидо;
для карбокси-(2-6С)алканоиламино: 2-карбоксиацетамидо и 3-карбоксипропионамидо;
для (1-6С)алкоксикарбонил-(2-6С)алканоиламино: 2-метоксикарбонилацетамидо, 2-(трет-бутоксикарбонил)ацетамидо и 3-метоксикарбонилпропионамидо;
для карбамоил-(2-6С)алканоиламино: 2-карбамоилацетамидо, 3-карбамоилпропионамидо и 4-карбамоилбутирамидо;
для N-(1-6С)алкилкарбамоил-(2-6С)алканоиламино: 2-(N-метилкарбамоил)ацетамидо и 3-(N-этилкарбамоил)пропионамидо;
для N,N-ди-[(1-6С)алкил]карбамоил-(2-6С)алканоиламино: 2-(N,N-диметилкарбамоил)ацетамидо, 2-(N,N-диэтилкарбамоил)ацетамидо и 3-(N,N-диметилкарбамоил)пропионамидо;
для амино-(2-6С)алканоиламино: 2-аминоацетамидо, 2-аминопропионамидо и 3-аминопропионамидо;
для (1-6С)алкиламино-(2-6С)алканоиламино: 2-метиламиноацетамидо, 2-этиламиноацетамидо, 2-метиламинопропионамидо и 3-метиламинопропионамидо;
для ди-[(1-6С)алкил]амино-(2-6С)алканоиламино: 2-диметиламиноацетамидо, 2-диэтиламиноацетамидо, 2-диметиламинопропионамидо и 3-диметиламинопропионамидо.
Когда, как определено выше, любой из заместителей радикалов R1 или Q, который содержит СН2-группу, которая присоединена к 2 атомам углерода, или СН3-группу, которая присоединена к атому углерода, может необязательно иметь на каждой указанной CH2 или СН3 группе заместитель, выбранный из гидрокси, амино, (1-6С)алкокси, (1-6С)алкиламино, ди-[(1-6С)алкил]амино и гетероциклила, такими подходящими заместителями являются, например, замещенные гетероциклил-(1-6С)алкоксигруппы, такие как 2-гидрокси-3-пиперидинопропокси и 2-гидрокси-3-морфолинопропокси, замещенные (1-6С)алкиламино-(2-6С)алкоксигруппы, такие как 2-гидрокси-3-метиламинопропокси, замещенные ди-[(1-6С)алкил]амино-(2-6С)алкоксигруппы, такие как 3-диметиламино-2-гидроксипропокси, 3-[N-(3-диметиламинопропил)-N-метиламино]пропокси и 3-[N-(3-диметиламинопропил)-N-метиламино]-2-гидроксипропокси, замещенные гетероциклил-(1-6С)алкиламиногруппы, такие как 2-гидрокси-3-пиперидинопропиламино и 2-гидкрокси-3-морфолинопропиламино, замещенные амино-(2-6С)алкиламиногруппы, такие как 3-амино-2-гидроксипропиламино, замещенные (1-6С)алкиламино-(2-6С)-алкиламиногруппы, такие как 2-гидрокси-3-метиламинопропиламино, замещенные ди-[(1-6С)алкил]-амино-(2-6C)-алкиламиногруппы, такие как 3-диметиламино-2-гидрокси-пропиламино, 3-[N-(3-диметиламинопропил)-N-метиламино]пропиламино и 3-[N-(3-диметиламинопропил)-N-метиламино]-2-гидроксипропиламино, и замещенные (1-6С)алкиламино-(1-6С)алкильные группы, такие как 2-диметиламиноэтиламинометил, 3-диметиламинопропиламинометил, 3-диметиламино-2,2-диметилпропиламинометил, 2-морфолиноэтиламинометил, 2-пиперазин-1-илэтиламинометил и 3-морфолинопропиламинометил.
Подходящей фармацевтически приемлемой солью соединения формулы Ia или Ib является, например, кислотно-аддитивная соль соединения формулы Ia или Ib, которое является достаточно основным, например кислотно-аддитивная соль с органической или неорганической кислотой, такой как соляная, бромистоводородная, серная, трифторуксусная, лимонная или малеиновая кислота, или, например, соль соединения формулы Ia или Ib, которое является достаточно кислым, например, соль с щелочным или щелочноземельным металлом, такая как кальциевая или магниевая соль, или аммониевая соль, или соль с органическим основанием, таким как метиламин, диметиламин, триметиламин, пиперидин, морфолин или трис-(2-гидроксиэтил)амин.
В данной области техники известны различные формы пролекарств. Примеры таких пролекарств можно найти в
a) Design of Prodrugs под редакцией H.Bundgaard (Elsevier, 1985) и Methods in Enzymology, том 42, стр. 309-396, под редакцией К. Widder, et al. (Academic Press, 1985);
b) A Textbook of Drug Design and Development под редакцией Krogsgaard-Larsen и H.Bungaard, глава 5 «Design and Application of Prodrugs», H. Bundgaard, стр. 113-191 (1991);
c) H.Bundgaard, Advanced Drug Delivery Reviews, 8, 1-38 (1992);
d) H.Bungaard, et al., Journal of Pharmaceutical Sciences, 77, 285 (1988) и
e) N.Kakeya, et al., Chem. Pharm. Bull., 32, 692 (1984).
Примеры таких пролекарств могут быть использованы для образования in vivo расщепляемых сложных эфиров соединения формулы Ia или Ib. In vivo расщепляемым эфиром соединения формулы Ia или Ib, содержащим карбоксильную группу, является, например, фармацевтически приемлемый сложный эфир, который расщепляется в организме человека или животного с образованием родительской кислоты. Подходящие фармацевтически приемлемые сложные эфиры для карбокси включают (1-6С)-алкоксиметиловые эфиры, например метоксиметил; (1-6С)-алканоилоксиметиловые эфиры, например пивалоилоксиметил; фталидиловые эфиры; (3-8С)циклоалкоксикарбонилокси(1-6С)-алкиловые эфиры, например 1-циклогексилкарбонилоксиэтил; 1,3-диоксолан-2-илметиловые эфиры, например 5-метил-1,3-диоксолан-2-илметил; (1-6С)алкоксикарбонилоксиэтиловые эфиры, например 1-метоксикарбонилоксиэтил, и могут быть образованы на любой карбоксильной группе в соединениях данного изобретения.
Конкретные новые соединения данного изобретения включают, например, подходящие амидные производные соединений формулы Ia или Ib или их фармацевтически приемлемые соли, где
(a) R3 является водородом или (1-6С)алкилом, таким как метил, этил, пропил и изопропил, предпочтительно R3 является водородом, метилом или этилом, более предпочтительно водородом или метилом, и X, R1, R2, Q, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(b) Q является фенилом или гетероароматическим 5- или 6-членным моноциклическим кольцом или 9- или 10-членным бициклическим кольцом, содержащим вплоть до пяти гетероатомов в кольце, выбранных из кислорода, азота и серы, которые имеют основной заместитель, выбранный из заместителей для Q, определенных выше, и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(c) Q является фенилом, инденилом, инданилом или флуоренилом, который необязательно имеет 1, 2 или 3 заместителя, выбранных из заместителей для Q, определенных выше, и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(d) Q является фенилом или гетероароматическим 5- или 6-членным моноциклическим кольцом или 9- или 10-членным бициклическим кольцом, содержащим вплоть до пяти гетероатомов в кольце, выбранных из кислорода, азота и серы, которые имеют основной заместитель, выбранный из амино, (1-6С)алкиламино, ди-[(1-6С)алкил]амино, амино-(1-6С)алкила, (1-6C)алкиламино-(1-6С)алкила, ди-[(1-6С)алкил]амино-(1-6С)алкила, амино-(2-6С)алкокси, (1-6С)алкиламино-(2-6С)алкокси, ди-[(1-6C)алкил]-амино-(2-6С)алкокси, амино-(2-6С)алкиламино, (1-6С)алкиламино-(2-6С)алкиламино, ди-[(1-6С)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкиламино-(2-6С)алкиламино, N-(1-6C)алкил- (1-6С)-алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-ди-[(1-6C)алкил]-амино-(2-6С)алкиламино, амино-(2-6С)алканоиламино, (1-6С)-алкиламино-(2-6С)алканоиламино, ди-[(1-6C)алкил]амино-(2-6C)-алканоиламино, гетероарила, гетероарил-(1-6C)алкила, гетероарил-(1-6С)алкокси, гетероциклила, гетероциклил-(1-6С)-алкила и гетероциклил-(1-6С)алкокси, и где любая гетероарильная или гетероциклильная группа в основном заместителе на Q может необязательно иметь 1 или 2 заместителя, выбранные из галогена, (1-6С)алкила, (2-6С)алканоила, амино, (1-6С)алкиламино и ди-[(1-6С)алкил]амино, и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(е) Q является фенилом или гетероароматическим 5- или 6-членным моноциклическим кольцом или 9- или 10-членным бициклическим кольцом, содержащим вплоть до пяти гетероатомов в кольце, выбранных из кислорода, азота и серы, которые необязательно имеют 1, 2 или 3 заместителя, выбранные из гидрокси, галогена, трифторметила, циано, нитро, амино, карбокси, (1-6С) алкила, (1-6С) алкокси, (1-6С)алкиламино, ди-[(1-6С)-алкил]амино, (1-6С)алкоксикарбонила, (2-6С)алканоила, галоген-(1-6С)алкила, (1-6С)алкокси-(1-6С)алкила, амино-(1-6С)алкила, (1-6С)алкиламино-(1-6С)алкила, ди-[(1-6С)алкил]амино-(1-6С)-алкила, галоген-(2-6С)алкокси, гидрокси-(2-6С)алкокси, (1-6С)алкокси-(2-6С)алкокси, циано-(1-6С)алкокси, карбокси-(1-6С)алкокси, (1-6С)алкоксикарбонил-(1-6С)алкокси, амино-(2-6С)алкокси, (1-6С)алкиламино-(2-6С)алкокси, ди-[(1-6С)алкил]-амино-(2-6С)алкокси, пиридила, имидазолила, пиридил-(1-6С)алкила, имидазолил-(1-6С)алкила, пиридил-(1-6С)алкокси, имидазолил-(1-6С)алкокси, пирролидинила, пиперидинила, морфолинила, пиперазинила, 4-(1-6С)алкилпиперазинила, 4-(2-6C)алканоилпиперазинила, пирролидинил-(1-6C)алкила, пиперидинил-(1-6С)алкила, морфолинил-(1-6C)алкила, пиперазинил-(1-6С)алкила, 4-(1-6C)алкилпиперазинил-(1-6C)алкила, 4-(2-6C)-алканоилпиперазинил-(1-6C)алкила, пирролидинилокси, пипериди-нилокси, 1-(1-6C)алкилпиперидинилокси, пирролидинил-(2-6C)-алкокси, пиперидинил-(2-6C)алкокси, морфолинил-(2-6С)алкокси, пиперазинил-(2-6С)алкокси, 4-(1-6С)алкилпиперазинил-(2-6С) -алкокси и 4-(2-6С)алканоилпиперазинил-(2-6С)алкокси или Q имеет (1-3С)алкилендиоксизаместитель, и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(f) Q является фенилом, инденилом, инданилом, флуоренилом или гетероароматическим 5- или 6-членным моноциклическим кольцом, содержащим вплоть до 3 гетероатомов в кольце, выбранных из кислорода, азота и серы, которые необязательно имеют 1, 2 или 3 заместителя, выбранные из гидрокси, галогена, трифторметила, циано, нитро, амино, карбокси, (1-6С)алкила, (1-6С)алкокси, (1-6С)алкиламино, ди-[(1-6С)-алкил]амино, (1-6С)алкоксикарбонила, (2-6С)алканоила, (1-6C)-алканоиламино, N-(1-6С)алкил-(1-6С)алканоиламино, (1-6C)-алкансульфониламино, N-(1-6C)алкил-(1-6С)алкансульфониламино, фенила, фурила, тиенила, азетидинила, пирролинила, пирролидинила, 1,1-диоксидоизотиазолидинила, пиперидинила, гомопиперидинила, морфолинила, пиперазинила, гомопиперазинила, пирролидинил-(1-6C) алкила, пиперидинил-(1-6С)алкила, морфолинил-(1-6С)алкила и пиперазинил-(1-6С)алкила, и где любая фенильная, фурильная, тиенильная или гетероциклильная группа в заместителе на Q может необязательно иметь 1 или 2 заместителя, выбранных из галогена, (1-6С)алкила, (1-6С)алкокси и (2-6С)алканоила, и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(g) Q является фенилом, фурилом, тиенилом, оксазолилом, изоксазолилом, имидазолилом, пиразолилом, тиазолилом, изотиазолилом, пиридилом, пиридазинилом, пиримидинилом, пиразинилом, бензофуранилом, индолилом, бензотиенилом, бензоксазолилом, бензимидазолилом, бензотиазолилом, индазолилом, бензофуразанилом, хинолилом, изохинолилом, хиназолинилом, хиноксалинилом или нафтиридинилом, которые необязательно имеют 1 или 2 заместителя, выбранных из заместителей, определенных выше в параграфах (b), (d) или (е), и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(h) Q является фенилом, 2- или 3-фурилом, 2- или 3-тиенилом, 2, 4- или 5-оксазолилом, 3-, 4- или 5-изоксазолилом, 2-, 4- или 5-имидазолилом, 3- или 4-пиразолилом, 2-, 4- или 5-тиазолилом, 3-, 4- или 5-изотиазолилом, 2-, 3- или 4-пиридилом, 3- или 4-пиридазинилом, 2-, 4- или 5-пиримидинилом, 2-пиразинилом, 2-, 3-, 5- или 6-бензофуранилом, 2-, 3-, 5- или 6-индолилом, 2-, 3-, 5- или 6-бензотиенилом, 2-, 5- или 6-бензоксазолилом, 2-, 5- или 6-бензимидазолилом, 2-, 5- или 6-бензотиазолилом, 3-, 5- или 6-индазолилом, 5-бензофуразанилом, 2-, 3-, 6- или 7-хинолилом, 3-, 6- или 7-изохинолилом, 2-, 6- или 7-хиназолинилом, 2-, 6- или 7-хиноксалинилом или 1,8-нафтиридин-2-илом или 1,8-нафтиридин-3-илом, которые необязательно имеют 1 или 2 заместителя, выбранных из заместителей, определенных выше в параграфах (b), (d) и (е), и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(i) Q является гетероароматическим 5- или 6-членным моноциклическим кольцом, 9- или 10-членным бициклическим кольцом или 13- или 14-членным трициклическим кольцом, содержащим вплоть до пяти гетероатомов в кольце, выбранных из кислорода, азота и серы, которые необязательно имеют 1, 2 или 3 заместителя, выбранных из гидрокси, галогена, трифторметила, циано, нитро, амино, карбокси, (1-6С)алкила, (1-6С)алкокси, (1-3С)алкилендиокси, (1-6С)алкиламино, ди-[(1-6С)алкил]амино и (1-6С) алкоксикарбонила, и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(j) Q является гетероароматическим 13- или 14-членным трициклическим кольцом, содержащим вплоть до пяти гетероатомов в кольце, выбранных из кислорода, азота и серы, которые необязательно имеют 1, 2 или 3 заместителя, выбранных из гидрокси, галогена, трифторметила, циано, нитро, амино, карбокси, (1-6С)алкила, (1-6С)алкокси, (1-3С)алкилендиокси, (1-6С)-алкиламино, ди-[(1-6С)алкил]амино и (1-6С)алкоксикарбонила, и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(k) Q является фурилом, тиенилом, оксазолилом, изоксазолилом, имидазолилом, пиразолилом, тиазолилом, изотиазолилом, пиридилом, пиридазинилом, пиримидинилом, пиразинилом, бензофуранилом, индолилом, бензотиофенилом, бензоксазолилом, бензимидазолилом, бензотиазолилом, индазолилом, бензофуразанилом, хинолилом, изохинолилом, хиназолинилом, хиноксалинилом, нафтиридинилом, карбазолилом, дибензофуранилом, дибензотиофенилом или ксантенилом, которые необязательно имеют 1 или 2 заместителя, выбранных из заместителей, определенных выше в параграфе (i), и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(l) Q является 1-, 2- или 3-карбазолилом, 1-, 2-, 3- или 4-дибензофуранилом или 1-, 2-, 3- или 4-дибензотиофенилом, которые необязательно имеют 1 или 2 заместителя, выбранных из заместителей, определенных выше в параграфе (i), и X, R1, R2, R3, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(m) n равно 0 и X, R1, R3, Q, m и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(n) n равно 1 и R2 является галогеном или (1-6C)алкилом и X, R1, R3, Q, m и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(о) q равно 0 и X, R1, R2, R3, Q, m и n подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(р) m равно 1 и R1 является амино, (1-6С)алкиламино, ди-[(1-6С)алкил]амино, амино-(1-6С)алкилом, (1-6C)алкиламино-(1-6С)алкилом, ди-[(1-6С)алкил]амино-(1-6С)алкилом, амино-(2-6С)алкокси, (1-6С)алкиламино-(2-6С)алкокси, ди-[(1-6C)алкил]-амино-(2-6С)алкокси, амино-(2-6С)алкиламино, (1-6C)алкиламино-(2-6С)алкиламино, ди-[(1-6С)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-(1-6С)алкиламино- (2-6С)алкиламино, N-(1-6С)алкил-ди-[(1-6C)алкил]амино-(2-6С)алкиламино, гетероарилом, гетероарил-(1-6C)алкилом, гетероарил-(1-6C)алкокси, гетероциклилом, гетероциклил-(1-6С)алкилом, гетероциклилокси или гетероциклил-(1-6C)алкокси, и где любая гетероарильная или гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из гидрокси, галогена, (1-6С)алкила, (1-6C)алкокси, (2-6С)алканоила, амино, (1-6C)алкиламино и ди-[(1-6С)-алкил]амино, и X, R2, R3, Q, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(q) m равно 1 и R1 является амино, (1-6С)алкиламино, ди-[(1-6C)алкил]амино, амино-(1-6C)алкилом, (1-6C)алкиламино-(1-6С)алкилом, ди-[(1-6C)алкил]амино-(1-6C)алкилом, амино-(2-6С)-алкокси, (1-6С)алкиламино-(2-6С)алкокси, ди-[(1-6С)алкил]-амино-(2-6С)алкокси, амино-(2-6С)алкиламино, (1-6С)алкиламино-(2-6С)алкиламино, ди-[(1-6С)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкиламино-(2-6С)алкиламино, N-(1-6С)алкил-(1-6С)-алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-ди-[(1-6С)алкил]-амино-(2-6С)алкиламино, пиридилом, имидазолилом, пиридил-(1-6С)алкилом, имидазолил-(1-6С)алкилом, пиридил-(1-6С)алкокси, имидазолил-(1-6С)алкокси, пирролидинилом, пиперидинилом, морфолинилом, пиперазинилом, 4-(1-6C)алкилпиперазинилом, гомопиперазинилом, 4-(1-6C)алкилгомопиперазинилом, 4-(2-6С)алканоилпиперазинилом, пирролидинил-(1-6C)алкилом, пиперидинил-(1-6С)алкилом, морфолинил-(1-6C)алкилом, пиперазинил-(1-6C)алкилом, 4-(1-6С)алкилпиперазинил-(1-6C)алкилом, 4-(2-6С)алканоилпиперазинил-(1-6C)алкилом, пирролидинилокси, пиперидинилокси, 1-(1-6С)алкилпиперидинилокси, пирролидинил-(2-6С)-алкокси, пиперидинил-(2-6С)алкокси, морфолинил-(2-6С)алкокси, пиперазинил-(2-6С)алкокси, 4-(1-6C)алкилпиперазинил-(2-6С)-алкокси или 4-(2-6С)алканоилпиперазинил-(2-6С)алкокси, и X, R2, R3, Q, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(r) m равно 1 и R1 является гидрокси, галогеном, трифторметилом, циано, меркапто, нитро, карбокси, (1-6С)алкоксикарбонилом, (1-6С)алкилом или (1-6С)алкокси, и X, R2, R3, Q, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(s) m равно 2 и первый R1 заместитель выбирают из заместителей, определенных выше в параграфе (q) и второй R1 заместитель выбирают из заместителей, определенных выше в параграфе (r), и X, R2, R3, Q, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения;
(t) Х является -NHCO- и R1, R2, R3, Q, m, n и q подходящим образом имеют любые значения, определенные выше или в данном параграфе для конкретных новых соединений данного изобретения.
Предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом, метилом или этилом;
m равно 0,1 или 2;
R1 является гидрокси, фтором, хлором, бромом, трифторметилом, циано, метилом, этилом, метокси, этокси, амино, метиламино, этиламино, диметиламино, диэтиламино, метиламинометилом, этиламинометилом, диметиламинометилом, диэтиламинометилом, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, 2-аминоэтиламино, 3-аминопропиламино, 2-метиламиноэтиламино, 2-этиламиноэтиламино, 3-метиламинопропиламино, 3-этиламинопропиламино, 2-диметиламиноэтиламино, 2-диэтиламиноэтиламино, 3-диметиламинопропиламино, 3-диэтиламинопропиламино, N-(2-аминоэтил)-N-метиламино, N-(3-аминопропил)-N-метиламино, N-(2-метиламиноэтил)-N-метиламино, N-(2-этиламиноэтил)-N-метиламино, N-(3-метиламинопропил)-N-метиламино, N-(3-этиламинопропил)метиламино, N-(2-диметил-аминоэтил)-N-метиламино, N-(2-диэтиламиноэтил)-N-метиламино, N-(3-диметиламинопропил)-N-метиламино, N-(3-диэтиламинопропил)-N-метиламино, пиридилом, пиридилметилом, пиридилметокси, пирролидинилом, пиперидинилом, морфолинилом, пиперазинилом, 4-метилпиперазинилом, гомопиперазинилом, 4-метилгомопиперазинилом, 4-ацетилпиперазинилом, пирролидинилметилом, пиперидинилметилом, морфолинилметилом, пиперазинилметилом, 4-метилпиперазинилметилом, 4-ацетилпиперазинилметилом, пирролидинилокси, 1-метилпирролидинилокси, пиперидинилокси, 1-метилпиперидинилокси, 2-(пирролидинил)этокси, 3-(пирролидинил)-пропокси, 2-(пиперидинил)этокси, 3-(пиперидинил)пропокси, 2-(морфолинил)этокси, 3-(морфолинил)пропокси, 2-(пиперазинил)-этокси, 3-(пиперазинил)пропокси, 2-(4-метилпиперазинил)этокси, 3-(4-метилпиперазинил)пропокси, 2-(4-ацетилпиперазинил)этокси или 3-(4-ацетилпиперазинил)пропокси;
n равно 0 или 1;
R2 является фтором, хлором, бромом, метилом или этилом;
q равно 0 и
Q является фенилом, фурилом, тиенилом, оксазолилом, изоксазолилом, имидазолилом, пиразолилом, тиазолилом, изотиазолилом, пиридилом, пиридазинилом, пиримидинилом, пиразинилом, бензофуранилом, индолилом, бензотиенилом, бензоксазолилом, бензимидазолилом, бензотиазолилом, индазолилом, бензофуразанилом, хинолилом, изохинолилом, хиназолинилом, хиноксалинилом или нафтиридинилом, которые необязательно имеют 1 или 2 заместителя, выбранных из гидрокси, фтора, хлора, трифторметила, циано, амино, метила, этила, метокси, этокси, метилендиокси, метиламино, этиламино, диметиламино, диэтиламино, аминометила, метиламинометила, этиламинометила, диметиламинометила, диэтиламинометила, 2-гидроксиэтокси, 3-гидроксипропокси, 2-метоксиэтокси, 2-этоксиэтокси, 3-метоксипропокси, 3-этоксипропокси, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, пиридила, пиридилметила, пиридилметокси, пирролидинила, пиперидинила, морфолинила, пиперазинила, 4-метилпиперазинила, гомопиперазинила, 4-метилгомопиперазинила, 4-ацетилпиперазинила, пирролидинилметила, пиперидинилметила, морфолинилметила, пиперазинилметила, 4-метилпиперазинилметила, 4-ацетилпиперазинилметила, пирролидинилокси, 1-метилпирролидинилокси, пиперидинилокси, 1-метилпиперидинилокси, 2-(пирролидинил)этокси, 3-(пирролидинил)-пропокси, 2-(пиперидинил)этокси, 3-(пиперидинил)пропокси, 2-(морфолинил)этокси, 3-(морфолинил)пропокси, 2-(пиперазинил)-этокси, 3-(пиперазинил)пропокси, 2-(4-метилпиперазинил)этокси, 3-(4-метилпиперазинил)пропокси, 2-(4-ацетилпиперазинил)этокси и 3-(4-ацетилпиперазинил)пропокси;
или его фармацевтически приемлемая соль.
Другим предпочтительным соединением данного изобретения является производное амида формулы Ia, в котором Х является -NHCO- или -CONH-;
R3 является водородом, метилом или этилом;
m равно 0, 1 или 2;
R1 является гидрокси, фтором, хлором, бромом, трифторметилом, циано, метилом, этилом, метокси, этокси, амино, метиламино, этиламино, диметиламино, диэтиламино, метиламинометилом, этиламинометилом, диметиламинометилом, диэтиламинометилом, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, 2-аминоэтиламино, 3-аминопропиламино, 2-метиламиноэтиламино, 2-этиламиноэтиламино, 3-метиламинопропиламино, 3-этиламинопропиламино, 2-диметиламиноэтиламино, 2-диэтиламиноэтиламино, 3-диметиламинопропиламино, 3-диэтиламинопропиламино, N-(2-аминоэтил)-N-метиламино, N-(3-аминопропил)-N-метиламино, N-(2-метиламиноэтил)-N-метиламино, N-(2-этиламиноэтил)-N-метиламино, N-(3-метиламинопропил)-N-метиламино, N-(3-этиламинопропил)-N-метиламино, N-(2-диметиламиноэтил)-N-метиламино, N-(2-диэтиламиноэтил)-N-метиламино, N-(3-диметиламинопропил)-N-метиламино, N-(3-диэтиламинопропил) -N-метиламино, пиридилом, пиридилметилом, пиридилметокси, 3-пирролинилом, пирролидинилом, пиперидинилом, гомопиперидинилом, морфолинилом, пиперазинилом, 4-метилпиперазинилом, 4-этилпиперазинилом, гомопиперазинилом, 4-метилгомопиперазинилом, 4-ацетилпиперазинилом, пирролидинилметилом, пиперидинилметилом, морфолинилметилом, пиперазинилметилом, 4-метилпиперазинилметилом, гомопиперазинилметилом, 4-метилгомопиперазинилметилом, 4-ацетилпиперазинилметилом, пирролидинилокси, 1-метилпирролидинилокси, пиперидинилокси, 1-метилпиперидинилокси, гомопиперидинилокси, 1-метилгомопиперидинилокси, 2-(пирролидинил)этокси, 3-(пирролидинил)пропокси, 2-(пиперидинил)этокси, 3-(пиперидинил)пропокси, 2-(морфолинил)этокси, 3-(морфолинил)пропокси, 2-(пиперазинил)этокси, 3-(пиперазинил)пропокси, 2-(4-метилпиперазинил)этокси, 3-(4-метилпиперазинил)пропокси, 2-(4-ацетилпиперазинил)этокси, 3-(4-ацетилпиперазинил)пропокси, 3-диметиламинопропиламинометилом, 3-диметиламино-2,2-диметилпропиламинометилом, 2-(1-метилпирролидинилэтил)аминометилом, 3-пирролидинилпропиламинометилом, 2-морфолинилэтиламинометилом, 3-морфолинилпропиламинометилом, 2-пиперазинилэтиламинометилом, 3-(4-метилпиперазинилпропил)-аминометилом, пиридилметокси, имидазолилметокси, тиазолилметокси и 2-метилтиазолилметокси;
n равно 0 или 1;
R2 является фтором, хлором, бромом, метилом или этилом;
q равно 0 и
Q является фенилом, инденилом, инданилом, тетрагидронафтилом, флуоренилом, фурилом, тиенилом, оксазолилом, изоксазолилом, имидазолилом, пиразолилом, тиазолилом, изотиазолилом, пиридилом, пиридазинилом, пиримидинилом, пиразинилом, бензофуранилом, индолилом, бензотиенилом, бензоксазолилом, бензимидазолилом, бензотиазолилом, индазолилом, бензофуразанилом, хинолилом, изохинолилом, хиназолинилом, хиноксалинилом, нафтиридинилом, карбазолилом, дибензофуранилом, дибензотиофенилом или ксантенилом, которые необязательно имеют 1 или 2 заместителя, выбранных из гидрокси, фтора, хлора, трифторметила, циано, амино, метила, этила, метокси, этокси, пропокси, изопропокси, циклопентокси, метилендиокси, метиламино, этиламино, диметиламино, диэтиламино, ацетамидо, пропионамидо, N-метилацетамидо, метансульфонамидо, N-метилметансульфонамидо, аминометила, метиламинометила, этиламинометила, диметиламинометила, диэтиламинометила, 2-гидроксиэтокси, 3-гидроксипропокси, 2-метоксиэтокси, 2-этоксиэтокси, 3-метоксипропокси, 3-этоксипропокси, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, фенила, фурила, тиенила, пиридила, пиридилметила, пиридилметокси, азетидинила, 3-пирролинила, пирролидинила, пиперидинила, гомопиперидинила, морфолинила, пиперазинила, 4-метилпиперазинила, гомопиперазинила, 4-метилгомопиперазинила, 4-ацетилпиперазинила, пирролидинилметила, пиперидинилметила, морфолинилметила, пиперазинилметила, 4-метилпиперазинилметила, 4-ацетилпиперазинилметила, пирролидинилокси, 1-метилпирролидинилокси, пиперидинилокси, 1-метилпиперидинилокси, 2-(пирролидинил)-этокси, 3-(пирролидинил)пропокси, 2-(пиперидинил)этокси, 3-(пиперидинил)пропокси, 2-(морфолинил)этокси, 3-(морфолинил)-пропокси, 2-(пиперазинил)этокси, 3-(пиперазинил)пропокси, 2-(4-метилпиперазинил)этокси, 3-(4-метилпиперазинил)пропокси, 2-(4-ацетилпиперазинил)этокси и 3-(4-ацетилпиперазинил)-пропокси, и где любая фенильная, фурильная, тиенильная, пиридильная или гетероциклильная группа в заместителе на Q может необязательно иметь 1 или 2 заместителя, выбранных из фтора, хлора, метила и метокси;
или его фармацевтически приемлемая соль.
Более предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом или метилом;
m равно 0, 1 или 2;
R1 является гидрокси, фтором, хлором, бромом, трифторметилом, циано, метилом, этилом, метокси, этокси, амино, метиламино, этиламино, диметиламино, диэтиламино, метиламинометилом, этиламинометилом, диметиламинометилом, диэтиламинометилом, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, 2-аминоэтиламино, 3-аминопропиламино, 2-метиламиноэтиламино, 2-этиламиноэтиламино, 3-метиламинопропиламино, 3-этиламинопропиламино, 2-диметиламиноэтиламино, 2-диэтиламиноэтиламино, 3-диметиламинопропиламино, 3-диэтиламинопропиламино, N-(2-аминоэтил)-N-метиламино, N-(3-аминопропил)-N-метиламино, N-(2-метиламино-этил)-N-метиламино, N-(2-этиламиноэтил)-N-метиламино, N-(3-метиламинопропил)-N-метиламино, N-(3-этиламинопропил)-N-метиламино, N-(2-диметиламиноэтил)-N-метиламино, N-(2-диэтиламиноэтил)-N-метиламино, N-(3-диметиламинопропил)-N-метиламино, N-(3-диэтиламинопропил)-N-метиламино, 2-пиридилметилом, 3-пиридилметилом, 4-пиридилметилом, 2-пиридилметокси, 3-пиридилметокси, 4-пиридилметокси, пирролидин-1-илом, пиперидино, морфолино, пиперазин-1-илом, 4-метилпиперазин-1-илом, гомопиперазин-1-илом, 4-метилгомопиперазин-1-илом, 4-ацетилпиперазин-1-илом, пирролидин-1-илметилом, пиперидинометилом, морфолинометилом, пиперазин-1-илметилом, 4-метилпиперазин-1-илметилом, 4-ацетилпиперазин-1-илметилом, пирролидин-3-илокси, 1-метилпирролидин-3-илокси, пиперидин-4-илокси, 1-метилпиперидин-4-илокси, 2-(пирролидин-1-ил)этокси, 3-(пирролидин-1-ил)пропокси, 2-пиперидиноэтокси, 3-пиперидинопропокси, 2-морфолиноэтокси, 3-морфолинопропокси, 2-пиперазин-1-илэтокси, 3-пиперазин-1-илпропокси, 2-(4-метилпиперазин-1-ил)этокси, 3-(4-метилпиперазин-1-ил)пропокси, 2-(4-ацетилпиперазин-1-ил)-этокси или 3-(4-ацетилпиперазин-1-ил)пропокси;
n равно 0 или 1;
R2 является фтором, хлором или метилом;
q равно 0 и
Q является фенилом, 2-фурилом, 2-тиенилом, 4-оксазолилом, 5-изоксазолилом, 4-тиазолилом, 5-изотиазолилом, 2-пиридилом, 3-пиридилом, 4-пиридилом, 2-бензофуранилом, 2-индолилом, 2-бензотиенилом, 2-бензоксазолилом, 2-бензимидазолилом, 2-бензотиазолилом, 4-бензофуразанилом, 2-хинолилом, 6-хинолилом, 7-хинолилом, 3-изохинолилом, 6-хиназолинилом, 7-хиназолинилом, 6-хиноксалинилом или 7-хиноксалинилом, которые необязательно имеют 1 или 2 заместителя, выбранных из гидрокси, фтора, хлора, трифторметила, циано, амино, метила, этила, метокси, этокси, метилендиокси, метиламино, этиламино, диметиламино, диэтиламино, аминометила, метиламинометила, этиламинометила, диметиламинометила, диэтиламинометила, 2-гидроксиэтокси, 3-гидроксипропокси, 2-метоксиэтокси, 2-этоксиэтокси, 3-метоксипропокси, 3-этоксипропокси, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, 2-пиридила, 3-пиридила, 4-пиридила, 2-пиридилметила, 3-пиридилметила, 4-пиридилметила, 2-пиридилметокси, 3-пиридилметокси, 4-пиридилметокси, пирролидин-1-ила, пиперидино, морфолино, пиперазин-1-ила, 4-метилпиперазин-1-ила, гомопиперазин-1-ила, 4-метилгомопиперазин-1-ила, 4-ацетилпиперазин-1-ила, пирролидин-1-илметила, пиперидинометила, морфолинометила, пиперазин-1-илметила, 4-метилпиперазин-1-илметила, 4-ацетилпиперазин-1-илметила, пирролидин-3-илокси, 1-метилпирролидин-3-илокси, пиперидин-4-илокси, 1-метилпиперидин-4-илокси, 2-пирролидин-1-илэтокси, 3-пирролидин-1-илпропокси, 2-пиперидиноэтокси, 3-пиперидинопропокси, 2-морфолиноэтокси, 3-морфолинопропокси, 2-пиперазин-1-илэтокси, 3-пиперазин-1-илпропокси, 2-(4-метилпиперазин-1-ил)этокси, 3-(4-метилпиперазин-1-ил)пропокси, 2-(4-ацетилпиперазин-1-ил)этокси и 3-(4-ацетилпиперазин-1-ил)пропокси;
или его фармацевтически приемлемая соль.
Более предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом или метилом;
m равно 0, 1 или 2;
R1 является гидрокси, фтором, хлором, бромом, трифторметилом, циано, метилом, этилом, метокси, этокси, амино, метиламино, этиламино, диметиламино, диэтиламино, метиламинометилом, этиламинометилом, диметиламинометилом, диэтиламинометилом, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, 2-аминоэтиламино, 3-аминопропиламино, 2-метиламиноэтиламино, 2-этиламиноэтиламино, 3-метиламинопропиламино, 3-этиламинопропиламино, 2-диметиламиноэтиламино, 2-диэтиламиноэтиламино, 3-диметиламинопропиламино, 3-диэтиламинопропиламино, N-(2-аминоэтил)-N-метиламино, N-(3-аминопропил)-N-метиламино, N-(2-метиламиноэтил)-N-метиламино, N-(2-этиламиноэтил)-N-метиламино, N-(3-метиламинопропил)-N-метиламино, N-(3-этиламинопропил)-N-метиламино, N-(2-диметиламиноэтил)-N-метиламино, N-(2-диэтиламиноэтил)-N-метиламино, N-(3-диметиламинопропил)-N-метиламино, N-(3-диэтиламинопропил)-N-метиламино, 2-пиридилметилом, 3-пиридилметилом, 4-пиридилметилом, 2-пиридилметокси, 3-пиридилметокси, 4-пиридилметокси, пирролидин-1-илом, пиперидино, морфолино, пиперазин-1-илом, 4-метилпиперазин-1-илом, гомопиперазин-1-илом, 4-метилгомопиперазин-1-илом, 4-ацетилпиперазин-1-илом, пирролидин-1-илметилом, пиперидинометилом, морфолинометилом, пиперазин-1-илметилом, 4-метилпиперазин-1-илметилом, 4-ацетилпиперазин-1-илметилом, пирролидин-3-илокси, 1-метилпирролидин-3-илокси, пиперидин-4-илокси, 1-метилпиперидин-4-илокси, 2-(пирролидин-1-ил)этокси, 3-(пирролидин-1-ил)пропокси, 2-пиперидиноэтокси, 3-пиперидинопропокси, 2-морфолиноэтокси, 3-морфолинопропокси, 2-пиперазин-1-илэтокси, 3-пиперазин-1-илпропокси, 2-(4-метилпиперазин-1-ил)этокси, 3-(4-метилпиперазин-1-ил)пропокси, 2-(4-ацетилпиперазин-1-ил)этокси или 3-(4-ацетилпиперазин-1-ил)пропокси;
n равно 0 или 1;
R2 является фтором, хлором или метилом;
q равно 0 и
Q является фенилом, 2-пиридилом, 3-пиридилом или 4-пиридилом, которые необязательно имеют 1 или 2 заместителя, выбранных из гидрокси, фтора, хлора, трифторметила, циано, амино, метила, этила, метокси, этокси, метилендиокси, метиламино, этиламино, диметиламино, диэтиламино, аминометила, метиламинометила, этиламинометила, диметиламинометила, диэтиламинометила, 2-гидроксиэтокси, 3-гидроксипропокси, 2-метоксиэтокси, 2-этоксиэтокси, 3-метоксипропокси, 3-этоксипропокси, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, 2-пиридила, 3-пиридила, 4-пиридила, 2-пиридилметила, 3-пиридилметила, 4-пиридилметила, 2-пиридилметокси, 3-пиридилметокси, 4-пиридилметокси, пирролидин-1-ила, пиперидино, морфолино, пиперазин-1-ила, 4-метилпиперазин-1-ила, гомопиперазин-1-ила, 4-метилгомопиперазин-1-ила, 4-ацетилпиперазин-1-ила, пирролидин-1-илметила, пиперидинометила, морфолинометила, пиперазин-1-илметила, 4-метилпиперазин-1-илметила, 4-ацетилпиперазин-1-илметила, пирролидин-3-илокси, 1-метилпирролидин-3-илокси, пиперидин-4-илокси, 1-метилпиперидин-4-илокси, 2-пирролидин-1-илэтокси, 3-пирролидин-1-илпропокси, 2-пиперидиноэтокси, 3-пиперидино-пропокси, 2-морфолиноэтокси, 3-морфолинопропокси, 2-пиперазин-1-илэтокси, 3-пиперазин-1-илпропокси, 2-(4-метилпиперазин-1-ил)этокси, 3-(4-метилпиперазин-1-ил)пропокси, 2-(4-ацетилпиперазин-1-ил)этокси и 3-(4-ацетилпиперазин-1-ил)пропокси;
или его фармацевтически приемлемая соль.
Более предпочтительным соединением данного изобретения является производное амида формулы Ib, в которой R3 является водородом или метилом;
m равно 1 или 2;
R1 является гидрокси, фтором, хлором, метилом, метокси, диметиламинометилом, диэтиламинометилом, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, 3-диметиламино-2-гидроксипропокси, 3-диэтиламино-2-гидроксипропокси, 2-аминоэтиламино, 3-аминопропиламино, 4-аминобутиламино, 3-метиламинопропиламино, 2-диметиламиноэтиламино, 2-диэтиламиноэтиламино, 3-диметиламинопропиламино, 4-диметиламинобутиламино, 3-амино-2-гидроксипропиламино, 3-диметиламино-2-гидроксипропиламино, N-(2-диметиламиноэтил)-N-метиламино, N-(3-диметиламинопропил)-N-метиламино, пирролидин-1-илом, морфолино, пиперидино, пиперазин-1-илом, 4-метилпиперазин-1-илом, 4-этилпиперазин-1-илом, 4-(2-гидроксиэтил)пиперазин-1-илом, гомопиперазин-1-илом, 4-метилгомопиперазин-1-илом, пиперазин-1-илметилом, 4-метилпиперазин-1-илметилом, гомопиперазин-1-илметилом, 4-метилгомопиперазин-1-илметилом, морфолинометилом, 3-аминопирролидин-1-илметилом, 3-гидроксипирролидин-1-илметилом, 4-(2-гидроксиэтил)пиперазин-1-илметилом, пирролидин-3-илокси, 1-метилпирролидин-3-илокси, пиперидин-4-илокси, 1-метилпиперидин-4-илокси, 1-бензилпиперидин-4-илокси, 2-пирролидин-1-илэтокси, 3-пирролидин-1-илпропокси, 2-пиперидиноэтокси, 3-пиперидинопропокси, 2-морфолиноэтокси, 3-морфолинопропокси, 2-пиперазин-1-илэтокси, 3-пиперазин-1-илпропокси, 2-(4-метилпиперазин-1-ил)этокси, 3-(4-метилпиперазин-1-ил)пропокси, 2-гидрокси-3-пирролидин-1-илпропокси, 2-гидрокси-3-пиперидинопропокси, 2-гидрокси-3-морфолинопропокси, пиперидин-4-иламино, 1-метилпиперидин-4-иламино, 1-бензилпиперидин-4-иламино, 2-пирролидин-1-илэтиламино, 3-пирролидин-1-илпропиламино, 2-морфолиноэтиламино, 3-морфолинопропиламино, 2-пиперидиноэтиламино, 3-пиперидинопропиламино, 2-пиперазин-1-илэтиламино, 3-пиперазин-1-илпропиламино, 2-(4-метилпиперазин-1-ил)этиламино, 3-(4-метилпиперазин-1-ил)пропиламино, 2-(1-метилпирролидин-2-ил)этиламино, 3-(1-метилпирролидин-2-ил)пропиламино, 2-диметиламиноэтиламинометилом, 3-диметиламинопропиламинометилом, 3-диметиламино-2,2-диметилпропиламинометилом, 2-(1-метилпирролидин-2-илэтил)аминометилом, 3-пирролидин-1-илпропиламинометилом, 2-морфолиноэтиламинометилом, 3-морфолинопропиламинометилом, 2-пиперазин-1-илэтиламинометилом, 3-(4-метилпиперазин-1-илпропил)аминометилом или 2-пиридилметокси;
n равно 0 или 1;
R2 является хлором или метилом;
q равно 0 и
Q является 2-пиридилом, 3-пиридилом или 4-пиридилом, которые имеют заместитель, выбранный из пирролидин-1-ила, 3-гидроксипирролидин-1-ила, 2-гидроксиметилпирролидин-1-ила, морфолино, пиперидино, 4-гидроксипиперидин-1-ила, пиперазин-1-ила и 4-метилпиперазин-1-ила;
или его фармацевтически приемлемая соль.
Особенно предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом или метилом;
m равно 1 и R1 выбирают из диэтиламинометила, N-(3-диметиламинопропил)-N-метиламино, пирролидин-1-ила, морфолино, пиперидино, пиперазин-1-ила, 4-метилпиперазин-1-ила, 4-этилпиперазин-1-ила, гомопиперазин-1-ила, 4-метилгомопиперазин-1-ила, пиперазин-1-илметила, 4-метилпиперазин-1-илметила, 4-метилгомопиперазин-1-илметила, морфолинометила, 3-аминопирролидин-1-илметила, 3-гидроксипирролидин-1-илметила, пирролидин-3-илокси, пиперидин-4-илокси, 2-пирролидин-1-илэтокси, 2-пиперидиноэтокси, 2-морфолиноэтокси, 3-диметиламинопропиламинометила, 3-диметиламино-2,2-диметилпропиламинометила, 2-(1-метилпирролидин-2-илэтил)аминометила, 3-пирролидин-1-илпропиламинометила, 2-морфолиноэтиламинометила, 3-морфолинопропиламинометила, 2-пиперазин-1-илэтиламинометила, 3-(4-метилпиперазин-1-илпропил)-аминометила и 2-пиридилметокси;
n равно 0 или 1;
R2 является метилом;
q равно 0 и
Q является 3-пиридилом или 4-пиридилом, которые имеют заместитель, выбранный из пирролидин-1-ила, морфолино, пиперидино, пиперазин-1-ила и 4-метилпиперазин-1-ила;
или его фармацевтически приемлемая соль.
Еще более предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом или метилом;
m равно 1 и R1 выбирают из диэтиламинометила, N-(3-диметиламинопропил)-N-метиламино, 3-пирролин-1-ила, пирролидин-1-ила, морфолино, пиперидино, гомопиперидин-1-ила, пиперазин-1-ила, 4-метилпиперазин-1-ила, 4-этилпиперазин-1-ила, гомопиперазин-1-ила, 4-метилгомопиперазин-1-ила, пиперазин-1-илметила, 4-метилпиперазин-1-илметила, гомопиперазин-1-илметила, 4-метилгомопиперазин-1-илметила, морфолинометила, 3-аминопирролидин-1-илметила, 3-гидроксипирролидин-1-илметила, пирролидин-3-илокси, N-метилпирролидин-3-илокси, пиперидин-4-илокси, N-метилпиперидин-4-илокси, гомопиперидин-4-илокси, N-метилгомопиперидин-4-илокси, 2-пирролидин-1-илэтокси, 2-пиперидиноэтокси, 2-морфолиноэтокси, 3-диметиламинопропиламинометила, 3-диметиламино-2,2-диметилпропиламинометила, 2-(1-метилпирролидин-2-илэтил)аминометила, 3-пирролидин-1-илпропиламинометила, 2-морфолиноэтиламинометила, 3-морфолинопропиламинометила, 2-пиперазин-1-илэтиламинометила, 3-(4-метилпиперазин-1-илпропил)аминометила, 2-пиридилметокси, 4-тиазолилметокси и 2-метилтиазол-4-илметокси;
n равно 0 или 1;
R2 является метилом;
q равно 0 и
Q является фенилом, который имеет 1 или 2 заместителя, выбранных из фтора, хлора, трифторметила, метокси, циклопентилокси, ацетамидо, N-метилметансульфонамидо, 2-фурила, азетидин-1-ила, 3-пирролин-1-ила, пирролидин-1-ила, морфолино, пиперидино, гомопиперидин-1-ила, пиперазин-1-ила, гомопиперазин-1-ила, 4-метилпиперазин-1-ила и 4-метилгомопиперазин-1-ила, или Q является 1-флуоренилом или 4-дибензофуранилом, или Q является 3-пиридилом или 4-пиридилом, которые имеют заместитель, выбранный из азетидин-1-ила, 3-пирролин-1-ила, пирролидин-1-ила, морфолино, пиперидино, гомопиперидино, пиперазин-1-ила, гомопиперазин-1-ила, 4-метилпиперазин-1-ила и 4-метилгомопиперазин-1-ила;
или его фармацевтически приемлемая соль.
Еще более предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом или метилом;
m равно 1 и R1 является 4-метилпиперазин-1-илом или N-(3-диметиламинопропил)-N-метиламино;
n равно 0 или 1;
R2 является 6-метилом;
q равно 0 и
Q является 2-морфолинопирид-4-илом;
или его фармацевтически приемлемая соль.
Еще более предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом или метилом;
m равно 1 и R1 является 4-метилпиперазин-1-илом, 4-метилгомопиперазин-1-илом или N-(3-диметиламинопропил)-N-метиламино;
n равно 0 или 1;
R2 является 6-метилом;
q равно 0; и
Q является 2-пирролидин-1-илпирид-4-илом, 2-(3-пирролин-1-ил)пирид-4-илом, 2-пиперидинопирид-4-илом, 2-морфолинопирид-4-илом, 1-флуоренилом, дибензофуран-4-илом, 3-ацетамидофенилом или 3-(2-фурил)фенилом;
или его фармацевтически приемлемая соль.
Еще более предпочтительным соединением данного изобретения является производное амида формулы Ib, в котором R3 является водородом;
m равно 1 и R1 является пиперазин-1-илом, 4-метилпиперазин-1-илом, 4-метилгомопиперазин-1-илом или N-(3-диметиламинопропил)-N-метиламино;
n равно 0 или 1;
R2 является 6-метилом или 6-фтором;
q равно 0 и
Q является 2-азетидин-1-илпирид-4-илом, 2-пирролидин-1-илпирид-4-илом, 2-(3-пирролин-1-ил)пирид-4-илом, 2-пиперидинопирид-4-илом, 2-морфолинопирид-4-илом, 1-флуоренилом, дибензофуран-4-илом, 5-(4-хлорфенил)фуран-2-илом, 4-(4-хлорфенил)-тиен-2-илом, 2-метоксифенилом, 3-этоксифенилом, 3-(1,1,2,2-тетрафторэтокси)фенилом, 3,4-метилендиоксифенилом, 3-ацетамидофенилом, 3-(4-фторфенил)фенилом, 3-(2-фурил)фенилом, 3-фтор-5-пирролидин-1-илфенилом, 3-фтор-5-пиперидинофенилом, 3-фтор-5-морфорлинофенилом или 3-морфолино-5-трифторметилфенилом;
или его фармацевтически приемлемая соль.
Конкретными предпочтительными соединениями данного изобретения являются, например:
6-[N-(3-диметиламинопропил)-N-метиламино]-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
6-[N-(3-диметиламинопропил)-N-метиламино]-2-метил-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
6-[N-(3-диметиламинопропил)-N-метиламино]-3-[5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
6-(4-метилпиперазин-1-ил)-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он
или 8-[N-(3-диметиламинопропил)-N-метиламино]-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он
или их фармацевтически приемлемая соль.
Более предпочтительными соединениями данного изобретения являются, например:
3-[2-метил-5-(2-пирролидин-1-илпирид-4-илкарбониламино)фенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-[2-метил-5-(2-пиперидинопирид-4-илкарбониламино)фенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-{2-метил-5-[2-(3-пирролин-1-ил)пирид-4-илкарбониламино]фенил)-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-[5-дибензофуран-4-илкарбониламино-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-{5-[3-(2-фурил)бензамидо]-2-метилфенил}-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он или
3-[5-(ацетамидобензамидо)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он
или его фармацевтически приемлемая соль.
Производное амида формулы Ia или Ib или его фармацевтически приемлемая соль или in vivo расщепляемый сложный эфир могут быть получены любым известным способом, применяемым для получения химически родственных соединений. Такие способы, при использовании для получения новых производных амида формулы Ia или Ib, представлены как еще одна особенность данного изобретения и проиллюститрованы следующим показательными вариантами способа, в которых, если не указано иначе, X, R1, R2, R3, m, n, q и Q имеют любое из значений, определенных выше. Необходимые исходные материалы могут быть получены стандартными методами органической химии. Получение таких исходных материалов описано совместно со следующим показательным способом и в представленных ниже примерах. Альтернативно необходимые исходные материалы могут быть получены методами, аналогичными тем, которые представлены как иллюстративные, что находится в компетенции специалиста в области органической химии.
(а) Соединение формулы Ia или его фармацевтически приемлемая соль или in vivo расщепляемый сложный эфир могут быть получены взаимодействием N-фенил-2-аминобензамида формулы II
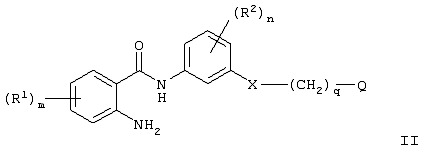
с карбоновой кислотой формулы III или ее реакционноспособным производным
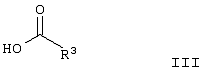
где переменные группы имеют значения, определенные выше, и где любая функциональная группа защищена при необходимости, и
(i) удалением имеющихся защитных групп и
(ii) необязательно образованием или его фармацевтически приемлемой соли или in vivo расщепляемого сложного эфира.
Подходящим реакционноспособным производным карбоновой кислоты формулы III является, например, галоидангидрид, например хлорангидрид, полученный взаимодействием кислоты и хлорида неорганической кислоты, например тионилхлорида; смешанный ангидрид, например ангидрид, полученный взаимодействием кислоты и хлорформиата, такого как изобутилхлорформиат; активный сложный эфир, например сложный эфир, полученный взаимодействием кислоты с фенолом, таким как пентафторфенол, со сложным эфиром, таким как пентафторфенилтрифторацетат или со спиртом, таким как N-гидроксибензотриазол; азид кислоты, например азид, полученный взаимодействием кислоты и азида, такого как дифенилфосфорилазид; нитрил кетонокислоты, например цианид, полученный взаимодействием кислоты и цианида, такого как диэтилфосфорилцианид; или продукт взаимодействия кислоты и карбодиимида, такого как дициклогексилкарбодиимид. Предпочтительным реакционноспособным производным карбоновой кислоты формулы III является, например, сложный эфир соответствующей ортокислоты карбоновой кислоты формулы III, например триалкиловый эфир, такой как триметиловый или триэтиловый эфир. Для карбоновой кислоты формулы III, в которой R3 является водородом, подходящим сложным эфиром ортокислоты является триэтилортоформиат и для карбоновой кислоты формулы III, в которой R3 является метилом, подходящим сложным эфиром ортокислоты является триэтилортоацетат.
Реакцию можно проводить в присутствии подходящего основания, такого как, например, карбонат, алкоголят, гидроксид или гидрид щелочного или щелочноземельного металла, например карбонат натрия, карбонат калия, этилат натрия, бутилат калия, гидроксид натрия, гидроксид калия, гидрид натрия или гидрид калия, или металлорганического основания, такого как алкиллитий, например, н-бутиллитий, или диалкиламинолитий, например диизопропиламид лития, или, например, основания органического амина, такого как, например, пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, морфолин или диазабицикло[5.4.0]ундец-7-ен.
Реакцию также можно проводить в присутствии подходящей кислоты, такой как, например, неорганическая или органическая кислота, такая как соляная, бромистоводородная, серная, уксусная, трифторуксусная, лимонная или малеиновая кислоты.
Реакцию также предпочтительно проводят в подходящем инертном растворителе или разбавителе, например метаноле, этаноле, тетрагидрофуране, метиленхлориде, 1,2-диметоксиэтане, N,N-диметилформамиде, N,N-диметилацетамиде, N-метилпирролидин-2-оне, диметилсульфоксиде или ацетоне и при температуре в интервале, например, от 0 до 150°С, предпочтительно при около 75°С.
Защитные группы в общем могут быть выбраны из любых групп, описанных в литературе или известных специалистам в области химии как подходящие для защиты интересующей группы и могут быть введены обычными методами. Защитные группы могут быть удалены любыми удобными методами, описанными в литературе или известными специалистам в области химии как подхождящие для удаления интересующей защитной группы, такие методы выбираются таким образом, чтобы эффективно удалять защитную группу с минимальным влиянием на остальные группы молекулы.
Определенные примеры защитных групп даны ниже для удобства, где термин «низший», например, в словосочетании низший алкил, означает что группа, к которой он относится, предпочтительно имеет 1-4 атома углерода. Понятно, что представленные примеры не являются ограничивающими. Так же и в случае, когда примеры способов удаления защитных групп, представленные ниже, не являются ограничивающими. Использование защитных групп и способы снятия зашиты, конечно, не входят в объем данного изобретения.
Карбоксильная защитная группа может быть остатком эфирообразующего алифатического или арилалифатического спирта или эфирообразующего силанола (указанный спирт или силанол предпочтительно содержат 1-20 атомов углерода). Примеры карбоксильных защитных групп включают прямые или разветвленные (1-12С)алкильные группы (например, изопропил, трет-бутил); низшие алкокси низшие алкильные группы (например, метоксиметил, этоксиметил, изобутоксиметил); низшие алифатические ацилокси низшие алкильные группы (например, ацетоксиметил, пропионилоксиметил, бутурилоксиметил, пивалоилоксиметил); низшие алкоксикарбонилокси низшие алкильные группы (например, 1-метоксикарбонилоксиэтил, 1-этоксикарбонилоксиэтил); арил низшие алкильные группы (например, бензил, п-метоксибензил, о-нитробензил, п-нитробензил, бензгидрил и фталидил); три(низший алкил)силильные группы (например, триметилсилил и трет-бутилдиметилсилил); три(низший алкил)силильные низшие алкильные группы (например, триметилсилилэтил) и (2-6С)-алкенильные группы (например, аллил и винилэтил). Методы, особенно подходящие для удаления карбоксильных защитных групп, включают, например, гидролиз с кислотным, основным, металлическим или ферментным катализатором.
Примеры гидроксильных защитных групп включают низшие алкильные группы (например, трет-бутил), низшие алкенильные группы (например, аллил); низшие алканоильные группы (например, ацетил; низшие алкоксикарбонильные группы (например, трет-бутоксикарбонил); низшие алкенилоксикарбонильные группы (например, аллилоксикарбонил; арил низшие алкоксикарбонильные группы (например, бензоилоксикарбонил, п-метоксибензилоксикарбонил, о-нитробензилоксикарбонил, п-нитробензилоксикарбонил); три(низший алкил)силильные группы (например, триметилсилил, трет-бутилдиметилсилил) и арил низшие алкильные группы (например, бензил).
Примеры аминозащитных групп включают формил, аралкильные группы (например, бензил и замещенный бензил, п-метоксибензил, нитробензил и 2,4-диметоксибензил, и трифенилметил); ди-п-анизилметильные и фурилметильные группы; низший алкоксикарбонил (например, трет-бутоксикарбонил); низший алкенилоксикарбонил (например, аллилоксикарбонил); арил низшие алкоксикарбонильные группы (например, бензилоксикарбонил, п-метоксибензилоксикарбонил, о-нитробензилоксикарбонил, п-нитробензилоксикарбонил); триалкилсилил (например, триметилсилил и трет-бутилдиметилсилил); алкилиден (например, метилиден); бензилиденовые и замещенные бензилиденовые группы.
Методы, подходящие для удаления гидрокси и аминозащитных групп включают, например, гидролиз с кислотным, основным, металлическим или ферментным катализатором для групп, таких как п-нитробензилоксикарбонил, гидрогенолиз для групп, таких как бензильная, и фотолитический метод для групп, таких как о-нитробензилоксикарбонил.
Условия реакции и реагенты представлены в Advanced Organic Chemistry, 4th Edition by Jerry March, опубликованной в John Wiley & Sons 1992. Общие сведения о защитных группах даны в Protective Groups in Organic Synthesis, 2nd Edition by Green et al., опубликованном в John Wiley & Sons.
N-Фенил-2-аминобензамид формулы II может быть получен восстановлением соответствующего нитросоединения формулы IV
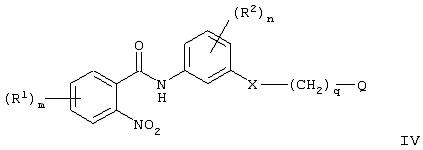
Обычные условия реакции включают использование формиата аммония или газообразного водорода в присутствии катализатора, например металлического катализатора, такого как палладий на углероде. Альтернативно растворяющее металл восстановление может проводиться, например, с использованием железа в присутствии кислоты, например, неорганической или органической кислоты, такой как соляная, бромистоводородная, серная или уксусная кислота. Реакцию обычно проводят в присутствии органического растворителя (предпочтительно полярного протонного растворителя) и предпочтительно при нагревании, например, при температуре 60°С. Любые функциональные группы могут быть защищены и лишены защиты при необходимости.
Нитробензол формулы IV, в котором Х является -NHCO-, может быть получен взаимодействием анилина формулы V
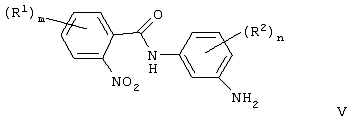
с карбоновой кислотой формулы VI или ее реакционноспособным производным, таким как определено выше,
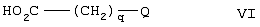
в стандартных условиях образования амидной связи, где переменные группы такие, как определено выше, и где любые функциональные группы защищены при необходимости.
Обычные условия включают активирование карбоксильной группы соединения формулы VI, например, обработкой галогеновым реагентом (например, оксалилхлоридом) с получением ацилгалогенида в органическом растворителе при температуре окружающей среды и затем взаимодействием активированного соединения с анилином формулы V. Любые функциональные группы могут быть защищены и лишены защиты при необходимости. Обычно используют конденсирующий агент карбодиимид в присутствии органического растворителя (предпочтительно безводного полярного апротонного органического растворителя) при невысокой температуре, например в интервале от -10 до 40°С, обычно при температуре окружающей среды, около 20°С.
Анилин формулы V может быть получен взаимодействием бензойной кислоты формулы VII или ее активированного производного, такого как определено выше,
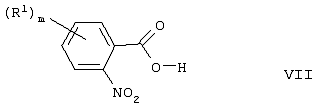
с анилином формулы VIII
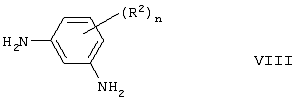
в условиях, подходящих для образования амидной связи, как определено выше.
Нитробензол формулы IV, когда Х является -NHCO-, также может быть получен взаимодействием бензойной кислоты формулы VII или ее активированного производного, как определено выше, с анилином формулы IX
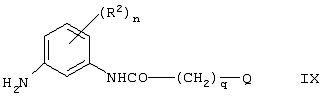
в условиях, подходящих для образования амидной связи, как определено выше.
Соответствующие реакции, представленные в примерах, используют для получения нитробензола формулы IV, где Х является -CONH-.
(b) Соединение формулы Ia, в котором Х является -NHCO- или его фармацевтически приемлемая соль или in vivo расщепляемый эфир, могут быть получены взаимодействием анилина формулы Х
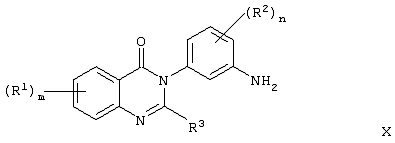
с карбоновой кислотой формулы VI или ее реакционноспособным производным, как определено выше,
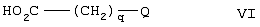
в стандартных условиях образования амидной связи, как определено выше, где переменные группы такие, как определено выше, и где любая функциональная группа защищена при необходимости, и
(i) удалением любых защитных групп;
(ii) необязательно образованием фармацевтически приемлемой соли или in vivo расщепляемого эфира.
Реакцию предпочтительно проводят в присутствии подходящего основания, как определено выше. Реакцию предпочтительно проводят в подходящем инертном растворителе или разбавителе, например тетрагидрофуране, метиленхлориде, 1,2-диметоксиэтане, N,N-диметилформамиде, N,N-диметилацетамиде, N-метилпирролидин-2-оне, диметилсульфоксиде или ацетоне, и при температуре в интервале, например, от -78 до 150°С, предпочтительно при температуре окружающей среды.
Обычно карбодиимидный конденсирующий агент используют в присутствии органического растворителя (предпочтительно безводного полярного апротонного органического растворителя) при умеренной температуре, например в интервале от -10 до 40°С, предпочтительно при температуре окружающей среды, около 20°С.
Анилин формулы Х может быть получен восстановлением в стандартных условиях, как описано выше, соответствующего соединения формулы XI
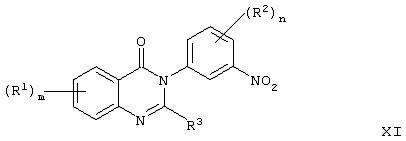
Нитросоединение формулы XI может быть получено взаимодействием N-фенил-2-аминобензамида формулы XII
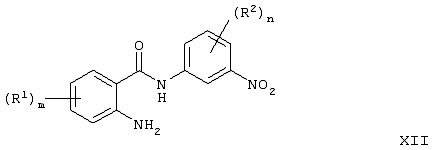
с карбоновой кислотой формулы III или ее реакционноспособным производным
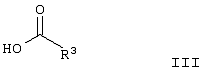
где переменные группы такие, как определены выше, и где любая функциональная группа защищена при необходимости.
(с) Соединение формулы Ia, в котором R1 или заместитель радикала Q является (1-6С)алкокси или замещенным (1-6С)-алкокси, (1-6С)алкилтио, (1-6С)алкиламино, ди-[(1-6С)алкил]-амино или замещенным (1-6С)алкиламино, может быть получено алкилированием, предпочтительно в присутствии подходящего основания, как определено выше, производного амида формулы Ia, в котором R1 или заместитель радикала Q является гидрокси, меркапто или амино соответственно.
Реакцию предпочтительно проводят в присутствии подходящего инертного растворителя или разбавителя, например галогенированного растворителя, такого как метиленхлорид, хлороформ или четыреххлористый углерод, простого эфира, такого как тетрагидрофуран или 1,4-диоксан, ароматического растворителя, такого как толуол, или диполярного апротонного растворителя, такого как N,N-диметилформамид, N,N-диметилацетамид, N-метилпирролидин-2-он или диметилсульфоксид. Реакцию предпочтительно проводят при температуре в интервале, например, от 10 до 150°С, предпочтительно в интервале от 20 до 80°С.
Подходящим алкилирующим агентом является, например, любой агент, известный в данной области техники для алкилирования гидрокси до алкокси или замещенного алкокси, или для алкилирования меркапто до алкилтио, или для алкилирования амино до алкиламино или замещенного алкиламино, например, алкил или замещенный алкилгалогенид, например (1-6С)алкилхлорид, бромид или йодид, или замещенный (1-6С)алкилхлорид, бромид или йодид, в присутствии подходящего основания, как определено выше, в подходящем растворителе или разбавителе, как определено выше, и при температуре в интервале, например, от 10 до 140°С, предпочтительно при температуре окружающей среды или около этого.
(d) Соединение формулы Ia, в котором заместитель радикала Q является амино, (1-6С)алкиламино, ди-[(1-6С)алкил]амино, замещенным (1-6С)алкиламино, замещенным N-(1-6C)алкил-(2-6С)-алкиламино или N-связанной гетероциклильной группой, может быть получено взаимодействием, предпочтительно в присутствии подходящего основания, как определено выше, производного амида формулы Ia, в котором заместитель радикала Q является подходящей уходящей группой, с подходящим амином.
Подходящей уходящей группой является, например, галогеновая группа, такая как фтор, хлор или бром, (1-6C)-алкансульфонилоксигруппа, такая как метансульфонилокси, или арилсульфонилоксигруппа, такая как 4-толуолсульфонилокси.
Реакцию предпочтительно проводят в присутствии подходящего инертного разбавителя или носителя, как определено выше, и при температуре в интервале, например, от 20 до 200°С, предпочтительно в интервале от 75 до 150°С.
(е) Соединение формулы Ia, в котором R1 или заместитель радикала Q является (1-6С)алканоиламино или замещенным (2-6С)алканоиламино, может быть получено ацилированием соединения формулы Ia, в котором R1 или заместителем радикала Q является амино.
Подходящим ацилирующим агентом является, например, любой агент, известный в данной области техники для ацилирования амино до ациламино, например ацилгалогенид, например (1-6С)алканоилхлорид или бромид, в присутствии подходящего основания, как определено выше, ангидрид алкановой кислоты или смешанный ангидрид, например ангидрид (1-6С)алкановой кислоты, такой как уксусный ангидрид, или смешанный ангидрид, полученный взаимодействием алкановой кислоты и (1-6С)-алкоксикарбонилгалогенида, например (1-6С)алкоксикарбонилхлорид, в присутствии подходящего основания, как определено выше. Обычно ацилирование проводят в подходящем растворителе или разбавителе, как определено выше, и при температуре в интервале, например, от -30 до 120°С, предпочтительно при температуре окружающей среды.
(f) Соединение формулы Ia, в котором R1 или заместитель радикала Q является (1-6С)алкансульфониламино, может быть получен взаимодействием соединения формулы Ia, в котором R1 или заместитель радикала Q является амино, с (1-6С)-алкансульфокислотой или ее активированным производным.
Подходящим активированным производным (1-6С)алкансульфокислоты является, например, алкансульфонилгалогенид, например алкансульфонилхлорид, полученный взаимодействием сульфокислоты и хлорида неорганической кислоты, например тионилхлорида. Реакцию предпочтительно проводят в присутствии подходящего основания, как определено выше, в частности пиридина, и в подходящем инертном растворителе или разбавителе, как определено выше, в частности метиленхлориде.
(g) Соединение формулы Ia, где R1 или заместитель радикала Q является карбокси, карбокси-(1-6С)алкилом, карбокси-(1-6С)алкокси, карбокси-(1-6С)алкиламино, N-(1-6С)алкилкарбокси-(1-6С)алкиламино или карбокси-(2-6С)алканоиламино, может быть получено расщеплением соединения формулы Ia, в котором R1 или заместитель радикала Q является (1-6С)алкоксикарбонилом, (1-6С)алкоксикарбонил-(1-6С)алкилом, (1-6С)алкоксикарбонил-(1-6С)-алкокси, (1-6С)алкоксикарбонил-(1-6С)алкиламино, N-(1-6C)-алкил-(1-6С)алкоксикарбонил-(1-6С)алкиламино или (1-6C)-алкоксикарбонил-(2-6С)алканоиламино соответственно.
Реакция расщепления предпочтительно может проводиться по любому из множества методов, известных в данной области техники для такого превращения. Реакция может представлять собой, например, гидролиз в кислых или основных условиях. Подходящим основанием является, например, карбонат или гидроксид щелочного металла, щелочноземельного металла или аммония, например карбонат натрия, карбонат калия, гидроксид натрия, гидроксид калия или гидроксид аммония. Реакцию предпочтительно проводят в присутствии воды и подходящего растворителя или разбавителя, такого как метанол или этанол. Реакцию обычно проводят при температуре в интервале от 10 до 150°С, предпочтительно при температуре окружающей среды.
(h) Соединение формулы Ia, в котором R1 является амино-(1-6С)алкилом, (1-6С)алкиламино-(1-6С)алкилом, ди[(1-6С)-алкил]амино-(1-6С)алкилом или гетероциклил-(1-6С)алкилом, может быть получено взаимодействием соединения формулы XIII предпочтительно в присутствии подходящего основания, как определено выше,
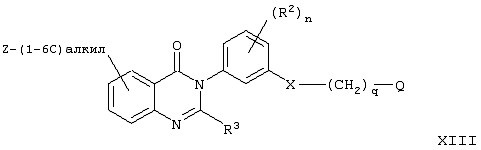
где X, R2, R3, n, q и Q имеют любые значения, определенные выше, и Z является подходящей уходящей группой,
с соответствующим амином или гетероциклом.
Подходящей уходящей группой Z является, например, галогеновая группа, такая как фтор, хлор или бром, (1-6С)-алкансульфонилоксигруппа, такая как метансульфонилокси или арилсульфонилоксигруппа, такая как 4-толуолсульфонилокси.
Реакцию предпочтительно проводят в присутствии подходящего инертного разбавителя или носителя, как определено выше, и при температуре в интервале, например, от 20 до 200°С, предпочтительно в интервале от 50 до 150°С.
Следующие биологические исследования и примеры даны с целью иллюстрации данного изобретения.
Биологические исследования
Следующие исследования могут быть использованы для определения способности ингибирования р38 киназы, ингибирования TNF и антиартритного действия соединений данного изобретения:
Ферментное исследование iv vitro
Оценивается способность соединений данного изобретения ингибировать фермент р38 киназу. Определяется активность соединений в отношении каждой р38 и р38 и р38 изоформы фермента. изоформы фермента.
Рекомбинантную МКК6 человека (GenBank Accesion Number G1209672) выделяют из клона Image 45578 (Genomics, 1996, 33, 151) и используют для получения белка в виде слитого белка GST в pGEX векторе, используя методы, аналогичные тем, которые описаны в J.Han et al., Journal of Biological Chemistry, 1996, 271, 2886-2891. p38 (GenBank Accesion Number G529039) и p38 (GenBank Accesion Number G529039) и p38 (GenBank Accesion Number G1469305) выделяют PCR амплификацией лимфобластной кДНК человека (GenBank Accesion Number GM1416) и кДНК мозга человеческого зародыша [синтезированной из мРНК (Clontech, каталог №6525-1) с использованием набора для синтеза кДНК Gibco superscript] соответственно, используя олигонуклеотиды, предназначенные для 5' и 3' концов р38 (GenBank Accesion Number G1469305) выделяют PCR амплификацией лимфобластной кДНК человека (GenBank Accesion Number GM1416) и кДНК мозга человеческого зародыша [синтезированной из мРНК (Clontech, каталог №6525-1) с использованием набора для синтеза кДНК Gibco superscript] соответственно, используя олигонуклеотиды, предназначенные для 5' и 3' концов р38 и p38 и p38 генов человека с использованием методов, аналогичных методам, описанным в J.Han et al., Biochimica et Biophysica Act a, 1995, 1265, 224-227, и Y.Jiang et al., Journal of Biological Chemistry, 1996, 271, 17920-17926. генов человека с использованием методов, аналогичных методам, описанным в J.Han et al., Biochimica et Biophysica Act a, 1995, 1265, 224-227, и Y.Jiang et al., Journal of Biological Chemistry, 1996, 271, 17920-17926.
Обе изоформы белка р38 экспрессируют в Е. coli в вектора PET. Рекомбинантные изоформы р38 и p38 и p38 человека получают в виде 5' c-myc, 6His меченых белков. Оба МКК6 и р38 белка очищают с использованием стандартных протоколов: GST MKK6 очищают с использованием колонки с глутатионсефарозой, и р38 белки очищают с использованием колонок с хелатом никеля. человека получают в виде 5' c-myc, 6His меченых белков. Оба МКК6 и р38 белка очищают с использованием стандартных протоколов: GST MKK6 очищают с использованием колонки с глутатионсефарозой, и р38 белки очищают с использованием колонок с хелатом никеля.
Ферменты р38 активируют до использования инкубацией с MKK6 в течение 3 часов при температуре 30°С. Не активированный, экспрессированный в coli MKK6 сохраняет значительную активность для того, чтобы полностью активировать обе изоформы р38. Инкубат для активации содержит р38 (10 мкл, 10 мг/мл) или p38 (10 мкл, 10 мг/мл) или p38 (10 мкл, 5 мг/мл) вместе с MKK6 (10 мкл 1 мг/мл), «буфером киназы» [100 мкл; рН 7,4 буфер, содержащий Трис (50 мМ), EGTA (0,1 мМ), ортованадат натрия (0,1 мМ) и (10 мкл, 5 мг/мл) вместе с MKK6 (10 мкл 1 мг/мл), «буфером киназы» [100 мкл; рН 7,4 буфер, содержащий Трис (50 мМ), EGTA (0,1 мМ), ортованадат натрия (0,1 мМ) и  -меркаптоэтанол (0,1%)] и МgАТФ (30 мкл 50мМ Mg (ОСОСН3)2 и 0,5 мМ АТФ). Метод дает достаточно активированный р38 фермент для 3 титрационных микропланшетов. -меркаптоэтанол (0,1%)] и МgАТФ (30 мкл 50мМ Mg (ОСОСН3)2 и 0,5 мМ АТФ). Метод дает достаточно активированный р38 фермент для 3 титрационных микропланшетов.
Тестируемые соединения растворяют в ДМСО и 10 мкл разбавленного 1:10 образца в «буфере киназы» добавляют в ячейки титрационного микропланшета. Для определения единичной дозы соединения тестируют при 10 мкм. Затем добавляют «Kinase Assay Mix» [30 мкл; содержащий Myelin Basic Protein (Gibco BRL, каталог №1322B-010; 1 мл 3,33 мг/мл раствор в воде), активированный р38 фермент (50 мкл) и «буфер киназы» (2 мл)] с последующим добавляением «Меченого АТФ» [10 мкл; содержащего 50 мкМ АТФ, 0,1 мкCi33P АТФ (Amersham International, каталог №BF1000) и 50 мМ Mg(ОСОСНз)2]. Планшеты инкубируют при комнатной температуре при слабом перемешивании. Планшеты, содержащие р38 , инкубируют в течение 90 мин и планшеты, содержащие р38 , инкубируют в течение 90 мин и планшеты, содержащие р38 , инкубируют в течение 45 мин. Инкубацию останавливают добавлением 50 мкл 20% трихлоруксусной кислоты (ТХК). Выпавший в осадок белок фосфорилируют р38 киназой и тестируемые соединения оценивают на способность ингибировать такое фосфорилирование. Содержимое планшетов фильтруют с использованием Canberra Packard Unifilter и промывают 2% ТХК, сушат в течение ночи и подсчитывают на сцинтилляционном счетчике Тор Count. , инкубируют в течение 45 мин. Инкубацию останавливают добавлением 50 мкл 20% трихлоруксусной кислоты (ТХК). Выпавший в осадок белок фосфорилируют р38 киназой и тестируемые соединения оценивают на способность ингибировать такое фосфорилирование. Содержимое планшетов фильтруют с использованием Canberra Packard Unifilter и промывают 2% ТХК, сушат в течение ночи и подсчитывают на сцинтилляционном счетчике Тор Count.
Тестируемые соединения испытывают сначала в разовой дозе и активные соединения повторно тестируют для определения IC50.
Основанные на клетках исследования in vitro
(i) РВМС
Способность соединений данного изобретения ингибировать образование TNF оценивают с использованием мононуклеарных клеток периферийной крови, которые синтезируют и выделяют TNF оценивают с использованием мононуклеарных клеток периферийной крови, которые синтезируют и выделяют TNF при стимулировании липополисахаридом. при стимулировании липополисахаридом.
Мононуклеарные клетки периферийной крови (РВМС) выделяют из гепаринизированной (10 единиц/мл гепарина) человеческой крови центрифугированием при градиенте плотности (LymphoprepTM; Nycomed). Мононуклеарные клетки повторно суспендируют в культуральной среде [среда RPMI 1640 (Gibco) с добавлением 50 единиц/мл пенициллина, 50 мкг/мл стрептомицина, 2 мМ глутамина и 1% инактивируемой теплом человеческой АВ сыворотки (Sigma Н-1513)]. Соединения растворяют в ДМСО при концентрации 50 мМ, разбавляют 1:100 в культуральной среде и затем проводят серийные разведения в культуральной среде, содержащей 1% ДМСО. РВМС (2,4×105 клетки в 160 мкл культуральной среды) инкубируют с 20 мкл тестируемых соединений различных концентраций (выполненные в трех повторах культуры) или 20 мкл культуральной среды, содержащей 1% ДМСО (контрольные ячейки) в течение 30 минут при температуре 37°С в инкубаторе с увлажнением (5% CO2/95% воздуха) (Falcon 3072; 96-ячеечные планшеты с плоским дном для культивации тканей). В соответствующие ячейки добавляют 20 мкл липополисахарида [ЛПС E.Coli 0111:В4 (Sigma L-4130), конечная концентрация 10 мкг/мл], солюбилизированного в культуральной среде. 20 мкл Культуральной среды добавляют в контрольные ячейки с «одной средой». Шесть контролей с «одним ЛПС» и четыре с «одной средой» включают в каждый 96-ячеечный планшет. В каждый тест включают различные концентрации известных ингибиторов TNF , т.е. Ингибитор фермента PDE Type IV (например, см. Semmler,J., Wachtel.H. и Endres, S., Int. J. Immunopharmac. (1993), 15(3), 409-413) или ингибитор про TNF , т.е. Ингибитор фермента PDE Type IV (например, см. Semmler,J., Wachtel.H. и Endres, S., Int. J. Immunopharmac. (1993), 15(3), 409-413) или ингибитор про TNF конвертазы (например, см. McGeehan, G.M. et al., Nature (1994), 370, 558-561). Планшеты инкубируют в течение 7 часов при температуре 37°С (инкубатор с увлажнением), после чего 100 мкл надсадочной жидкости удаляют из каждой ячейки и хранят при температуре -70°С (96-ячеечные планшеты с круглым дном; Corning 25850). Уровни TNF конвертазы (например, см. McGeehan, G.M. et al., Nature (1994), 370, 558-561). Планшеты инкубируют в течение 7 часов при температуре 37°С (инкубатор с увлажнением), после чего 100 мкл надсадочной жидкости удаляют из каждой ячейки и хранят при температуре -70°С (96-ячеечные планшеты с круглым дном; Corning 25850). Уровни TNF определяют в каждом образце, используя ELISA для человеческого TNF определяют в каждом образце, используя ELISA для человеческого TNF (см. WO 92/10190 и Current Protocols in Molecular Biology, том 2, Frederick M. Ausbel et al., John Wiley and Sons Inc.). (см. WO 92/10190 и Current Protocols in Molecular Biology, том 2, Frederick M. Ausbel et al., John Wiley and Sons Inc.).
 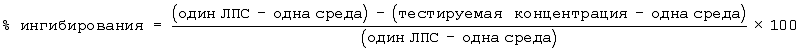
(ii) Цельная кровь человека
Способность соединений данного изобретения ингибировать образование TNF также оценивалась в исследовании цельной крови человека. Цельная кровь человека выделяет TNF также оценивалась в исследовании цельной крови человека. Цельная кровь человека выделяет TNF при стимулировании ЛПС. Это свойство форм крови является основой исследования, которое используется как вторичный тест для соединений, которые показали себя активными в тесте с РВМС. при стимулировании ЛПС. Это свойство форм крови является основой исследования, которое используется как вторичный тест для соединений, которые показали себя активными в тесте с РВМС.
Гепаринизированную (10 единиц/мл) кровь человека получают от добровольцев. 160 мкл цельной крови добавляют в 96-ячеечные планшеты с ячейками с круглым дном (Corning 25850).
Соединения растворяют и последовательно разбавляют в среде RPMI 1640 (Gibco) с добавлением 50 единиц/мл пенициллина, 50 мкг/мл стрептомицина и 2 мМ глутамина, как описано выше. 20 мкл каждой тестируемой концентрации добавляют в соответствующие ячейки (выполненные в трех повторах культуры). 20 мкл среды RPMI 1640, дополненной антибиотинами и глутамином, добавляют в контрольные ячейки. Планшеты инкубируют в течение 30 минут при температуре 37°С (инкубатор с увлажнением) до добавления 20 мкл ЛПС (конечная концентрация 10 мкг/мл). Шесть контролей с «одним ЛПС» и четыре с «одной средой» включают в каждый планшет. В каждый тест включают известные ингибиторы синтеза/выделения TNF . Планшеты инкубируют в течение 6 часов при температуре 37°С (инкубатор с увлажнением). Планшеты центрифугируют (2000 об/мин в течение 10 минут) и 100 мкл плазмы удаляют и хранят при температуре -70°С (планшеты Corning 25850). Уровни TNF . Планшеты инкубируют в течение 6 часов при температуре 37°С (инкубатор с увлажнением). Планшеты центрифугируют (2000 об/мин в течение 10 минут) и 100 мкл плазмы удаляют и хранят при температуре -70°С (планшеты Corning 25850). Уровни TNF измеряют по ELISA (см. WO 92/10190 и Current Protocols in Molecular Biology, том 2, Frederick M. Ausbel et al., John Wiley and Sons Inc.). Спаренные антитела, которые используют в ELISA, получают от R&D Systems (каталоги №№МАВ610 античеловеческие TNF измеряют по ELISA (см. WO 92/10190 и Current Protocols in Molecular Biology, том 2, Frederick M. Ausbel et al., John Wiley and Sons Inc.). Спаренные антитела, которые используют в ELISA, получают от R&D Systems (каталоги №№МАВ610 античеловеческие TNF покрывающие антитела, BAF210 биотинилированные античеловеческие TNF покрывающие антитела, BAF210 биотинилированные античеловеческие TNF детектирующие антитела). детектирующие антитела).
Ex vivo/in vivo оценка
Способность соединений данного изобретения ингибировать TNF ex vivo оценивают на мышах или крысах. Вкратце, группе самцов крыс Wistar Alderley Park (АР) (180-210 г) вводят дозы соединения (6 крыс) или носитель лекарственного средства (10 крыс) подходящим способом, например пероральным (п.о.), внутрибрюшинным (в.б.) или подкожным (п.к.). Через 19 минут крыс умерщвляют с помощью увеличения концентрации CO2 и выпускают кровь через заднюю полую вену в 5 единиц гепарина натрия/мл крови. Образцы крови сразу же помещают на лед и центрифугируют при 2000 об/мин в течение 10 минут при температуре 4°С, и собранную плазму замораживают при температуре -20°С для дальнейшего исследования их влияния на образование TNF ex vivo оценивают на мышах или крысах. Вкратце, группе самцов крыс Wistar Alderley Park (АР) (180-210 г) вводят дозы соединения (6 крыс) или носитель лекарственного средства (10 крыс) подходящим способом, например пероральным (п.о.), внутрибрюшинным (в.б.) или подкожным (п.к.). Через 19 минут крыс умерщвляют с помощью увеличения концентрации CO2 и выпускают кровь через заднюю полую вену в 5 единиц гепарина натрия/мл крови. Образцы крови сразу же помещают на лед и центрифугируют при 2000 об/мин в течение 10 минут при температуре 4°С, и собранную плазму замораживают при температуре -20°С для дальнейшего исследования их влияния на образование TNF стимулированной ЛПС кровью человека. Образцы плазмы крыс оттаивают и 175 мкл каждого образца добавляют согласно указанному способу в 96-ячеечные планшеты с ячейками с круглым дном (Corning 25850). Затем в каждуют ячейку добавляют 50 мкл гепаринизированной крови человека, смешивают и планшеты инкубируют в течение 30 мин при температуре 37°С (инкубатор с увлажнением). В ячейки добавляют ЛПС (25 мкл; конечная концентрация 10 мкг/мл) и инкубацию продолжают в течение еще 5,5 часов. Контрольные ячейки инкубируют с 25 мкл одной среды. Затем планшеты центрифугируют в течение 10 минут при 2000 об/мин, 200 мкл надсадочной жидкости переносят в 96-ячеечный планшет и замораживают при температуре -20°С для последующего анализа концентрации TNF с помощью ELISA. стимулированной ЛПС кровью человека. Образцы плазмы крыс оттаивают и 175 мкл каждого образца добавляют согласно указанному способу в 96-ячеечные планшеты с ячейками с круглым дном (Corning 25850). Затем в каждуют ячейку добавляют 50 мкл гепаринизированной крови человека, смешивают и планшеты инкубируют в течение 30 мин при температуре 37°С (инкубатор с увлажнением). В ячейки добавляют ЛПС (25 мкл; конечная концентрация 10 мкг/мл) и инкубацию продолжают в течение еще 5,5 часов. Контрольные ячейки инкубируют с 25 мкл одной среды. Затем планшеты центрифугируют в течение 10 минут при 2000 об/мин, 200 мкл надсадочной жидкости переносят в 96-ячеечный планшет и замораживают при температуре -20°С для последующего анализа концентрации TNF с помощью ELISA.
Данные анализируют с помощью предназначенного для данной цели программного обеспечения для каждого соединения/дозы:
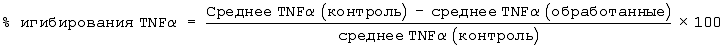
Альтернативно в представленном выше методе вместо крыс могут быть использованы мыши.
Тест на определение антиартритного действия
Действие соединений в качестве антиартритных агентов тестируют следующим образом. Trentham et al [1] показали, что растворимый в кислоте нативный коллаген типа II является артрогенным для крыс; он вызывает полиартрит при введении в неполном адъюванте Фрейнда. В настоящее время он известен как вызванный коллагеном артрит (CIA), и подобные состояния могут быть вызваны у мышей и приматов. Недавние исследования показали, что анти-TNF моноклональные антитела [2] и TNF рецептор-IgG слитые белки [3] улучшают установленный CIA, отмечая, что TNF играет ключевую роль в патофизиологии CIA. Более того, примечательная эффективность, отмеченная у анти-TNF моноклональных антител в процессе проведения последних клинических исследований ревматоидного артрита, показывает, что TNF играет основную роль в данных хронических воспалительных заболеваниях. Таким образом, CIA у DBA/l мышей, как описано в ссылках 2 и 3, представляет собой третичную модель, которая может быть использована для демонстрации антиартритного действия соединения. Также см. ссылку 4.
1. Trentham, D.E. et al., (1977) J. Exp. Med., 146, 857.
2. Williams, R.O. et al., (1992) Proc. Natl. Acad. Sci., 89, 9784.
3. Williams, R.O. et al., (1995) Immunology, 84, 433.
4. Badger, M.B. et al., (1996) The Journal of Pharmacology and Experimental Therapeutics, 279, 1453-1461.
Хотя, как ожидается, фармакологические свойства соединений формулы Ia изменяются в зависимости от структурных изменений, в общем соединения формулы Ia дают более 30% ингибирования р38 и/или р38 и/или р38 при концентрациях вплоть до 10 мкм. Для тестируемых соединений данного изобретения в эффективных дозах не было отмечено никакой физиологически неприемлемой токсичности. при концентрациях вплоть до 10 мкм. Для тестируемых соединений данного изобретения в эффективных дозах не было отмечено никакой физиологически неприемлемой токсичности.
Например:
(i) 6-[N-(3-диметиламинопропил)-N-метиламино]-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он имеет IC50 приблизительно 0,2 мкМ в отношении p38 и IC50 приблизительно 2 мкМ по данным тестирования с цельной кровью человека; и IC50 приблизительно 2 мкМ по данным тестирования с цельной кровью человека;
(ii) 6-[N-(3-диметиламинопропил)-N-метиламино]-3- [5- (2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он имеет IC50 приблизительно 0,05 мкМ в отношении р38 и IC50 приблизительно 5 мкМ по данным тестирования с цельной кровью человека и и IC50 приблизительно 5 мкМ по данным тестирования с цельной кровью человека и
(iii) 8-[N-(3-диметиламинопропил)-N-метиламино]-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он имеет IC50 приблизительно 0,1 мкМ в отношении р38 и IC50 приблизительно 7 мкМ по данным тестирования с цельной кровью человека. и IC50 приблизительно 7 мкМ по данным тестирования с цельной кровью человека.
Согласно другому аспекту данного изобретения представлена фармацевтическая композиция, которая содержит производное амида формулы Ia или Ib, или его фармацевтически приемлемую соль, или его in vivo расщепляемый сложный эфир, как определено выше, или производное амида, выбранное из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-З,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она, в сочетании с фармацевтически приемлемым разбавителем или носителем.
Композиции данного изобретения могут быть в форме, подходящей для перорального применения (например, в виде таблеток, пастилок, жестких или мягких капсул, водных или масляных суспензий, эмульсий, диспергируемых порошков или гранул, сиропов или эликсиров), для местного использования (например, в виде кремов, мазей, гелей или водных или масляных растворов или суспензий), для введения ингаляцией (например, в виде тонкоизмельченного порошка или жидкого аэрозоля), для введения пневматически (например, в виде тонкоизмельченного порошка) или для парентерального введения (например, в виде стерильного водного или масляного раствора для внутривенного, подкожного или внутримышечного введения или в виде суппозиториев для ректального введения).
Композиции данного изобретения могут быть получены обычными методами с использованием обычных фармацевтических эксципиентов, хорошо известных в данной области техники. Таким образом, композиции, предназначенные для перорального применения, могут содержать, например, один или более красителей, подсластителей, вкусовых агентов и/или консервантов.
Количество активного ингредиента, которое объединяют с одним или более эксципиентами для получения разовой дозированной формы, обязательно зависит от принимающего лечение пациента и конкретного способа введения. Например, композиция для перорального применения человеком обычно содержит, например, от 0,5 мг до 0,5 г активного соединения с соответствующим и удобным количеством эксципиентов, которое может варьироваться от около 5 до около 98% мас. от массы всей композиции.
Величина дозы для терапевтических или профилактических целей соединения формулы Ia естественно зависит от природы и тяжести состояний, возраста и пола животного или пациента и способа введения согласно хорошо известным принципам медицины.
При использовании соединения формулы Ia для терапевтических или профилактических целей оно обычно вводится таким образом, чтобы ежедневная доза составляла, например, от 0,5 до 75 мг на 1 кг веса тела, при необходимости разделенная на несколько доз. Обычно при парентеральном введении используют более низкие дозы. Таким образом, например, для внутривенного введения доза составляет, например, от 0,5 до 30 мг на 1 кг веса тела. Также, для введения ингаляцией, используется доза в интервале, например, от 0,5 до 25 мг на 1 кг веса тела. Однако предпочтительно пероральное введение, особенно в виде таблеток. Обычно единичная дозированная форма содержит от примерно 1 мг до примерно 500 мг соединения данного изобретения.
Согласно другому аспекту данного изобретения представлено новое производное амида формулы Ia или его фармацевтически приемлемая соль или in vivo расщепляемый сложный эфир, как определено выше, для применения в способе терапевтического лечения организма человека или животного.
Согласно другому аспекту данного изобретения представлено использование производного амида формулы Ia или Ib или или его фармацевтически приемлемой соли или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она для производства лекарственного средства для применения при лечении заболеваний или клинических состояний, медиированных цитокинами.
В другом аспекте данное изобретение представляет способ лечения заболеваний или клинических состояний, медиированных цитокинами, который включает введение теплокровному животному эффективного количества производного амида формулы Ia или Ib или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В другом аспекте данное изобретение представляет применение производного амида формулы Ia или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3, 4-дигидрохиназолин-4-она для производства лекарственного средства для применения при лечении заболеваний или клинических состояний, медиированных TNF, IL-1, IL-6 или IL-8.
В другом аспекте данное изобретение представляет способ лечения заболеваний или клинических состояний, медиированных TNF, IL-1, IL-6 или IL-8, который включает введение теплокровному животному эффективного количества производного амида формулы Ia или Ib, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо) -2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В другом аспекте данное изобретение представляет применение производного амида формулы Ia или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3- [5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она для производства лекарственного средства для применения при лечении заболеваний или клинических состояний, медиированных TNF.
В другом аспекте данное изобретение представляет способ лечения заболеваний или клинических состояний, медиированных TNF, который включает введение теплокровному животному эффективного количества производного амида формулы Ia, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В другом аспекте данное изобретение представляет применение производного амида формулы Ia или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она, как определено выше, для производства лекарственного средства для применения для ингибирования TNF, IL-1, IL-6 или IL-8.
В другом аспекте данное изобретение представляет способ ингибирования TNF, IL-1, IL-6 или IL-8, который включает введение теплокровному животному эффективного количества производного амида формулы Ia, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3- [5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В другом аспекте данное изобретение представляет применение производного амида формулы Ia или его фармацевтически приемлемой соли или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-З,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она для производства лекарственного средства для применения для ингибирования TNF.
В другом аспекте данное изобретение представляет способ ингибирования TNF, который включает введение теплокровному животному эффективного количества производного амида формулы Ia, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В другом аспекте данное изобретение представляет применение производного амида формулы Ia или его фармацевтически приемлемой соли или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она для производства лекарственного средства для применения при лечении заболеваний или клинических состояний, медиированных р38 киназой.
В другом аспекте данное изобретение представляет способ лечения заболеваний или клинических состояний, медиированных р38 киназой, который включает введение теплокровному животному эффективного количества производного амида формулы Ia, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В другом аспекте данное изобретение представляет применение производного амида формулы Ia или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидро-хиназолин-4-она для производства лекарственного средства, используемого для генерирования ингибирующего действия в отношении р38 киназы.
В другом аспекте данное изобретение представляет способ генерирования ингибирующего действия в отношении р38 киназы, который включает введение теплокровному животному эффективного количества производного амида формулы Ia, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
В другом аспекте данное изобретение представляет применение производного амида формулы Ia или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она для производства лекарственного средства для применения при лечении ревматоидного артрита, астмы, синдрома раздраженной толстой кишки, рассеянного склероза, СПИДа, септического шока, ишемической болезни сердца или псориаза.
В другом аспекте данное изобретение представляет способ лечения ревматоидного артрита, астмы, синдрома раздраженной толстой кишки, рассеянного склероза, СПИДа, септического шока, ишемической болезни сердца или псориаза, который включает введение теплокровному животному эффективного количества производного амида формулы Ia, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира, как определено выше, или производного амида, выбранного из 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
Соединения данного изобретения могут быть использованы в сочетании с другими лекарствами и терапевтическими методами, используемыми при лечении болезненных состояний, которые облегчаются при ингибировании цитокинов, в частности TNF и IL-1. Например, соединения формулы Ia могут быть использованы в сочетании с лекарствами и терапевтическими методами, используемыми при лечении ревматоидного артрита, астмы, синдрома раздраженной толстой кишки, рассеянного склероза, СПИДа, септического шока, ишемической болезни сердца, псориаза и других болезненных состояний, указанных выше в данном описании.
Например, благодаря своей способности ингибировать цитокины соединения формулы Ia являеются ценными при лечении определенных воспалительных и невоспалительных заболеваний, которые одновременно лечатся ингибирующими циклооксигеназу нестероидными противовоспалительными препаратами (НСПВП), такими как индометацин, кеторолак, ацетилсалициловая кислота, ибупрофен, сулиндак, толметин и пироксикам. Совместное введение соединения формулы I с НСПВП может дать снижение количества последнего агента, необходимого для получения терапевтического эффекта. Таким образом, вероятность возникновения побочных эффектов при применении НСПВП, таких как желудочно-кишечные эффекты, снижается. Согласно другой особенности данного изобретения представлена фармацевтическая композиция, которая содержит производное амида формулы Ia или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира в сочетании или с добавкой ингибирующих циклооксигеназу нестероидных противовоспалительных агентов и фармацевтически приемлемый носитель или разбавитель.
Соединения данного изобретения также могут быть использованы с противовоспалительными агентами, такими как ингибитор фермента 5-липоксигеназы.
Соединения формулы Ia также могут быть применены для лечения состояний, таких как ревматоидный артрит, в сочетании с антиартритными агентами, такими как золото, метотрексат, стероиды и пенициллинамин, и таких состояний, как остеоартрит вместе со стероидами.
Соединения данного изобретения также могут вводиться при дегенеративных заболеваниях, например остеоартритах, с хондрозащитными, антидеградационными и/или репаративными агентами, такими как Диацерхейн, препаративные формы с гиалуроновой кислотой, такие как Гиалан, Румалон, Артепарон и соли глюкозамина, такие как Антрил.
Соединения формулы Ia могут быть использованы при лечении астмы в сочетании с антиастматическими агентами, такими как бронходилататоры и антагонисты лейкотриена.
При существовании фиксированной дозы, в таких объединенных продуктах соединения данного изобретения используются в дозе, описанной выше, и другие фармацевтически активные агенты - в пределах утвержденной дозы. При невозможности получения комбинированной препаративной формы используют последовательное применение.
Хотя соединения формулы Ia более ценны в качестве терапевтических агентов для применения на теплокровных животных (включая человека), они также полезны при необходимости ингибирования действия цитокинов. Таким образом, они применяются в качестве фармакологических стандартов при разработке новых биологических тестов и при поиске новых фармакологических агентов.
Далее изобретение проиллюстрировано не ограничивающими его объем примерами, в которых, если не указано иначе:
(i) операции проводят при температуре окружающей среды, т.е. в интервале от 17 до 25°С и в атмосфере инертного газа, такого как аргон, если не указано иначе;
(ii) выпаривание проводят на роторном испарителе в вакууме и процедуры обработки проводят после удаления остаточных твердых веществ фильтрацией;
(iii) хроматографию на колонке (флэш-хроматографию) и жидкостную хроматографию среднего давления (ЖХСД) проводят на колонке с обращенной фазой с двуокисью кремния Merck Kieselgel silica (Арт. 9385) или Merck Lichroprep RP-18 (Арт. 9303) от Е.Merck, Darmstadt, Germany, или жидкостную хроматографию высокого давления (ЖХВД) проводят на колонке с обращенной фазой с двуокисью кремния С18, например на препаративной колонке с обращенной фазой Dynamax C-18 60Å;
(iv) выход дан только для иллюстрации и не обязательно является максимально достигаемым;
(v) в общем, конечные продукты формулы Ia имеют удовлетворительный микроанализ и их структуры подтверждены методами ядерного магнитного резонанса (ЯМР) и/или масс спектра; масс спектральные данные бомбардировки быстрыми атомами (ББА) получают с помощью спектрометра Platform и, если возможно, получают либо данные положительных ионов, либо данные отрицательных ионов; значения химического сдвига ЯМР измеряют по шкале дельта [спектр протонного магнитного резонанса определяют с помощью спектрометра Varian Gemini 2000, работающего при напряженности поля 300 МГц, или спектрометра Bruker АМ250, работающего при напряженности поля 250 МГц]; использованы следующие аббревиатуры: с, синглет; д, дублет; т, триплет; м, мультиплет; ш, широкий;
(vi) промежуточные соединения обычно не имеют полной характеристики и их чистота оценивается с помощью тонкослойной хроматографии, ВЭЖХ, инфракрасного спектра (ИК) и/или ЯМР анализа;
(vii) температуры плавления не корректировались и определены с помощью автоматического аппарата для определения температуры плавления Mettler SP62 или аппарата с масляно-водяной баней; температуры плавления для конечных продуктов формулы Ia определяли после кристаллизации из обычного органического растворителя, такого как этанол, метанол, ацетон, эфир или гексан, чистого или в смеси, и
(viii) использованы следующие аббревиатуры:
| ДМФ |
N,N-диметилформамид |
| ДМСО |
иметилсульфоксид. |
Пример 1
3-(5-Бензамидо-2-хлорфенил)-7-метокси-3,4-дигидрохиназолин-4-он
Триэтилортоформиат (0,189 мл) добавляют к перемешиваемой смеси N-(5-бензамидо-2-хлорфенил)-2-амино-4-метоксибензамида (0,15 г), этанола (10 мл) и ледяной уксусной кислоты (0,022 мл) и полученную смесь нагревают при температуре 70°С в течение 16 часов. Смесь выпаривают. Остаток распределяют между метиленхлоридом и насыщенным водным раствором бикарбоната натрия. Органическую фазу сушат (MgSO4) и выпаривают, и остаток растирают под смесью этилацетата и диэтилового эфира. Полученное соединение далее очищают хроматографией на ионообменной колонке (колонка isolute SCX от International Sorbent Technology Limited, Hengoed, Mid-Glamorgan, UK) используя сначала метанол и затем 99:1 смесь метанола и насыщенного водного раствора гидроксида аммония в качестве элюента. Таким образом получают указанное в заголовке соединено (0,054 г).
Спектр ЯМР: (ДMCOd6) 3,92(с, 3Н), 7,12-7,22 (м, 2Н), 7,48-7,6(м, 3Н), 7,68(д, 1Н), 7,88-8,0(м, 3Н), 8,04-8,12(м, 2Н), 8,28(м, 1Н), 10,06(с, 1Н). Масс спектр: М+Н+ 406 и 408.
N-(5-Бензамидо-2-хлорфенил)-2-амино-4-метоксибензамид, используемый в качестве исходного соединения, получают следующим образом.
Бензоилхлорид (5,2 мл) добавляют к перемешиваемой смеси 2,4-диаминохлорбензола (6,42 г), триэтиламина (12,5 мл) и метиленхлорида (100 мл), которая охлаждена до температуры 0°С. Смесь нагревают при температуре окружающей среды и перемешивают в течение 16 часов. Смесь выпаривают и остаток растирают под водным раствором насыщенного бикарбоната натрия. Полученное твердое вещество выделяют, промывают последовательно водой и изогексаном и сушат в вакууме при температуре 55°С. Таким образом получают N-(3-амино-4-хлорфенил)бензамид в виде твердого вещества (10,38 г). Спектр ЯМР: (ДМСОd6) 5,32 (с, 2Н), 6,9(м, 1H), 7,1(д, 1H), 7,37(д, 1H), 7,52(м, 3Н), 7,9(д, 2Н), 10,05(с, 1H).
Оксалилхлорид (0,781 мл) добавляют по каплям к перемешиваемой смеси 4-метокси-2-нитробензойной кислоты (1,6 г), ДМФ (несколько капель) и метиленхлорида (30 мл), которая охлаждена до температуры 0°С. Смеси дают возможность нагреться до температуры окружающей среды и перемешивают в течение 4 часов. Смесь выпаривают. Остаток растворяют в метиленхлориде (10 мл) и по каплям добавляют к перемешиваемой смеси N-(3-амино-4-хлорфенил)бензамида (2,0 г), триэтиламина, (2,49 мл) и метиленхлорида (30 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Осадок выделяют, промывают 1N водным раствором соляной кислоты и метанолом и сушат в вакууме при температуре 40°С. Таким образом получают N-(5-бензамидо-2-хлорфенил)-4-метокси-2-нитробензамид (2,49 г). Спектр ЯМР: (ДМСОd6) 3,9 (с, 3Н), 7,39(д, 1H), 7,47-7,62(м, 5Н), 7,72(д, 1H), 7,78(д, 1H), 7,97(д, 2Н), 8,14(с, 1H), 10,28(с, 1H), 10,46(с, 1H). Масс спектр: M+H+ 426 и 428.
Железный порошок (2,79 г) добавляют к перемешиваемой суспензии части (2,13 г) полученного выше соединения в смеси этанола (100 мл), воды (20 мл) и уксусной кислоты (4 мл). Смесь перемешивают и нагревают при температуре кипения с обратным холодильником в течение 6 часов. Смесь охлаждают до температуры окружающей среды. Добавляют воду (50 мл) и полученную смесь подщелачивают добавлением карбоната натрия. Смесь фильтруют и фильтрат выпаривают. Остаток растирают под водой. Полученное твердое вещество выделяют и сушат в вакууме при температуре 40°С. Таким образом получают требуемое исходное соединение (0,911 г). Спектр ЯМР: (ДМСОd6) 3,72(с, 3Н), 6,09(д, 1Н), 6,27(с, 1Н), 6,62(с, 2Н), 7,45-7,61(м, 4Н), 7,66-7,72(м, 2Н), 7,95(д, 2Н), 8,07(с, 1Н), 9,52(с, 1Н), 10,37(с, 1Н). Масс спектр: M+H+ 396 и 398.
Пример 2
3-(5-Бензамидо-2-хлорфенил)-7-метокси-2-метил-3,4-дигидрохиназолин-4-он
По методике примера 1 триэтилортоацетат подвергают взаимодействию с N-(5-бензамидо-2-хлорфенил)-2-амино-4-метоксибензамидом. Полученое соединение очищают колоночной хроматографией на isolute SCX ионообменной колонке, используя сначала метанол, затем 99:1 смесь метанола и насыщенного водного раствора гидроксида аммония в качестве элюента. Получают указанное в заголовке соединение с 27% выходом.
Спектр ЯМР: (ДМСОd6) 2,15(с, 3Н), 3,91(с, 3Н), 7,09-7,14(м, 2Н), 7,46-7,6(м, 3Н), 7,71(д, 1Н), 7,87-8,06(м, 5Н), 10,57(с, 1Н). Масс спектр: M+H+ 420 и 422.
Пример 3
Используя методики примеров 1 и примера 2, подходящий 2-аминобензамид подвергают взаимодействию с триэтилортоформиатом или триэтилортоацетатом с получением соединений, описанных в таблице 1.
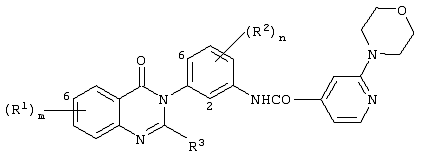
| Таблица I |
| № |
(R1)m |
(R2)n |
R3 |
Прим. |
| 1 |
6-[N-(3-диметиламинопропил)-N-метиламино] |
6-метил |
водород |
а |
| 2 |
6-[N-(3-диметиламинопропил)-N-метиламино] |
6-метил |
метил |
b |
| 3 |
6-[N-(3-диметиламинопропил)-N-метиламино] |
водород |
водород |
с |
| 4 |
6-[N-(3-диметиламинопропил)-N-метиламино] |
водород |
метил |
d |
| 5 |
6-(4-метилпиперазин-1-ил) |
6-метил |
водород |
е |
| 6 |
6-(4-метилпиперазин-1-ил) |
6-метил |
метил |
f |
| 7 |
6-(4-метилпиперазин-1-ил) |
водород |
водород |
9 |
| 8 |
6-(4-метилпиперазин-1-ил) |
водород |
метил |
h |
| 9 |
8-[N-(3-диметиламинопропил)-N-метиламино] |
6-метил |
водород |
i |
| 10 |
6-[N-(3-метиламинопропил)-N-метиламино] |
6-метил |
водород |
j |
Примечания
а) Продукт имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,73-1,83(м, 2Н), 1,88(с, 3Н), 2,23(с, 6Н), 2,26-2,34(м, 2Н), 3,07(с, 3Н), 3,44-3,55(м, 6Н), 3,67-3,71(м, 4Н), 7,0(д, 1Н), 7,09(с, 1Н), 7,19(д, 1Н), 7,31(д, 1Н), 7,43(с, 1Н), 7,54(с, 1Н), 7,66(д, 1Н), 7,75(д, 2Н), 8,23(д, 1Н), 8,69 (с, 1Н). Масс спектр: М+H+ 556.
N-[2-Метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-2-мино-5-[N-(3-диметиламинопропил)-N-метиламино]бензамид, используемый в качестве исходного соединения, получают следующим образом.
Триэтиламин (31,8 мл) добавляют к перемешиваемой смеси 4-метил-3-нитроанилина (15,8 г), 2-хлорпиридин-4-карбонилхлорида (20 г) и метиленхлорида (1 литр) и полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Осадок выделяют, промывают насыщенным водным растовром бикарбоната натрия и метиленхлоридом и сушат в вакууме при температуре 40°С. Получают 2-хлор-N-(4-метил-3-нитрофенил)пиридин-4-карбоксамид (10,2 г). Органический фильтрат промывают насыщенным водным раствором бикарбоната натрия, сушат (MgSO4) и выпаривают. Остаток растирают под метиленхлоридом и полученное твердое вещество выделяют и сушат в вакууме при температуре 40°С. Получают вторую порцию (8,13 г) 2-хлор-N-(4-метил-3-нитрофенил)пиридин-4-карбоксамида. Спектр ЯМР: (ДМСОd6) 2,48(с, 3Н), 7,51(д, 1Н), 7,86(м, 1Н), 7,96(м, 2Н), 8,49(м, 1Н), 10,85(с, 1Н). Масс спектр: M+H+ 292 и 294.
Смесь полученного пиридин-4-карбоксамида и морфолина (250 мл) перемешивают и нагревают при температуре 100°С в течение 18 часов. Смесь выливают в воду (250 мл) и перемешивают в течение 10 минут. Добавляют метиленхлорид и полученную смесь перемешивают в течение 30 минут. Полученное твердое вещество выделяют, промывают метиленхлоридом и сушат в вакуумной печи при температуре 40°С в течение 18 часов. Получают N-(4-метил-3-нитрофенил)-2-морфолинопиридин-4-карбоксамид (17,34 г). Спектр ЯМР: (ДМСОd6 2,48 (с, 3Н), 3,52(м, 4Н), 3,71(м, 4Н), 7,1(д, 1Н), 7,25(с, 1Н), 7,49(д, 1Н), 7,97(м, 1Н), 8,29(м, 1Н), 8,49(м, 1Н), 10,62(с, 1Н). Масс спектр: M+H+ 343.
Смесь части (8,5 г) полученного соединения, катализатора 5% палладия на углероде (0,85 г) и метанола (600 мл) перемешивают при атмосферном давлении водорода в течение 18 часов. Добавляют метиленхлорид и реакционную смесь фильтруют через диатомовую землю. Фильтрат выпаривают с получением N-(3-амино-4-метилфенил)-2-морфолинопиридин-4-карбоксамида (6,41 г). Спектр ЯМР: (ДМСОd6) 2,01(с, 3Н), 3,52(м, 4Н), 3,73(м, 4Н), 4,83(с, 2Н), 6,78(д, 1Н), 6,84(д, 1Н), 7,04-7,08(м, 2Н), 7,2(с, 1Н), 8,24(д, 1Н), 9,95 (с, 1Н). Масс спектр: М+Н+ 313.
Оксалилхлорид (0,55 г) по каплям добавляют к перемешиваемой смеси 5-хлор-2-нитробензойной кислоты (0,726 г), ДМФ (несколько капель) и метиленхлорида (25 мл), охлажденной до температуры 0°С. Смесь нагревают при температуре окружающей среды и перемешивают в течение 5 часов. Смесь выпаривают. Остаток растворяют в метиленхлориде (10 мл) и по каплям добавляют к перемешиваемой смеси N-(3-амино-4-метилфенил)-2-морфолинопиридин-4-карбоксамида (0,933 г), триэтиламина (1,12 мл) и метиленхлорида (25 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Полученный осадок выделяют, промывают последовательно водой, метиленхлоридом и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-5-хлор-2-нитробензамид (1,12 г). Спектр ЯМР: (ДМСОd6) 2,23 (с, 3Н), 3,5-3,54 (м, 4Н), 3,69-3,73(м, 4Н), 7,12(д, 1Н), 7,2-7,25(м, 2Н), 7,58(д, 1Н), 7,81(д, 1Н), 7,87-7,9(м, 2Н), 8,15(д, 1Н), 8,26(д, 1Н). Масс спектр: M+H+ 496 и 498.
Смесь части (0,2 г) полученного соединения и N-(3-диметиламинопропил)-N-метиламина (1,5 мл) перемешивают и нагревают при температуре 100°С в течение 16 часов. Смесь охлаждают и выливают в воду. Полученный осадок выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают N-(2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-5-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамид (0,223 г). Спектр ЯМР: (ДМСОd6) 1,62-1,74(м, 2Н), 2,12(с, 6Н), 2,18-2,26(м, 5Н), 3,08(с, 3Н), 3,50-3,54(м, 6Н), 3,69-3,71(м, 4Н), 6,75(с, 1Н), 6,84(с, 1Н), 7,12(д, 1Н), 7,2(д, 1Н), 7,26(с, 1Н), 7,68(д, 1Н), 7,9(с, 1Н), 8,04(д, 1Н), 8,26(д, 1Н), 9,82(с, 1Н), 10,04(с, 1Н).
Масс спектр: M+H+ 576.
Смесь полученного соединения, 10% палладия на углероде (0,02 г) и метанола (15 мл) перемешивают в атмосфере водорода. После прекращения поглощения водорода катализатор удаляют фильтрацией через диатомовую землю и фильтрат выпаривают. Получают требуемое исходное соединение (0,15 г). Масс спектр: M+H+ 546.
a) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,58-1,7(м, 2Н), 1,97(с, 3Н), 2,06(с, 3Н), 2,12(с, 6Н), 2,23(т, 2Н), 2,96(с, 3Н), 3,39-3,48(м, 2Н), 3,48-3,52(м, 4Н), 3,68-3,71(м, 4Н), 7,08(д, 1Н), 7,15(с, 1Н), 7,22(с, 1Н), 7,32(м, 1Н), 7,42(д, 1Н), 7,51(д, 1Н), 7,67(с, 1Н), 7,74(д, 1Н), 8,26(д, 1Н), 10,42(с, 1Н). Масс спектр: М+H+ 570.
b) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,66(м, 2Н), 2,12(с, 6Н), 2,22(м, 2Н), 2,99(с, 3Н), 3,51(м, 6Н), 3,71(т, 4Н), 7,1(д, 1Н), 7,24(м, 3Н), 7,35(м, 1Н), 7,55(м, 2Н), 7,85(м, 2Н), 8,05(с, 1Н), 8,27(д, 1Н), 10,51(широкий с, 1Н). Масс спектр: M+H+ 542.
N-[3-(2-Морфолинопирид-4-илкарбониламино)фенил]-2-амино-5-[N-3-диметиламинопропил)-N-метиламино]бензамид, используемый в качестве исходного соединения, получают следующим образом.
Триэтиламин (6,7 мл) добавляют к перемешиваемой смеси 3-нитроанилина (3 г), 2-хлорпиридин-4-карбонилхлорида (4,6 г) и метиленхлорида (50 мл) и полученную смесь перемешивают при температуре окружающей среды в течение 40 часов. Смесь выпаривают и остаток растирают под водой. Полученное твердое вещество выделяют, промывают насыщенным водным раствором бикарбоната натрия и сушат в вакууме при температуре 55°С. Получают 2-хлор-N-(3-нитрофенил)пиридин-4-карбоксамид (6,03 г). Спектр ЯМР: (ДМСОd6) 7,68(т, 1Н), 7,88 (т, 1Н), 7,99(м, 2Н), 8,16(д, 1Н), 8,63(д, 1Н), 8,73 (т, 1Н), 10,95 (широкий с, 1Н); Масс спектр: М+Н+ 278.
Смесь полученного пиридин-4-карбоксамида и морфолина (100 мл) перемешивают и нагревают при температуре 130°С в течение 3,5 часов и до температуры 150°С в течение 2 часов. Смесь выливают в воду (250 мл) и перемешивают в течение 10 минут. Полученное твердое вещество выделяют, промывают последовательно водой и изогексаном и сушат в вакууме при температуре 55°С. Получают N-(3-нитрофенил)-2-морфолинопиридин-4-карбоксамид (6,8 г). Спектр ЯМР: (ДМСОd6) 3,52 (т, 4Н), 3,71(т, 4Н), 7,12(д, 1Н), 7,25(с, 1Н), 7,66(т, 1Н), 7,97(д, 1Н), 8,15(д, 1Н), 8,29(д, 1Н), 8,73(т, 1Н), 10,72(широкий с, 1Н). Масс спектр: М+Н+ 329.
Смесь полученного соединения, катализатора 10% палладия на углероде (0,68 г), формиата аммония (13 г) и метанола (150 мл) перемешивают и нагревают при температуре кипения с обратным холодильником в течение 2 часов. Реакционную смесь фильтруют через диатомовую землю. Фильтрат выпаривают и остаток растирают под водой. Полученное твердое вещество выделяют, промывают последовательно водой и изогексаном и сушат в вакууме при температуре 55°С. Получают N-(3-аминофенил)-2-морфолинопиридин-4-карбоксамид (5,38 г). Спектр ЯМР: (ДМСОd6) 3,51(т, 4Н), 3,71(т, 4Н), 5,07(широкий с, 2Н), 6,33(д, 1Н), 6,81(д, 1Н), 6,95(т, 1Н), 7,05(м, 2Н), 7,2(с, 1Н), 8,24(д, 1Н), 9, 96 (широкий с, 1Н). Масс спектр: М+Н+ 299.
Оксалилхлорид (0,66 мл) по каплям добавляют к перемешиваемой смеси 5-хлор-2-нитробензойной кислоты (1,22 г), ДМФ (несколько капель) и метиленхлорида (20 мл). Смесь перемешивают при температуре окружающей среды в течение 4 часов. Смесь выпаривают. Остаток растворяют в метиленхлориде (10 мл) и добавляют к перемешиваемой смеси N-(3-аминофенил)-2-морфолинопиридин-4-карбоксамида (1,5 г), триэтиламина (1,75 мл) и метиленхлорида (20 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Смесь выпаривают и остаток растирают под водой. Полученное твердое вещество отделяют, промывают последовательно 2N водным раствором гидроксида натрия и диэтиловым эфиром. Полученное соединение очищают на ионообменной колонке SCX isolute, используя сначала метанол, а затем 99:1 смесь метанола и насыщенного водного раствора гидроксида аммония в качестве элюента. Получают N- [3-(2-морфолинопирид-4-илкарбониламино)фенил]-5-хлор-2-нитробензамид (1,96 г). Спектр ЯМР: (ДМСОd6) 3,51(т, 4Н), 3,71(т, 4Н), 7,1(д, 1Н), 7,23(с, 1Н), 7,36(м, 2Н), 7,51(д, 1Н), 7,82(д, 1Н), 7,93(с, 1Н), 8,18(м, 2Н), 8,26(д, 1Н), 10,37(широкий с, 1Н), 10,73(широкий с, 1Н). Масс спектр: M+H+ 482.
Смесь части (0,384 г) полученного соединения и N-(3-диметиламинопропил)-N-метиламина (4 мл) перемешивают и нагревают при температуре 120°С в течение 4 часов. Смесь охлаждают и выливают в смесь льда и воды. Полученный осадок выделяют, промывают изогексаном и сушат в вакууме при температуре 55°С. Получают N-[3-(2-морфолинопирид-4-илкарбониламино)фенил]-5-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамид (0,376 г). Спектр ЯМР: (ДМСОd6) 1,67(м, 2Н), 2,11 (с, 6Н), 2,2(т, 2Н), 3,07(с, 3Н), 3,51(м, 6Н), 3,71(т, 4Н), 6,77(д, 1Н), 6,84(м, 1Н), 7,1(д, 1Н), 7,24(с, 1Н), 7,31(м, 2Н), 7,48(д, 1Н), 8,04(д, 1Н), 8,17(с, 1Н), 8,26(д, 1Н), 10,34 (широкий с, 1Н), 10,42 (широкий с, 1Н). Масс спектр: М+Н+ 562.
Смесь полученного соединения, 10% палладия на углеродероде (0,036 г), формиата аммония (0,4 г) и метанола (4 мл) перемешивают и нагревают при температуре кипения с обратным холодильником в течение 2 часов. Смесь фильтруют через диатомовую землю. Фильтрат выпаривают и остаток очищают хроматографией на колонке с использованием колонки с обращеной фазой С18 с двуокисью кремния и смеси воды и метанола с уменьшающейся полярностью в качестве элюента. Получают требуемое исходное соединение (0,256 г). Спектр ЯМР: (ДМСОd6) 1,59(м, 2Н), 2,14(с, 6Н), 2,26(т, 2Н), 2,11 (с, 3Н), 3,18(т, 2Н), 3,52(т, 4Н), 3,71(т, 4Н), 6,67(д, 1Н), 6,82(м, 1Н), 6,93(д, 1Н), 7,11(д, 1Н), 7,29(м, 2Н), 7,39(д, 1Н), 7,46(д, 1Н), 8,17(с, 1Н), 8,26(д, 1Н), 10,05(широкий с, 1Н), 10,31(широкий с, 1Н).
Масс спектр: М+Н+ 532.
с) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,64(м, 2Н), 2,11(с, 9Н), 2,21(м, 2Н), 2,96(с, 3Н), 3,43(т, 2Н), 3,51(м, 4Н), 3,7(м, 4Н), 7,09(д, 1Н), 7,15(м, 2Н), 7,23(с, 1Н), 7,33(м, 1Н), 7,48(м, 2Н), 7,73(с, 1Н), 7,83(д, 1Н), 8,27(д, 1Н), 10,49 (широкий с, 1Н). Масс спектр: M+H+ 556.
d) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 540.
N-[2-Метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-2-амино-5-(4-метилпиперазин-1-ил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
По методике, описанной в пятом параграфе части примечания а), относящейся к получению исходных соединений, N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-5-хлор-2-нитробензамид подвергают взаимодействию с 1-метилпиперазином с получением N-[2-метил-5-(2-морфолинопирид-4-илкарбонил-амино)фенил]-5-(4-метилпиперазин-1-ил)-2-нитробензамида.
Спектр ЯМР: (ДМСОd6) 2,21(с, 3Н), 2,24(с, 3Н), 2,41-2,47(м, 4Н), 2,63-2,69(м, 2Н), 3,46-3,53(м, 8Н), 3,69-3,72(м, 4Н), 7,0(с, 1Н), 7,04-7,12(м, 2Н), 7,19(д, 1Н), 7,25(с, 1Н), 7,57(д, 1Н), 7,88(с, 1Н), 8,04(д, 1Н), 8,26(д, 1Н), 9,83(с, 1Н), 10,33(с, 1Н). Масс спектр: M+H+ 560.
По методике, описанной в шестом параграфе части примечания а), относящейся к получению исходных соединений, N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-5-(4-метилпиперазин-1-ил)-2-нитробензамид восстанавливают с получением требуемого исходного соединения. Масс спектр: М+Н+ 530.
e) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 554.
f) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,22(с, 3Н), 2,4(м, 4Н), 3,3(м, 4Н), 3,51(т, 4Н), 3,71(т, 4Н), 7,1(д, 1Н), 7,25(м, 2Н), 7,47(с, 1Н), 7,54(т, 1H), 7,6(c, 2Н), 7,87(м, 2Н), 8,14(с, 1Н), 8,28(д, 1H), 10,52(широкий с, 1Н). Масс спектр: M+H+ 526.
N-[3-(2-Морфолинопирид-4-илкарбониламино)фенил]-2-амино-5-(4-метилпиперазин-1-ил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
По методике, описанной в пятом параграфе части примечания с), относящейся к получению исходных соединений, N-[3-(2-морфолинопирид-4-илкарбониламино)фенил]-5-хлор-2-нитробензамид подвергают взаимодействию с 1-метилпиперазином с получением N-[3-(2-морфолинопирид-4-илкарбониламино)фенил]-5-(4-метилпиперазин-1-ил)-2-нитробензамида с 89% выходом. Спектр ЯМР: (ДМСОd6) 2,2(с, 3Н), 2,41(м, 4Н), 3,5(м, 8Н), 3,71(т, 4Н), 7,07(м, 3Н), 7,31(м, 3Н), 7,48(д, 1Н), 8,03(д, 1Н), 8,16(с, 1Н), 8,26(д, 1Н), 10,35(широкий с, 1Н), 10,44(широкий с, 1Н). Масс спектр: М+Н+ 546.
По методике, описанной в шестом параграфе части примечания с), относящейся к получению исходных соединений, N-[3-(2-морфолинопирид-4-илкарбониламино)фенил]-5-(4-метилпиперазин-1-ил)-2-нитробензамид восстанавливают. Полученное соединение очищают хроматографией на ионообменной колонке SCX isolute с использованием сначала метанола и затем 99:1 смеси метанола и насыщенного водного раствора гидроксида аммония в качестве элюента. Получают требуемое исходное соединение с 50% выходом. Спектр ЯМР: (ДМСОd6) 2,2 (с, 3Н), 2,4(м, 2Н), 3,0 (т, 4Н), 3,52(т, 4Н), 3,71(т, 4Н), 6,68(д, 1Н), 6,96(д, 1Н), 7,1(м, 2Н), 7,25(м, 2Н), 7,4(м, 2Н), 8,15(с, 1Н), 8,26(д, 1Н), 10,01(широкий с, 1H), 10,31(широкий с, 1Н). Масс спектр: М+Н+ 516.
g) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,12 (с, 3Н), 2,21 (с, 3Н), 2,5(м, 4Н), 3,22(м, 4Н), 3,51(м, 4Н), 3,7(м, 4Н), 7,09(д, 1Н), 7,18(м, 2Н), 7,37(с, 1Н), 7,54(м, 3Н), 7,74(с, 1Н), 7,83(д, 1Н), 8,27(д, 1Н), 10,5(широкий с, 1Н). Масс спектр: М+Н+ 540.
h) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 556.
N-[2-Метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-2-амино-3-[N-(3-диметиламинопропил)-N-метиламино]бензамид, используемый в качестве исходного соединения, получают следующим образом.
По методике, описанной в четвертом параграфе части примечания а), относящейся к получению исходных соединений, 3-хлор-2-нитробензоилхлорид (полученный взаимодействием 3-хлор-2-нитробензойной кислоты и оксалилхлорида) подвергают взаимодействию с N-(3-амино-4-метилфенил)-2-морфолинопиридин-4-карбоксамидом с получением N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3-хлор-2-нитробензамида. Спектр ЯМР: (ДМСОd6) 2,2(с, 3Н), 3,49-3,53(м, 4Н), 3,69-3,73(м, 4Н), 7,1(д, 1Н), 7,18-7,24(м, 2Н), 7,58(д, 1Н), 7,68-7,78(м, 2Н), 7,58(д, 1Н), 7,68-7,78(м, 2Н), 7,84-8,0(м, 2Н), 8,25(д, 1H). Масс спектр: М+Н+ 496 и 498.
По методике, описанной в пятом параграфе части примечания а), относящейся к получению исходных соединений, N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3-хлор-2-нитробензамид подвергают взаимодействию с N-(3-диметиламинопропил)-N-метиламином с получением N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамида. Спектр ЯМР: (ДМСОd6) 1,44-1,58(м, 2Н), 2,06(с, 6Н), 2,15(т, 2Н), 2,21(с, 3Н), 2,69(с, 3Н), 3,02(т, 2Н), 3,48-3,53(м, 4Н), 3,69-3,73(м, 4Н), 7,1(д, 1Н), 7,19-7,25(м, 2Н), 7,44-7,62(м, 3Н), 7,74-7,64(м, 1Н), 7,94(д, 1Н), 8,26(д, 1Н), 10,13(с, 1Н), 10,32(с, 1Н). Масс спектр: М+Н+ 576.
По методике, описанной в шестом параграфе части примечания а), относящейся к получению исходных соединений, N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамид каталитически восстанавливают с получением требуемого исходного соединения. Масс спектр: М+Н+ 546.
i) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,6-1,75(м, 2Н), 2,05(с, 3Н), 2,28(с, 3Н), 2,47-2,52(м, 2Н), 2,99(с, 3Н), 3,49-3,53(м, 6Н), 3,69-3,73(м, 4Н), 7,08(д, 1Н), 7,22(с, 2Н), 7,34-7,24(м, 2Н), 7,6(д, 1Н), 7,75-7,8(м, 2Н), 7,97(с, 1Н),8,28(д, 1Н), 10,42(с, 1Н). Масс спектр: М+Н+ 542.
N-(2-Метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-2-амино-5-[N-(3-метиламинопропил)-N-метиламино]бензамид, используемый в качестве исходного соединения, получают следующим образом.
По методике, описанной в пятом параграфе части примечания а), относящейся к получению исходных соединений, N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-5-хлор-2-нитробензамид подвергают взаимодействию с N-(3-метиламинопропил)-N-метиламином с получением N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-5-[N-(3-метиламинопропил)-N-метиламино]-2-нитробензамида. Спектр ЯМР: (ДМСОd6) 1,61-1,74(м, 2Н), 2,35(с, 3Н), 2,26(м, 3Н), 2,38-2,44(м, 2Н), 3,09(с, 3Н), 3,5-3,55(м, 6Н), 3,7-3,74(м, 4Н), 6,78(с, 1Н), 6,84(д, 1Н), 7,14(д, 1Н), 7,21(д, 1Н), 7,27(с, 1Н), 7,6(д, 1Н), 7,9(с, 1Н), 8,04(д, 1Н), 8,27(д, 1Н), 9,83(с, 1Н), 10,55 (с, 1Н). Масс спектр: M+H+ 562.
По методике, описанной в шестом параграфе части примечания а), относящейся к получению исходных соединений, N-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3-[N-(3-метиламинопропил)-N-метиламино]-2-нитробензамид каталитически восстанавливают с получением требуемого исходного соединения.
Спектр ЯМР: (ДМСОd6) 1,57-1,62(м, 2Н), 2,2(с, 3Н), 2,25(с, 3Н), 2,47-2,5(м, 2Н), 2,77 (с, 3Н), 3,19-3,23(м, 2Н), 3,5-3,54(м, 4Н), 3,69-3,73(м, 4Н), 5,6(с, 2Н), 6,68(д, 1Н), 6,82(д, 1Н), 7,04(с, 1Н), 7,1(д, 1Н), 7,2-7,23(м, 2Н), 7,54(д, 1Н), 7,83(д, 1Н), 8,26(д, 1Н), 9,75(с, 1Н), 10,28(с, 1Н). Масс спектр: M+H+ 532.
Пример 4
С использованием методики, аналогичной описанной в примере 1, подходящий 2-аминобензамид подвергают взаимодействию с триметилортоформиатом с получением соединений, описанных в таблице II.
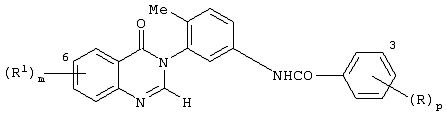
| Таблица II |
| № |
(R1)m |
(R)p |
Прим. |
| 1 |
6-(4-метилпиперазин-1-ил) |
3-морфолино-5-трифторметил |
а |
| 2 |
6-[N-(3-диметиламинопропил)-N-метиламино] |
3-морфолино-5-трифторметил |
b |
| 3 |
8-[N-(3-диметиламинопропил)-N-метиламино] |
3-морфолино-5-трифторметил |
с |
| 4 |
6-метокси |
3-фтор-5-морфолино |
d |
Примечания
а) В качестве реагента используют триметилортоформиат и полученное соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05 (с, 3Н), 2,23 (с, 3Н), 2,5(м, 4Н), 3,3 (м, 8Н), 3,76(т, 4Н), 7,44(М, 3Н), 7,72(м, 6Н), 8,1(с, 1Н), 10,52(ш с, 1Н). Масс спектр. M+H+ 607.
N-[2-Метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-2-амино-5-(4-метилпиперазин-1-ил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Этил-3-морфолино-5-трифторметилбензоат получают из этил-3-фтор-5-трифторметилбензоата по методике, описанной в Brown et al., Tetrahedron Lett., 1999, 40, 1219. Полученное соединение имеет следующие характеристики. Спектр ЯМР: (CDCl3) 1,36(т, 3Н), 3,19(т, 4Н), 3,81(т, 4Н), 4,34(м, 2Н), 7,22(д, 1Н), 7,72(д, 1Н), 7,76(с, 1Н).
Смесь этил-3-морфолино-5-трифторметилбензоата (0,67 г), 1N водного раствора гидроксида натрия (3,3 мл) и этанола (6 мл) перемешивают и нагревают до температуры кипения с обратным холодильником в течение 15 минут и затем оставляют на 16 часов. Этанол выпаривают и остаток растворяют в воде (6 мл). Добавляют соляную кислоту (1М, 3,3 мл) и полученное твердое вещество промывают водой и сушат. Получают 3-морфолино-5-трифторметилбензойную кислоту в виде твердого вещества (0,464 г). Спектр ЯМР: (ДМСОd6) 3,25(т, 4Н), 3,73(т, 4Н), 7,4(с, 1Н), 7,53(с, 1Н), 7,65(с, 1Н), 13,3(с, 1Н).
Раствор 3-морфолино-5-трифторметилбензоилхлорида (11,43 г, полученный взаимодействием бензойной кислоты с оксалилхлоридом с использованием обычной методики) в метиленхлориде (200 мл) добавляют к перемешиваемой смеси 4-метил-3-нитроанилина (5,47 г), триэтиламина (10 мл) и метиленхлорида (200 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 18 часов. Реакционную смесь промывают водой и насыщенным водным раствором бикарбоната натрия, сушат (MgSO4) и выпаривают. Полученное твердое вещество перемешивают с диэтиловым эфиром (300 мл) в течение 16 часов. Полученное твердое вещество собирают, промывают диэтиловым эфиром и сушат. Получают N-(4-метил-3-нитрофенил)-3-морфолино-5-фторбензамид в виде твердого вещества (10,4 г). Спектр ЯМР: (CDCl3) 2,58 (с, 3Н), 3,22 (т, 4Н), 3,83 (т, 4Н), 7,21 (с, 2Н), 7,32 (д, 1Н), 7,41 (с, 1Н), 7,58 (с, 1Н), 7,82 (м, 1Н), 8,02 (с, 1Н), 8,23 (д, 1Н).
Полученное соединение растворяют в этилацетате (500 мл) и гидрируют над катализатором 10% палладием на углеродероде (1,1 г) под давлением водорода 3 атмосферы до тех пор, пока не прекратится поглощение водорода. Катализатор удаляют фильтрацией и фильтрат выпаривают. Остаток растирают под этилацетатом с получением N-(3-амино-4-метилфенил)-3-морфолино-5-трифторметилбензамида (8,1 г). Спектр ЯМР: (COCl3) 2,01(с, 3Н), 3,23(т, 4Н), 3,75(т, 4Н), 4,81(с, 2Н), 6,77(м, 1Н), 6,83(д, 1Н), 7,02(д, 1Н), 7,25(с, 1Н), 7,58(с, 1Н), 7,63(с, 1Н), 9,9(с, 1Н).
Диизопропилэтиламин (0,918 мл) добавляют к смеси N-(3-амино-4-метилфенил)-3-морфолино-5-трифторметилбензамида (1 г), 5-хлор-2-нитробензойной кислоты (0,584 г), 2-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилуронийгексафторфосфата(V) (1.2 г) и ДМФ (6 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение 16 часов. Смесь выливают в смесь льда и воды и полученный осадок выделяют, промывают последовательно метанолом и изогексаном и сушат в вакууме при температуре 55°С. Получают N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-5-хлор-2-нитробензамид (0,965 г). Спектр ЯМР: (ДМСОd6) 2,24 (с, 3Н), 3,3(м, 4Н), 3,76(м, 4Н), 7,23(д, 1Н), 7,36(с, 1Н), 7,6(д, 1Н), 7,65(с, 1Н), 7,72(с, 1Н), 7,82(д, 1Н), 7,90(м, 2Н), 8,17(д, 1Н), 10,17 (с, 1Н), 10, 38 (с, 1Н). Масс спектр: М+Н+ 563.
Смесь части (0,45 г) полученного соединения и N-метилпиперазина (2 мл) перемешивают и нагревают при температуре 120°С в течение 16 часов. Реакционную смесь выливают в смесь льда и воды. Полученное твердое вещество выделяют, промывают водой и сушат в вакууме при температуре 55°С. Полученное твердое вещество очищают хроматографией на ионообменной колонке (колонка isolute SCX), используя сначала метанол и затем смесь метанола и 1% водного раствора гидроксида аммония в качестве элюента. Получают N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-5-(4-метилпиперазин-1-ил)-2-нитробензамид (0,29 г). Спектр ЯМР: (ДМСОd6) 2,21 (с, 3Н), 2,24 (с, 3Н), 2,5-3,3 (м, 8Н), 3,48 (м, 4Н), 3,76 (м, 4Н), 7,0 (д, 1Н), 7,07 (д, 1Н), 7,2 (д, 1Н), 7,36 (с, 1Н), 7,6 (м, 3Н), 7,88 (с, 1Н), 8,04 (д, 1Н), 9,84 (с, 1Н), 10,37 (с, 1Н). Масс спектр: М+Н+ 627.
Смесь полученного соединения, формиата аммония (0,146 г), катализатора 10% палладия на углероде (0,029 г) и метанола (5 мл) перемешивают и нагревают при температуре 65°С в течение 2 часов. Полученную смесь фильтруют и фильтрат выпаривают. Остаток растирают под метиленхлоридом и фильтруют. Фильтрат выпаривают с получением N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-2-амино-5-(4-метилпиперазин-1-ил)бензамида, который используют без дальнейшей очистки.
b) В качестве реагента используют триметилортоформиат и продукт имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,67(м, 2Н), 2,05(с, 3Н), 2,13(с, 6Н), 2,27(м, 2Н), 3,0(с, 1Н), 3,3(м, 4Н), 3,47(м, 2Н), 3,76(ш с, 4Н), 7,25(д, 1Н), 7,39(м, 3Н), 7,62(м, 3Н), 7,73(д, 1Н), 7,81(д, 1Н), 8,0(с, 1Н), 10,51(ш с, 1Н). Масс спектр: M+H+ 623.
N -[2-Метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-2-амино-5-[N-(3-диметиламинопропил)-N-метиламино]бензамид, используемый в качестве исходного материала, получают следующим образом.
Смесь N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-5-хлор-2-нитробензамида (0,45 г), N-(3-диметиламинопропил)-N-метиламина (2 мл) и ДМСО (1 мл) перемешивают и нагревают при температуре 120°С в течение 16 часов. Реакционную смесь выливают в смесь льда и воды. Полученное твердое вещество выделяют, промывают водой и сушат в вакууме при температуре 55°С. Получают N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-5-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамид (0,51 г). Спектр ЯМР: (ДМСОd6) 1,69(м, 2Н), 2,12(с, 6Н), 2,24(м, 5Н), 3,08(с, 3Н), 3,3(м, 4Н), 3,52(т, 2Н), 3,76(м, 4Н), 6,76(С, 1Н), 6,83(д, 1Н), 7,2(д, 1Н), 7,36(с, 1Н), 7,66(м, 3Н), 7,89(с, 1Н), 8,04(д, 1Н), 9,82(с, 1Н), 10,37(с, 1Н).
Смесь полученного соединения, формиата аммония (0,24 г), катализатора 10% палладия на углероде (0,05 г) и метанола (10 мл) перемешивают и нагревают при температуре 65°С в течение 7 часов. Полученную смесь фильтруют и фильтрат выпаривают. Остаток растирают под метиленхлоридом и фильтруют. Фильтрат выпаривают с получением N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-2-амино-5-[N-(3-диметиламинопропил)-N-метиламино]бензамида, который используют без дальнейшей очистки.
с) В качестве реагента используют триметилортоформиат и продукт имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,72(м, 2Н), 2,06(м, 9Н), 2,19(т, 2Н), 2,94(с, 3Н), 3,3(м, 4Н), 3,49(т, 2Н), 3,76(ш с, 4Н), 7,26(д, 1Н), 7,42(м, 3Н), 7,68(м, 3Н), 7,8(м, 2Н), 8,21(с, 1Н), 10,49(ш с, 1Н). Масс спектр: М+Н+ 623.
N-[2-Метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-2-амино-3-[N-(3-диметиламинопропил)-N-метиламино]бензамид, используемый в качестве исходного материала, получают следующим образом.
Диизопропилэтиламин (0,46 мл) добавляют к смеси N-(3-амино-4-метилфенил)-3-морфолино-5-трифторметилбензамида (0,5 г), 3-хлор-2-нитробензойной кислоты (0,292 г), 2-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилуронийгексафторфосфата(V) (0,6 г) и ДМФ (3 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение 16 часов. Смесь выливают в смесь льда и воды и полученный осадок выделяют, промывают последовательно метанолом и изогексаном и сушат в вакууме при температуре 55°С. Получают N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-3-хлор-2-нитробензамид (0,45 г). Спектр ЯМР: (ДМСОd6) 2,22 (с, 3Н), 3,3 (м, 4Н), 3,76(м, 4Н), 7,25(д, 1Н), 7,37(с, 1Н), 7,71(м, 5Н), 7,96(д, 2Н), 10,36(ш с, 1Н), 10,38(ш с, 1Н). Масс спектр: M+H+ 563.
Смесь полученного соединения, N-(3-диметиламинопропил)-N-метиламина (2 мл) и ДМСО (1 мл) перемешивают и нагревают при температуре 120°С в течение 16 часов. Реакционную смесь выливают в смесь льда и воды. Полученное твердое вещество выделяют, промывают водой и сушат в вакууме при температуре 55°С. Получают N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-3-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамид (0,51 г). Спектр ЯМР: (ДМСОd6) 1,52(м, 2Н), 2,06(с, 6Н), 2,15(м, 2Н), 2,22(с, 3Н), 2,69(с, 3Н), 3,03(т, 2Н), 3,3(м, 4Н), 3,76(м, 4Н), 7,22(д, 1Н), 7,36(м, 2Н), 7,53(м, 4Н), 7,73(д, 2Н), 10,14(ш с, 1Н), 10,35(ш с, 1Н).
Смесь полученного соединения, формиата аммония (0,24 г), катализатора 10% палладия на углероде (0,05 г) и метанола (10 мл) перемешивают и нагревают при температуре 65°С в течение 7 часов. Полученную смесь фильтруют и фильтрат выпаривают. Остаток растирают под метиленхлоридом и фильтруют. Фильтрат выпаривают с получением N-[2-метил-5-(3-морфолино-5-трифторметилбензамидо)фенил]-2-амино-3-[N-(3-диметиламинопропил)-N-метиламино]бензамида, который используют без дальнейшей очистки.
d) В качестве реагента используют триметилортоформиат и продукт имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,06(с, 3Н), 3,21(м, 4Н), 3,73(м, 4Н), 3,89(с, 3Н), 6,97(д, 1Н), 7,11(д, 1Н), 7,29(с, 1Н), 7,42(д, 1Н), 7,49(д, 1Н), 7,58(д, 1Н), 7,72(д, 1Н), 7,78(м, 2Н), 8,17(с, 1Н), 10,33(с, 1Н). Масс спектр: M+H+ 489.
N-[2-Метил-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-метоксибензамид, используемый в качестве исходного материала, получают следующим образом.
Раствор 3,5-дифторбензоилхлорида (2,82 г) в метиленхлориде (20 мл) добавляют к перемешиваемой смеси 4-метил-3-нитроанилина (2,28 г), триэтиламина (4,35 мл) и метиленхлорида (80 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Осадок выделяют, промывают метиленхлоридом и сушат. Получают N-(4-метил-3-нитрофенил)-3,5-дифторбензамид. Спектр ЯМР: (ДМСОd6) 2,43(с, 3Н), 7,43(м, 2Н), 7,63(м, 2Н), 7,95(м, 2Н), 8,43(д, 1Н), 10,42(с, 1Н).
Масс спектр: M+H+ 293.
Смесь части (1 г) полученного соединения и морфолина (5 мл) перемешивают и нагревают при температуре 100°С в течение 48 часов и до температуры 120°С в течение 24 часов. Реакционную смесь охлаждают и выливают в воду (100 мл). Полученное твердое вещество выделяют, промывают водой и сушат. Полученное соединение очищают хроматографией на колонке с двуокисью кремния, используя 1:1 смесь изогексана и этилацетата в качестве элюента. Получают N-(4-метил-3-нитрофенил)-3-фтор-5-морфолинобензамид в виде твердого вещества (0,53 г). Спектр ЯМР: (ДМСОd6) 2,46(с, 3Н), 3,22(т, 4Н), 3,75(т, 4Н), 6,98(м, 1Н), 7,12(д, 1Н), 7,27(с, 1Н), 7,46(д, 1Н), 7,96(м, 1Н), 8,43(д, 1Н), 10,48 (с, 1Н). Масс спектр: М+Н+ 360.
Часть (0,483 г) полученного соединения растворяют в этилацетате (40 мл) и гидрируют над катализатором 10% палладием на углероде (0,6 г) в атмосфере водорода до тех пор, пока не прекратится поглощение водорода. Катализатор удаляют фильтрацией и фильтрат выпаривают. Остаток растирают под диэтиловым эфиром (25 мл). Полученное твердое вещество сибирают, промывают диэтиловым эфиром и сушат. Получают N-(3-амино-4-метилфенил)-3-фтор-5-морфолинобензамид (0,341 г). Спектр ЯМР: (ДМСОd6) 1,99(с, 3Н), 3,19(т, 4Н), 3,76(т, 4Н), 4,8(с, 2Н), 6,75(д, 1Н), 6,82(д, 1Н), 6,9(д, 1Н), 7,02(с, 1Н), 7,04(д, 1Н), 7,23(с, 1Н), 9,81(с, 1Н).
Оксалилхлорид (0,523 мл) добавляют к перемешиваемой смеси 5-метокси-2-нитробензойной кислоты (0,99 г), ДМФ (несколько капель) и метиленхлорида (30 мл) и смесь перемешивают при температуре окружающей среды в течение 3,5 часов. Смесь выпаривают и остаток растворяют в метиленхлориде (30 мл) и последовательно добавляют N-(3-амино-4-метилфенил)-3-фтор-5-морфолинобензамид (1,65 г) и триэтиламин (0,697 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 2 часов. Смесь выпаривают и остаток растирают под водой. Полученное твердое вещество выделяют, промывают последовательно насыщенным водным раствором бикарбоната натрия, водой и диэтиловым эфиром и сушат в вакууме при температуре 55°С. Получают N-[2-метил-5-(3-фтор-5-морфолинобензамидо)фенил]-5-метокси-2-нитробензамид (2,29 г). Спектр ЯМР: (ДМСОd6) 2,24(с, 3Н), 3,23(м, 4Н), 3,75(м, 4Н), 3,95(с, 3Н), 6,96(д, 1Н), 7,17(м, 4Н), 7,32(с, 1Н), 7,58(д, 1Н), 7,89(с, 1Н), 8,18(д, 1Н), 10,0(с, 1Н), 10,22(с, 1Н). Масс спектр: М+Н+ 509.
Смесь части (1,28 г) полученного соединения, катализатора 10% палладия на углероде (0,128 г) и метанола (60 мл) перемешивают в атмосфере водорода в течение 20 часов. Добавляют этилацетат (30 мл) и реакционную смесь перемешивают в течение еще 2 часов в атмосфере водорода. Реакционную смесь фильтруют и фильтрат выпаривают. Остаток растворяют в минимальном количестве этилацетата и твердое вещество осаждают добавлением диэтилового эфира. Твердое вещество выделяют и сушат в вакууме при температуре 55°С. Получают N-[2-метил-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-метоксибензамид (0,98 г).
Спектр ЯМР: (ДМСОd6) 2,2 (с, 3Н), 3,22(м, 4Н), 3,74(м, 7Н), 5,93(ш с, 2Н), 6,72(д, 1Н), 6,92(м, 2Н), 7,12(д, 1Н), 7,22(д, 1Н), 7,27(м, 2Н), 7,54(д, 1Н), 7,77(с, 1Н), 9,69(с, 1Н), 10,14(с, 1Н). Масс спектр: M+H+ 479.
Пример 5
3-[5-(2-Хлорпирид-4-илкарбониламино)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он
2-Хлорпиридин-4-карбонилхлдорид (0,61 г) добавляют к перемешиваемой смеси 3-(5-амино-2-метилфенил)-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-она (1 г), триэтиламина (1 г) и метиленхлорида (15 мл) и полученную смесь перемешивают при температуре окружающей среды в течение 18 часов. Смесь промывают насыщенным водным раствором бикарбоната натрия и органическую фазу выпаривают. Получают указанное в заголовке соединение (1,28 г). Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,22(с, 3Н), 2,46-2,5(м, 4Н), 3,25-3,28(м, 4Н), 7,42-7,47(м, 2Н), 7,62(с, 1Н), 7,76-7,79(м, 2Н), 7,85(д, 1Н), 7,98(с, 1Н), 8,07(с, 1Н), 8,61(д, 1Н), 10,65(с, 1Н). Масс спектр: M+H+ 489 и 491.
3-(5-Амино-2-метилфенил)-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он, используемый в качестве исходного соединения, получают следующим образом.
Оксалилхлорид (8,5 мл) по каплям добавляют к перемешиваемому раствору 5-хлор-2-нитробензойной кислоты (15,1 г) в смеси метиленхлорида (200 мл) и ДМФ (несколько капель), охлажденному до температуры 0°С. Смесь нагревают при температуре окружающей среды и перемешивают в течение еще 4 часов. Растворитель выпаривают. Остаток растворяют в метиленхлориде (300 мл) и по каплям добавляют к перемешиваемой смеси 2-метил-5-нитроанилина (10,6 г), триэтиламина (27,2 мл) и метиленхлорида (300 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Осадок выделяют, промывают последовательно водой и диэтиловым эфром и сушат в вакууме при температуре 40°С. Получают N-(2-метил-5-нитрофенил)-5-хлор-2-нитробензамид (24,9 г). Спектр ЯМР: (ДМСОd6) 2,34(с, 3Н), 7,46(Д, 1Н), 7,75(с, 1Н), 7,88(д, 1Н), 8,03-8,16(м, 2Н), 8,56(с, 1Н). Масс спектр: M+H+ 335.
Смесь части (15 г) полученного соединения и N-метилпиперазина (24,8 мл) перемешивают и нагревают при температуре 100°С в течение 16 часов. Реакционную смесь охлаждают до температуры окружающей среды и выливают в воду. Полученный осадок выделяют, промывают водой и сушат в вакууме при температуре 40°С. Получают N-(2-метил-5-нитрофенил)-5-(4-метилпиперазин-1-ил)-2-нитробензамид (14,8 г). Спектр ЯМР: (ДМСОd6) 2,22(с, 3Н), 2,38(с, 3Н), 2,41-2,45(м, 4Н), 3,48-3,53(м, 4Н), 7,08(д, 1Н), 7,17(с, 1Н), 7,53(д, 1Н), 7,98(д, 1Н), 8,07(д, 1Н), 8,53 (с, 1Н), 10,15 (с, 1Н). Масс спектр: М+Н+ 400.
Смесь полученного соединения, катализатора 10% палладия на углероде (1,48 г) и метанола (500 мл) перемешивают в атмосфере водорода до тех пор, пока не прекратится поглощение водорода. Катализатор отфильтровывают и фильтрат выпаривают. Получают N-(5-амино-2-метилфенил)-2-амино-5-(4-метилпиперазин-1-ил)бензамид (10,11 г). Спектр ЯМР: (ДМСОd6) 2,02(с, 3Н), 2,2 (с, ЗН), 2,4-2,45(м, 4Н), 2,97-3,0(м, 4Н), 4,84(с, 2Н), 5,82(с, 2Н), 6,36(д, 1Н), 6,57(с, 1Н), 6,66(д, 1Н), 6,85(д, 1Н), 6,92(д, 1Н), 7,18 (с, 1Н), 9,4(с, 1Н). Масс спектр: M+H+ 340.
Смесь части (8,27 г) полученного материала, триэтилортоформиата (8,27 мл), ледяной уксусной кислоты (0,7 мл) и этанола (150 мл) перемешивают и нагревают при температуре 70°С в течение 16 часов. Добавляют 1N водный раствор соляной кислоты (24 мл) и смесь перемешивают при температуре 60°С в течение 1 часа. Полученную смесь выпаривают. Остаток растворяют в воде, подщелачивают добавлением бикарбоната натрия и экстрагируют метиленхлоридом. Органический экстракт выпаривают с получением 3-(5-амино-2-метилфенил)-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-она (8,29 г). Спектр ЯМР: (ДМСОd6) 1,86(с, 3Н), 2,22(с, 3Н), 2,42-2,45(м, 4Н), 3,24-3,28(м, 4Н), 5,14(с, 2Н), 6,47(с, 1Н), 6,61(д, 1Н), 7,02(д, 1Н), 7,45(с, 1Н), 7,59 (с, 1Н), 7,96(с, 1Н). Масс спектр: M+H+ 350.
Пример 6
3-[2-Метил-5-(2-пирролидин-1-илпирид-4-илкарбониламино)фенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он
Смесь 3-[5-(2-хлорпирид-4-илкарбониламино)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-она (0,18 г) и пирролидина (2 мл) перемешивают и нагревают при температуре 100°С в течение 16 часов. Смесь охлаждают до температуры окружающей среды и выливают в воду. Полученное твердове вещество выделяют, промывают водой и сушат в вакууме при температуре 40°С. Получают указанное в заголовке соединение (0,11 г).
Спектр ЯМР: (ДМСОd6) 1,94-1,97(м, 4Н), 2,04(с, 3Н), 2,22(с, 3Н), 2,45-2,49(м, 4Н), 3,25-3,28(м, 4Н), 3,4-3,45(м, 4Н), 6,85(с, 1Н), 6,96(д, 1Н), 7,42(д, 1Н), 7,42(д, 1Н), 7,44(с, 1Н), 7,62(с, 2Н), 7,77-7,79(м, 2Н), 8,07(с, 1Н), 8,2(с, 1Н), 10,42(с, 1Н). Масс спектр: М+Н+ 524.
Пример 7
Используя методику, аналогичную той, что описана в примере 6, подходящий 6-замещенный 3-[5-(2-хлорпирид-4-илкарбониламино)-2-метилфенил]-3,4-дигидрохиназолин-4-он подвергают взаимодействию с подходящим амином с получением соединений, описанных в таблице III.
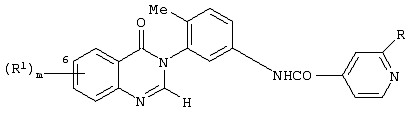
| Таблица III |
| № |
(R1)m |
R |
Прим. |
| 1 |
6-(4-метилпиперазин-1-ил) |
пиперидино |
а |
| 2 |
6-(4-метилпиперазин-1-ил) |
3-пирролин-1-ил |
b |
| 3 |
6-(4-метилпиперазин-1-ил) |
гомопиперидин-1-ил |
с |
| 4 |
6-(4-метилпиперазин-1-ил) |
азетидин-1-ил |
d |
| 5 |
6-(4-метилгомопиперазин-1-ил) |
пиперидино |
е |
| 6 |
6-(4-метилгомопиперазин-1-ил) |
пирролидин-1-ил |
f |
| 7 |
6-(4-метилгомопиперазин-1-ил) |
морфолино |
9 |
Примечания
a) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,5-1,64(м, 6Н), 2,04(с, 3Н), 2,2(с, 3Н), 2,45-2,49(м, 4Н), 3,26-3,29(м, 4Н), 3,55-3,59(м, 4Н), 6,98(д, 1Н), 7,19(с, 1Н), 7,42(д, 1Н), 7,47(с, 1Н), 7,62(с, 2Н), 7,76-7,78(м, 2Н), 8,07(с, 1Н), 8,21(с, 1Н), 10,42(с, 1Н). Масс спектр: М+Н+ 538.
b) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,04(с, 3Н), 2,22(с, 3Н), 2,47-2,5(м, 4Н), 3,25-3,31(м, 4Н), 4,23(с, 4Н), 6,03(с, 2Н), 6,87(с, 1Н), 7,01(д, 1Н), 7,42(д, 1Н), 7,47(с, 2Н), 7,62(д, 2Н), 7,76-7,81(м, 2Н), 8,07(с, 1Н), 8,23(д, 1Н), 10,45(с, 1Н). Масс спектр: M+H+ 522.
c) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,45-1,47(м, 4Н), 1,54-1,56(м, 4Н), 2,04(с, 3Н), 2,22(с, 3Н), 2,45-2,5(м, 4Н), 3,25-3,27(м, 4Н), 3,62-3,64(м, 4Н), 6,91(д, 1Н), 6,96(с, 1Н), 7,02(д, 1Н), 7,42(д, 1Н), 7,47(с, 1Н), 7,62(с, 2Н), 7,76-7,81(м, 2Н), 8,07(с, 1Н), 8,18(д, 1Н), 10,42(с, 1Н). Масс спектр: M+H+ 552.
d) Соединение имеет следующие характеристики. Масс спектр: M+H+ 510.
e) Соединение имеет следующие характеристики. Спектр ЯМР: (CDCl3) 1,42-1,46(м, 6Н), 1,78 (с, 3Н), 1,92-2,04(м, 2Н), 2,48(с, 3Н), 2,48-2,56(м, 2Н), 2,64-2,72(м, 2Н), 3,44-3,58(м, 6Н), 3,6-3,64(м, 2Н), 6,78(д, 1Н), 7,01(с, 1Н), 7,15-7,2(м, 2Н), 7,38(с, 1Н), 7,5(с, 1Н), 7,58-7,68(м, 3Н), 8,12(д, 1Н), 8,4(с, 1Н). Масс спектр: M+H+ 552.
f) Соединение имеет следующие характеристики. Спектр ЯМР: (CDCl3) 1,84-2,04(м, 9Н), 2,32(с, 3Н), 2,48-2,58(м, 2Н), 2,64-2,7(м, 2Н), 3,32-3,44(м, 4Н), 3,5-3,58(м, 2Н), 3,6-3,64(м, 2Н), 6,72-6,79(м, 2Н), 7,14-7,2(м, 2Н), 7,38(с, 1Н), 7,52-7,62(м, 3Н), 7,64(с, 1Н), 8,12(д, 1Н), 8,44(с, 1Н). Масс спектр: М+Н+ 538.
g) Соединение имеет следующие характеристики. Спектр ЯМР: (CDCl3) 1,98(с, 3Н), 2,02-2,12(м, 2Н), 2,39(с, 3Н), 2,58-2,62(м, 2Н), 2,74-2,8(м, 2Н), 3,5-3,58(м, 4Н), 3,6-3,66(м, 2Н), 3,66-3,78(м, 6Н), 6,98(д, 1Н), 7,08(с, 1Н), 7,2-7,26(м, 2Н), 7,44(с, 1Н), 7,58(С, 1Н), 7,64(д, 1Н), 7,72-7,78(м, 2Н), 8,24(д, 1Н), 8,44(с, 1Н). Масс спектр: M+H+ 554.
Пример 8
3-[5-(3,5-Дифторбензамидо)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он
3,5-Дифторбензоилхлорид (0,91 г) добавляют к перемешиваемой смеси 3-(5-амино-2-метилфенил)-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-она (1,5 г), триэтиламина (1,04 г) и метиленхлорида (50 мл) и полученную смесь перемешивают при температуре окружающей среды в течение 18 часов. Смесь промывают насыщенным водным раствором бикарбоната натрия и органическую фазу выпаривают. Получают указанное в заголовке соединение (2,04 г). Спектр ЯМР: (ДМСОd6) 2,05 (с, 3Н), 2,22(с, 3Н), 2,45-2,5(м, 4Н), 3,24-3,3(м, 4Н), 7,41-7,56(м, 3Н), 7,61-7,68(м, 4Н), 7,75-7,79(м, 2Н), 8,06(с, 1Н), 10,5(с, 1Н). Масс спектр: М+Н+ 490.
Пример 9
По методике, описанной в примере 6, 3-[5-(3,5-дифторбензамидо)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он, 3-[5-(3-фтор-4-трифторметилбензамидо)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он или 3-[5-(3,5-дифторбензамидо)-2-метилфенил]-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он соответствующим образом подвергают взаимодействию с подходящим амидом с получением соединений, описанных в таблице IV.

| Таблица IV |
| № |
(R1)m |
(R)p |
Прим. |
| 1 |
6-(4-метилпиперазин-1-ил) |
3-фтор-5-пирролидин-1-ил |
а |
| 2 |
6-(4-метилпиперазин-1-ил) |
3-фтор-5-пиперидино |
b |
| 3 |
6-(4-метилпиперазин-1-ил) |
3-азетидин-1-ил-5-фтор |
с |
| 4 |
6-(4-метилпиперазин-1-ил) |
3-фтор-5-(3-пирролин-1-ил) |
d |
| 5 |
6-(4-метилпиперазин-1-ил) |
3-фтор-3-морфолино |
е |
| 6 |
6-(4-метилпиперазин-1-ил) |
3-морфолино-5-трифторметил |
f |
| 7 |
6-(4-метилгомопиперазин-1-ил) |
3-фтор-5-пирролидин-1-ил |
g |
| 8 |
6-(4-метилгомопиперазин-1-ил) |
3-фтор-5-пиперидино |
h |
Примечания
a) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,95-2,0(м, 4Н), 2,04 (с, 3Н), 2,18(с, 3Н), 2,0-2,23(м, 4Н), 2,47-2,5(м, 4Н), 3,25-3,3(м, 4Н), 6,84-6,89(м, 2Н), 7,22(д, 1Н), 7,4(д, 1Н), 7,47(с, 1Н), 7,6-7,62(м, 2Н), 7,76-7,82(м, 2Н), 8,07 (с, 1Н), 10,27(с, 1Н). Масс спектр: M+H+ 541.
b) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,22-1,58(м, 6Н), 2,04(с, 3Н), 2,2(с, 3Н), 2,45-2,5(м, 4Н), 3,25-3,29(м, 4Н), 6,91(д, 1Н), 7,02(д, 1Н), 7,26(с, 1Н), 7,4(д, 1Н), 7,47(с, 1Н), 7,62(с, 2Н), 7,76-7,81(м, 2Н), 8,06(с, 1Н), 10,3(с, 1Н). Масс спектр: М+Н+ 555.
c) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 527.
d) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 539.
e) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 557.
f) 3-[5-(3-Фтор-4-трифторметилбензамидо)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он и морфолин нагревают вместе при температуре 130°С в течение 4 дней. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,22(с, 3Н), 2,4-2,6(м, 4Н), 2,86-2,96(м, 4Н), 3,22-3,32(м, 4Н), 3,64-3,74(м, 4Н), 7,4-7,48(м, 2Н), 7,62(с, 2Н), 7,76-7,86(м, 4Н), 8,06(д, 2Н), 10,53(с, 1Н). Масс спектр: М+Н+ 607.
g) 3-[5-(3,5-Дифторбензамидо)-2-метилфенил]-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он и пирролидин нагревают вместе при температуре 95°С в течение 16 часов и при температуре 105°С в течение 4 дней. Соединение имеет следующие характеристики. Спектр ЯМР: (CDCl3) 1,98-2,1(м, 9Н), 2,19(с, 3Н), 2,58-2,62(м, 2Н), 2,72-2,8(м, 2Н), 3,24-3,32(м, 4Н), 3,58-3,62(м, 2Н), 3,68-3,72(м, 2Н), 6,32(д, 1Н), 6,76(д, 1Н), 6,82(с, 1Н), 7,2-7,3(м, 2Н), 7,44(с, 1Н), 7,6-7,68(м, 3Н), 7,78(с, 1Н), 8,19(с, 1Н). Масс спектр: М+Н+ 555.
h) Соединение имеет следующие характеристики. Спектр ЯМР: (CDCl3) 1,52-1,74(м, 6Н), 2,02-2,1(м, 5Н), 2,4(с, 3Н), 2,58-2,6(м, 2Н), 2,76-2,8(м, 2Н), 3,18-3,28(м, 4Н), 3,58-3,62(м, 2Н), 3,68-3,72 (м, 2Н), 6,68(д, 1Н), 6,88(д, 1Н), 7,18(с, 1Н), 7,2-7,32(м, 2Н), 7,44(с, 1Н), 7,6-7,68(м, 3Н), 7,78(с, 1Н), 8,17 (с, 1Н). Масс спектр: М+Н+ 569.
Пример 10
3-[5-Дибензофуран-4-илкарбониламино-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он
Раствор 3-(5-амино-2-метилфенил)-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-она (0,165 г) в ДМФ (0,5 мл) добавляют к перемешиваемой смеси дибензофуран-4-карбоновой кислоты (0,1 г), диизопропилэтиламина (0,164 мл), 2-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилуронийгексафторфосфата(V) (0,214 г) и ДМФ (0,5 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение 16 часов. Смесь разбавляют водой и полученное твердое вещество выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 55°С. Получают указанное в заголовке соединение (0,228 г). Спектр ЯМР: (ДМСОd6) 2,07(с, 3Н), 2,25(с, 3Н), 2,5-3,3(м, 8Н), 7,55(м, 7Н), 7,83(м, 4Н), 8,12(с, 1Н), 8,21(д, 1Н), 8,34(д, 1Н), 10,59(с, 1Н). Масс спектр: М+Н+ 544.
Пример 11
По методике, аналогичной описанной в примере 10, 3-(5-амино-2-метилфенил)-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он, 3-(5-амино-2-метилфенил)-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он или 3-(5-амино-2-метилфенил)-8-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он подвергают взаимодействию с подходящей карбоновой кислотой с получением соединений, описанных в таблице V.

| Таблица V |
| № |
(R1)m |
(R)p |
Прим. |
| 1 |
6-(4-метилпиперазин-1-ил) |
2-метокси-3-фенил |
а |
| 2 |
6-(4-метилпиперазин-1-ил) |
3-(4-фторфенил) |
b |
| 3 |
6-(4-метилпиперазин-1-ил) |
3-(2-фурил) |
с |
| 4 |
6-(4-метилпиперазин-1-ил) |
3-циклопентилокси |
d |
| 5 |
6-(4-метилпиперазин-1-ил) |
3-циклопентилокси-4-метокси |
е |
| 6 |
6-(4-метилпиперазин-1-ил) |
3-ацетамидо |
f |
| 7 |
6-(4-метилпиперазин-1-ил) |
3-(N-метилметансульфонамидо) |
g |
| 8 |
6-(4-метилпиперазин-1-ил) |
3-(1,1-диоксидоизотиазолидин-2-ил) |
h |
| 9 |
6-(4-метилпиперазин-1-ил) |
3-морфолино |
i |
| 10 |
6-(4-метилпиперазин-1-ил) |
3-фтор-4-трифторметил |
j |
| 11 |
6-(4-метилпиперазин-1-ил) |
3-тетрагидрофуранилокси |
k |
| 12 |
6-(4-метилпиперазин-1-ил) |
2-метокси |
l |
| 13 |
6-(4-метилпиперазин-1-ил) |
3-этокси |
m |
| 14 |
6-(4-метилпиперазин-1-ил) |
3-(1,1,2,2-тетрафторэтокси) |
n |
| 15 |
6-(4-метилгомопиперазин-1-ил) |
3-морфолино |
о |
| 16 |
6-(4-метилгомопиперазин-1-ил) |
3-фтор-5-морфолино |
p |
| 17 |
6-(4-метилгомопиперазин-1-ил) |
3-морфолино-5-трифторметил |
q |
| 18 |
6-(4-метилгомопиперазин-1-ил) |
3-(2-фурил) |
r |
| 19 |
8-(4-метилпиперазин-1-ил) |
3-морфолино |
s |
| 20 |
8-(4-метилпиперазин-1-ил) |
3-фтор-5-морфолино |
t |
| 21 |
8-(4-метилпиперазин-1-ил) |
3-морфолино-5-трифторметил |
u |
| 22 |
8-(4-метилпиперазин-1-ил) |
3-(2-фурил) |
v |
| 23 |
8-(4-метилпиперазин-1-ил) |
3-(4-фторфенил) |
w |
Примечания
а) Продукт реакции очищают хроматографией на колонке с обращенной фазой с двуокисью кремния, используя сначала воду и затем смеси метанола и воды со снижающейся полярностью в качестве элюента. Получают требуемое соединение с 33% выходом. Спектр ЯМР: (ДМСОd6) 2,04(с, 3Н), 2,27(с, 3Н), 2,5-3,3(м, 8Н), 3,42(с, 3Н), 7,54(м, 13Н), 7,72(д, 1Н), 8,09(с, 1Н), 10,52(с, 1Н). Масс спектр: M+H+ 560.
2-Метокси-3-фенилбензойную кислоту, используемую в качестве исходного соединения, получают следующим образом.
Метилйодид (0,409 мл) добавляют к перемешиваемой смеси метил-2-гидрокси-3-фенилбензоата (0,5 г), карбоната калия (0,606 г) и ацетона (5 мл) и реакционную смесь перемешивают при температуре 55°С в течение 2,5 часов. Смесь выпаривают и остаток разделяют между этилацетатом и водой. Органическую фазу сушат (MgSO4) и выпаривают с получением смеси исходного соединения и метил 2-метокси-3-фенилбензоата. Полученную смесь растворяют в ДМФ и добавляют карбонат калия (0,606 г) и диметилсульфат (0,207 мл) и полученную реакционную смесь перемешивают при температуре 80°С в течение 16 часов. Смесь разделяют между этилацетатом и водой. Органическую фазу сушат (MgSO4) и выпаривают с получением метил-2-метокси-3-фенилбензоата (0,458 г) в виде масла. Спектр ЯМР: (ДМСОd6) 3,48(с, 3Н), 3,94(с, 3Н), 7,21(м, 1Н), 7,4(м, 6Н), 7,73(д, 1Н).
Смесь полученного соединения, 2N водного раствора гидроксида натрия (5 мл), метанола (10 мл) и ТГФ (3 мл) перемешивают при температуре окружающей среды в течение 16 часов. Органические растворители выпаривают и водную реакционную смесь подкисляют добавлением 2N водного раствора соляной кислоты. Осадок выделяют, промывают водой и сушат в вакууме при температуре 55°С. Получают 2-метокси-3-фенилбензойную кислоту (0,395 г). Спектр ЯМР: (ДМСОd6) 3,4(с, 3Н), 7,25(т, 1Н), 7,4(м, 6Н), 7,62(д, 1Н), 12,92(ш с, 1Н).
b) Исходное соединение, 3-(4-фторфенил)бензойная кислота, описано в Tetrahedron, 1997, 53, 14437-14450. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,02(с, 3Н), 2,32(с, 3Н), 2,42-2,49(м, 4Н), 3,25-3,29(м, 4Н), 7,28-7,38(м, 2Н), 7,41-7,48(м, 2Н), 7,57-7,84(м, 3Н), 7,84-7,88(м, 5Н), 7,92(д, 1Н), 8,06(с, 1Н), 8,19(с, 1Н). Масс спектр: M+H+ 548.
c) Исходное соединение, 3-(2-фурил)бензойная кислота, описано в Tetrahedron Letters, 1998, 39, 4175-4178. Продукт очищают хроматографией на ионообменной колонке isolute SCX, используя сначала метанол, затем 99:1 смесь метанола и насыщенного водного раствора гидроксида аммония в качестве элюента, получая следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,23(с, 3Н), 2,45-2,5(м, 4Н), 3,2-3,35(м, 4Н), 6,62(с, 1Н), 7,06(с, 1Н), 7,42(с, 1Н), 7,48(с, 1Н), 7,57-7,63(м, 3Н), 7,78-7,84(м, 4Н), 7,9(д, 1Н), 8,08(с, 1Н), 8,24(с, 1Н), 10,49(с, 1Н). Масс спектр: M+H+ 520.
d) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,69-1,8 (м, 6Н), 1,84-1, 98 (м, 2Н), 2,04 (с, 3Н), 2,24(с, 3Н), 2,45-2,5(м, 4Н), 3,25-3,29(м, 4Н), 4,86-4,92(м, 1Н), 7,05(д, 1Н), 7,37-7,48(м, 5Н), 7,63(с, 2Н), 7,79(д, 2Н), 8,07(с, 1Н), 10,32(с, 1Н). Масс спектр: M+H+ 538.
3-Циклопентилоксибензойную кислоту, используемую в качестве исходного соединения, получают следующим образом.
1,1'-Азодикарбонилдипиперидин (6,64 г) добавляют к перемешиваемой смеси циклопентанола (1,59 мл), этил-3-гидроксибензоата (4,37 г), трибутилфосфина (6,48 мл) и ТГФ (100 мл) и полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Смесь фильтруют и фильтрат выпаривают. Остаток очищают хроматографией на колонке с двуокисью кремния, используя изогексан в качестве элюента. Получают этил-3-циклопентилоксибензоат (4,3 г). Масс спектр: М+Н+ 235.
Смесь части (1 г) полученного соединения, 2N водного раствора гидроксида натрия (4,27 мл), метанола (20 мл) и воды (5 мл) перемешивают при температуре окружающей среды в течение 4 часов. Смесь выпаривают и остаток распределяют между метиленхлоридом и водой. Водную фазу подкисляют добавлением 1N водного раствора соляной кислоты и экстрагируют метиленхлоридом. Органический экстракт выпаривают. Получают 3-циклопентилоксибензойную кислоту (0,864 г). Спектр ЯМР: (ДМСОd6) 1,51-1,75(м, 6Н), 1,8-2,0(м, 2Н), 4,8-4,86(м, 1Н), 7,12(д, 1Н), 7,34-7,49(м, 2Н), 7,46-7,49(м, 1Н), 12,89(с, 1Н).
e) Продукт реакции очищают хроматографией на колонке с обращенной фазой с двуокисью кремния, используя сначала воду и затем смеси метанола и воды со снижающейся полярностью в качестве элюента. Очищенное соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,48-1,62(м, 2Н), 1,64-1,78(м, 4Н), 1,8-1,95(м, 2Н), 2,04(с, 3Н), 2,23(с, 3Н), 2,45-2,5(м, 4Н), 3,2-3,35(м, 4Н), 3,81(с, 3Н), 7,06(д, 1Н), 7,39(д, 1Н), 7,48(д, 2Н), 7,57-7,63(м, 3Н), 7,77-7,82(м, 2Н), 8,07(с, 1Н), 10,17 (с, 1Н). Масс спектр: M+H+ 568.
3-Циклопентилокси-4-метоксибензойная кислота, используемая в качестве исходного материала, коммерчески доступна от Maybridge International, Tintagel, Cornwall, United Kingdom, или может быть получена из этил-3-гидрокси-4-метоксибензоата по методике, аналогичной методике примечания d) выше, используемой для получения 3-циклопентилоксибензойной кислоты.
f) Продукт реакции очищают хроматографией на колонке с обращенной фазой с двуокисью кремния, используя сначала воду и затем смеси метанола и воды со снижающейся полярностью в качестве элюента. Очищенное соединение имеет следующие характеристики. Спектр ЯМР: (ДMCOd6) 2,04(с, 3Н), 2,05 (с, 3Н), 2,22(с, 3Н), 2,45-2,5(м, 4Н), 3,2-3,35(м, 4Н), 7,38-7,47(м, 3Н), 7,58-7,62(м, 3Н), 7,75-7,81(м, 3Н), 8,05-8,08(м, 2Н), 10,39 (с, 1Н). Масс спектр: М+Н+ 511.
g) Продукт реакции очищают хроматографией на колонке с обращенной фазой с двуокисью кремния, используя сначала воду и затем смеси метанола и воды со снижающейся полярностью в качестве элюента. Очищенное соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,02(с, 3Н), 2,22(с, 3Н), 2,43-2,5(м, 4Н), 2,98(с, 3Н), 3,21-3,3(м, 4Н), 7,4-7,48(м, 2Н), 7,52-7,62(м, 4Н), 7,78-7,82(м, 2Н), 7,88(д, 1Н), 7,92(с, 1Н), 8,06(с, 1Н), 10,55(с, 1Н). Масс спектр: M+H+ 561.
3-(N-Метилметансульфонамидо)бензойную кислоту, используемую в качестве исходного соединения, получают следующим образом.
Метансульфонилхлорид (12,1 мл) добавляют к перемешиваемой смеси этил-3-аминобензоата (24,55 г), пиридина (14,42 мл) и метиленхлорида (300 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение 18 часов. Смесь промывают последовательно водой, 1N водным раствором соляной кислоты и водой. Органическую фазу сушат (MgSO4) и выпаривают. Получают этил-3-метансульфонамидобензоат (35,2 г). Спектр ЯМР: (ДМСОd6) 1,3 (т, 3Н), 3,0(с, 3Н), 4,3(м, 2Н), 7,46(м, 2Н), 7,66(м, 1Н), 7,8(м, 1Н), 9,95(с, 1Н). Масс спектр: М-Н- 242.
Метилйодид (4,23 мл) добавляют к перемешиваемой смеси этил-3-метансульфонамидобензоата (15 г), карбоната цезия (22,12 г) и ДМФ (60 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение 18 часов. Смесь распределяют между этилацетатом и водой. Органическую фазу промывают водой, сушат (MgSO4) и выпаривают. Получают этил-3-(N-метилметансульфонамидо)бензоат (14,87 г). Спектр ЯМР: (ДМСОd6) 1,32(т, 3Н), 2,95(с, 3Н), 3,26(с, 3Н), 4,32(м, 2Н), 7,55(т, 1Н), 7,68(м, 1Н), 7,87(м, 1Н), 7,92(м, 1Н). Масс спектр: M+H+ 258.
Смесь полученного соединения, 10N водного раствора гидроксида натрия (11,5 мл), этанола (150 мл) и воды (30 мл) перемешивают при температуре окружающей среды в течение 4 часов. Смесь выпаривают и к остатку добавляют 1N водный раствор соляной кислоты (125 мл), что приводит к образованию белого осадка, который выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 60°С. Получают 3-(N-метилметансульфонамидо)бензойную кислоту (9,72 г). Спектр ЯМР: (ДМСОd6) 2,94(с, 3Н), 3,26(с, 3Н), 7,52(т, 1Н), 7,65(м, 1Н), 7,84(м, 1Н), 7,91(м, 1Н). Масс спектр: М-Н- 228.
h) Продукт реакции очищают хроматографией на колонке с обращенной фазой с двуокисью кремния, используя сначала воду и затем смеси метанола и воды со снижающейся полярностью в качестве элюента. Очищенное соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,04(с, 3Н), 2,23(с, 3Н), 2,4-2,5(м, 6Н), 3,25-3,29(м, 4Н), 3,53(т, 2Н), 3,81(т, 2Н), 7,39-7,58(м, 4Н), 7,61(с, 1Н), 7,67-7,68(м, 2Н), 7,78-7,79(м, 2Н), 8,07 (с, 1Н), 10,43(с, 1Н). Масс спектр: M+H+ 573.
3-(1,1-Диоксидоизотиазолидин-2-ил)бензойную кислоту, используемую в качестве исходного соединения, получают следующим образом.
3-Хлорпропансульфонилхлорид (5,1 г) по каплям добавляют к перемешиваемой смеси этил-3-аминобензоата (4,5 г), пиридина (2,423 мл), 4-диметиламинопиридина (0,03 г) и метиленхлорида (100 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение 48 часов. Смесь промывают 2N водным раствором соляной кислоты и органическую фазу сушат (MgSO4) и выпаривают. Получают этил-3-(3-хлорпропансульфонамидо)бензоат (8,19 г). Спектр ЯМР: (ДМСОd6) 1,29 (т, 3Н), 2,19(м, 2Н), 3,24(т, 2Н), 3,72(т, 2Н), 4,31(м, 2Н), 7,47(м, 2Н), 7,68(м, 1Н), 7,83(м, 1Н), 10,12 (с, 1Н). Масс спектр: (М-Н)- 303 и 305.
Смесь полученного соединения, триэтиламина (7,3 мл) и этанола (120 мл) перемешивают и нагревают при температуре кипения с обратным холодильником в течение 6 часов. Смесь выпаривают. Остаток распределяют между метиленхлоридом и водой. Органическую фазу сушат (MgSO4) и выпаривают. Получают этил-3-(1,1-диоксидоизотиазолидин-2-ил)бензоат (6,99 г). Спектр ЯМР: (ДМСОd6) 1,3(т, 3Н), 2,42(м, 2Н), 3,53(т, 2Н), 3,78(т, 2Н), 4,32(м, 2Н), 7,43(м, 1Н), 7,52(т, 1Н), 7,66(м, 1Н), 7,78(м, 1Н). Масс спектр: M+H+ 269.
Смесь части (6,87 г) полученного соединения, 10N водного раствора гидроксида натрия (5,1 мл), этанола (80 мл) и воды (14 мл) перемешивают при температуре окружающей среды в течение 18 часов. Смесь выпаривают и к остатку добавляют 1N водный раствор соляной кислоты (160 мл), что дает образование белого осадка, который выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 60°С. Получают 3-(1,1-диоксидоизотиазолидин-2-ил)бензойную кислоту (5,45 г). Спектр ЯМР: (ДМСОd6) 2,43(м, 2Н), 3,5 (т, 2Н), 3,78(т, 2Н), 7,39(м, 1Н), 7,48(т, 1Н), 7,66(м, 1Н), 7,78(м, 1Н), 13,06(с, 1Н). Масс спектр: М-Н- 239.
i) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,04(с, 3Н), 2,48(с, 3Н), 2,78-2,88(м, 4Н), 3,15-3,19(м, 4Н), 3,28-3,42(м, 4Н), 3,73-3,77(м, 4Н), 7,1-7,18(м, 1Н), 7,35-7,42(м, 4Н), 7,51(с, 1Н), 7,65(с, 2Н), 7, 77-7, 8 (м, 2Н), 8,1 (с, 1Н), 10, 29 (с, 1Н). Масс спектр: М+Н+ 539.
3-Морфолинобензойную кислоту, используемую в качестве исходного соединения, получают следующим образом.
Смесь этил-3-бромбензоата (1,92 мл), морфолина (1,25 мл), 2,2'-бис(дифенилфосфино)-1,1'-бинафтила (0,336 г), трет-бутоксида натрия (1,615 г) и трис(дибензилиденацетон)-дипалладия (0) (0,33 г) и толуола (25 мл) перемешивают и нагревают при температуре 90°С в атмосфере аргона в течение 18 часов. Реакицонную смесь охлаждают до температуры окружающей среды и экстрагируют 1N водной соляной кислотой. Водную фазу подщелачивают концентрированным раствором гидроксида натрия и экстрагируют этилацетатом. Органическую фазу сушат (MgSO4) и выпаривают. Остаточное масло очищают хроматографией на колонке с силикагелем, используя 47:3 смесь метиленхлорида и метанола в качестве элюента. Получают N-(3-морфолинобензоил)морфолин (0,45 г).
Смесь полученного соединения, 5М раствора гидроксида натрия (2,5 мл) и бутанола (2 мл) перемешивают и нагревают при температуре 115°С в течение 18 часов. Смесь выпаривают и остаток подкисляют добавлением 1N водного раствора соляной кислоты (12,5 мл). Полученный осадок выделяют, промывают водой и сушат с получением 3-морфолинобензойной кислоты (0,15 г).
Спектр ЯМР: (ДМСОd6) 3,1(т, 4Н), 3,73(т, 4Н), 7,19(д, 1Н), 7,32(д, 1Н), 7,38(т, 1Н), 7,42(с, 1Н).
j) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,26(с, 3Н), 2,47-2,53(м, 4Н), 3,2-3,3(м, 4Н), 7,42-7,48(м, 2Н), 7,62(с, 2Н), 7,76-7,8(м, 2Н), 7,93-8,07(м, 4Н), 7,93-8,07(м, 4Н), 10,64(с, 1H). Масс спектр: М+H+ 540.
k) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,97(с, 3Н), 2,18-2,28(м, 2Н), 2,38 (с, 3Н), 2,62-2,78(м, 4Н), 3,2-3,41(м, 4Н), 3,7-3,92(м, 4Н), 5,04-5,14(м, 1H), 7,14(д, 1Н), 7,39-7,57(м, 5Н), 7,64(с, 2Н), 7,77-7,82(м, 2Н), 8,08(с, 1H), 10,35(с, 1H). Масс спектр: М+Н+ 540.
3-Тетрагидрофуранилоксибензойную кислоту, используемую в качестве исходного соединения, получают по методике, аналогичной методике примечания d), описанной выше, за исключением того, что вместо циклопентанола используют 3-гидрокситетра-гидрофуран.
l) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05 (с, 3Н), 2,25 (с, 3Н), 2,5(м, 4Н), 3,28(м, 4Н), 3,88(с, 3Н), 7,06(т, 1Н), 7,18(д, 1Н), 7,4(д, 1Н), 7,5(м, 2Н), 7,62(м, 3Н), 7,74-7,81(м, 2Н), 8,1(с, 1Н), 10,29(с, 1Н). Масс спектр: M+H+ 484.
m) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,34(т, 3Н), 2,05(с, 3Н), 2,25(с, 3Н), 2,5(м, 4Н), 3,25(м, 4Н), 4,08(кв, 2Н), 7,14(м, 1Н), 7,39-7,55(м, 5Н), 7,64(м, 2Н), 7,8(м, 2Н), 8,1(с, 1Н), 10,36(с, 1Н). Масс спектр: M+H+ 498.
n) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05 (с, 3Н), 2,25 (с, 3Н), 2,5-3,3(м, 8Н), 6,85(м, 1Н), 7,40-7,55(м, 3Н), 7,65(м, 3Н), 7,8(м, 3Н), 7,98(м, 1Н), 8,1(с, 1Н), 10,55(с, 1Н). Масс спектр: M+H+ 570.
о) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,86-1,98(м, 2Н), 2,04(с, 3Н), 2,25(с, 3Н), 2,42-2,5(м, 2Н), 2,62-2,66(м, 2Н), 3,15-3,19(м, 4Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 3,72-3,76(м, 4Н), 7,1-7,18(м, 1Н), 7,24(с, 1Н), 7,34-7,44(м, 5Н), 7,58(д, 1Н), 7,76-7,82(м, 2Н), 7,96(с, 1Н), 10,29(с, 1Н). Масс спектр: М+Н+ 553.
р) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,86-1,98(м, 2Н), 2,04(с, 3Н), 2,25(с, 3Н), 2,42-2,5(м, 2Н), 2,62-2,66(м, 2Н), 3,19-3,23(м, 4Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 3,71-3,75(м, 4Н), 6,98(д, 1Н), 7,12(д, 1Н), 7,24(с, 1Н), 7,28(с, 1Н), 7,32-7,44(м, 2Н), 7,58(д, 1Н), 7,74-7,82(м, 2Н), 7,96(с, 1Н), 10,32(с, 1Н). Масс спектр: M+H+ 571.
3-Фтор-5-морфолинобензойную кислоту, используемую в качестве исходного соединения, получают следующим образом.
Смесь этил-3-фтор-5-морфолинобензоата (Tetrahedron, 1999, 55, 13285-13300; 6,7 г), 10 М раствора гидроксида натрия (13,6 мл), воды (13,6 мл) и этанола (67 мл) перемешивают при температуре окружающей среды в течение 20 часов. Смесь концентрируют выпариванием и остаток подкисляют добавлением концентрированной соляной кислоты. Полученный осадок выделяют, промывают водой и сушат с получением 3-фтор-5-морфолинобензойной кислоты (5,7 г). Спектр ЯМР: (ДМСОd6) 3,16(т, 4Н), 3,71(т, 4Н), 7,01(м, 2Н), 7,27(с, 1Н).
q) Соединение имеет следующие характеристики Спектр ЯМР: (ДМСОd6) 1,86-1,98(м, 2Н), 2,05(с, 3Н), 2,25(с, 3Н), 2,42-2,5(м, 2Н), 2,62-2,66(м, 2Н), 3,24-3,34(м, 4Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 3,73-3,77(м, 4Н), 7,24(с, 1Н), 7,32-7,43(м, 3Н), 7,58(д, 1Н), 7,63(с, 1Н), 7,7(с, 1Н), 7,74(с, 1Н), 7,8(д, 1Н), 7,97(с, 1Н), 10,45(с, 1Н); Масс спектр: M+H+ 621.
r) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,86-1,98(м, 2Н), 2,05(с, 3Н), 2,25(с, 3Н), 2,42-2,5(м, 2Н), 2,62-2,66(м, 2Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 6,61(с, 1Н), 7,04(с, 1Н), 7,24(с, 1Н), 7,38(д, 1Н), 7,42(д, 1Н), 7,52-7,6(м, 2Н), 7,78-7,92(м, 5Н), 7,98(с, 1Н), 8,24(с, 1Н), 10,49(с, 1Н). Масс спектр: M+H+ 534.
s) Остаток реакционной смеси очищают хроматографией на ионообменной колонке SCX isolute, используя сначала метанол и затем 99:1 смесь метанола и насыщенного водного раствора гидроксида аммония в качестве элюента. Полученное соединение растворяют в ацетоне и осаждают добавлением изогексана. Полученное соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,25(с, 3Н), 3,3-3,4(м, 4Н), 3,7-3,8(м, 4Н), 7,1-7,2(м, 1Н), 7,3-7,5(м, 7Н), 7,75-7,85(м, 3Н), 8,25(с, 1Н), 10,3(с, 1Н). Масс спектр: М+Н+ 539.
3-(5-Амино-2-метилфенил)-8-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он, используемый в качестве исходного соединения, получают следующим образом.
Оксалилхлорид (8,5 мл) по каплям добавляют к перемешиваемому раствору 3-хлор-2-нитробензойной кислоты (15,1 г) в смеси метиленхлорида (200 мл) и ДМФ (несколько капель), охлажденому до температуры 0°С. Смесь нагревают при температуре окружающей среды и перемешивают в течение еще 16 часов. Растворитель выпаривают. Остаток растворяют в метиленхлориде (300 мл) и по каплям добавляют к перемешиваемой смеси 2-метил-5-нитроанилина (10,6 г), триэтиламина (27,2 мл) и метиленхлорида (300 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Осадок выделяют, промывают последовательно насыщенным водным раствором бикарбоната натрия и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают N-(2-метил-5-нитрофенил)-3-хлор-2-нитробензамид (14,2 г). Спектр ЯМР: (ДМСОd6) 2,37 (с, 3Н), 7,57(д, 1Н), 7,8-7,85(м, 1Н), 7,95-8,05(м, 3Н), 8,35(м, 1Н). Масс спектр: М+Н+ 335.
Смесь полученного соединения и N-метилпиперазина (24,5 мл) перемешивают и нагревают при температуре 100°С в течение 16 часов. Реакционную смесь охлаждают до температуры окружающей среды и выливают в воду. Полученный осадок выделяют, промывают водой и сушат в вакууме при температуре 40°С. Получают N-(2-метил-5-нитрофенил)-3-(4-метилпиперазин-1-ил)-2-нитробензамид (11,8 г). Спектр ЯМР: (ДМСОd6) 2,2 (с, 3Н), 2,35-2,45(м, 7Н), 2,9-3,0(м, 4Н), 7,5-7,7(м, 4Н), 8,0-8,05(м, 1Н), 8,3(с, 1Н). Масс спектр: M+H+ 400.
Смесь полученного соединения, катализатора 10% палладия на углероде (1,2 г) и метанола (600 мл) перемешивают в атмосфере водорода до тех пор, пока не прекратится поглощение водорода. Катализатор отфильтровывают и фильтрат выпаривют. Полученное соединение очищают хроматографией на колонке с двуокисью кремния, используя 4:1 смесь метиленхлорида и метанола в качестве элюента. Получают N-(5-амино-2-метилфенил)-2-амино-3-(4-метилпиперазин-1-ил)бензамид (7,36 г). Спектр ЯМР: (ДМСОd6) 2,0(с, 3Н), 2,2(с, 3Н), 2,75-2,85(м, 4Н), 4,85(с, 2Н), 6,0(с, 2Н), 6,35-6,4(м, 1Н), 6,57(м, 2Н), 6,85(д, 1Н), 7,07(д, 1Н), 7,45(д, 1Н), 9,35(с, 1Н). Масс спектр: М+Н+ 340.
Смесь части (4 г) полученного соединения, триэтилортоформиата (3,92 мг), ледяной уксусной кислоты (0,34 мл) и этанола (72 мл) перемешивают и нагревают при температуре 80°С в течение 2 дней. Реакционную смесь охлаждают и выпаривают. Остаток растворяют в воде, подщелачивают добавлением бикарбоната натрия и экстрагируют метиленхлоридом. Органический экстракт выпаривают и остаток очищают хроматографией на колонке с двуокисью кремния, используя 20:1 смесь метиленхлорида и метанола в качестве элюента. Получают 3-(5-амино-2-метилфенил)-8-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он (4,1 г). Спектр ЯМР: (ДМСОd6) 1,85(с, 3Н), 2,2 (с, 3Н), 2,5-2,6(м, 4Н), 5,15(с, 2Н), 6,5(д, 1Н), 6,6-6,65(м, 1Н), 7,0(д, 1Н), 7,3(д, 1Н), 7,42(т, 1Н), 7,75(д, 1Н), 8,15(с, 1Н). Масс спектр: M+H+ 350.
t) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,25(с, 3Н), 3,2-3,25(м, 4Н), 3,7-3,8(м, 4Н), 6,95-7,0(м, 1Н), 7,1-7,15(м, 1Н), 7,3-7,4(м, 2Н), 7,4-7,5(м, 2Н), 7,75-7,8(м, 3Н), 8,25(с, 1Н), 10,33(с, 1Н). Масс спектр: М+Н+ 557.
u) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,25(с, 3Н), 3,7-3,8(м, 4Н), 7,3-7,5(м, 4Н), 7,6-7,85(м, 5Н), 8,25(с, 1Н), 10,48(с, 1Н). Масс спектр: М+Н+ 607.
v) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,25(с, 3Н), 6,6-6,65(м, 1Н), 7,05(м, 1Н), 7,3-7,35(м, 1Н), 7,4-7,5(м, 2Н), 7,5-7,6(м, 1Н), 7,75-7,95(м, 6Н), 8,25-8,3(м, 2Н), 10,5(с, 1Н). Масс спектр: M+H+ 520.
w) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,25(с, 3Н), 7,3-7,4(м, 3Н), 7,4-7,5(м, 2Н), 7,55-7,65(м, 1Н), 7,75-7,95(м, 7Н), 8,18(с, 1Н), 8,3 (с, 1Н), 10,48(с, 1Н). Масс спектр: M+H+ 548.
Пример 12
По методике примера 1 или примера 2 подходящий 2-аминобензамид подвергают взаимодействию с триэтилортоформиатом или триэтилортоацетатом с получением соединеий, представленных в таблице VI.
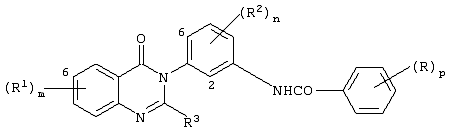
| Таблица VI |
| № |
(R1)m |
(R2)n |
R3 |
(R)p |
Прим. |
| 1 |
8-морфолино |
4-метил |
Н |
3-(4-метилпиперазин-1- |
а |
|
|
|
|
ил)метил |
|
| 2 |
8-морфолино |
4-метил |
метил |
3-(4-метилпиперазин-1 - |
b |
|
|
|
|
ил)метил |
|
Примечания
а) Реакционную смесь нагревают при температуре 70°С в течение 48 часов. Соединение имеет следующие характеристики.
Спектр ЯМР: (ДМСОd6) 2,1(с, 3Н), 2,2-2,45(м, 11Н), 3,5(с, 2Н), 3,7-3,8(м, 4Н), 7,3-7,35(м, 2Н), 7,4-7,55(м, 4Н), 7,55-7,6(м, 1Н), 7,8(д, 1Н), 7,8-7,9(м, 2Н), 8,3(с, 1Н), 10,0(с, 1Н). Масс спектр: М+Н+ 553.
N-{3-[3-(4-Метилпиперазин-1-илметил)бензамидо]-4-метилфенил)-2-амино-3-морфолинобензамид, используемый в качестве исходного соединения, получают следующим образом.
3-Хлорметилбензоилхлорид (24,8 мл) добавляют к перемешиваемой смеси 2-метил-5-нитроанилина (26,6 г), триэтиламина (49 мл) и метиленхлорида (800 мл) и смесь перемешивают при температуре окружающей среды в течение 16 часов. Осадок выделяют, промывают 1N водным раствором соляной кислоты и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают 3-хлорметил-N-(2-метил-5-нитрофенил)бензамид (43,5 г). Спектр ЯМР: (ДМСОd6) 2,38(с, 3Н), 2,85(с, 2Н), 7,53-7,58(м, 2Н), 7,67(д, 1Н), 7,95(д, 1Н), 8,01-8,04(м, 2Н), 8,32(с, 1Н), 10,19(с, 1Н). Масс спектр: М+Н+ 305.
1-Метилпиперазин (8,03 мл) добавляют к перемешиваемой смеси части (20 г) полученного соединения, карбоната калия (18,2 г) и ацетона (750 мл) и смесь нагревают при температуре 54°С и перемешивают в течение 16 часов. Полученный раствор выпаривают и остаток растворяют в метиленхлориде. Органический раствор промывают водой и выпаривают. Получают N-(2-метил-5-нитрофенил)-3-(4-метилпиперазин-1-илметил)бензамид (26,4 г).
Спектр ЯМР: (ДМСОd6) 2,06(с, 3Н), 2,12(с, 3Н), 2,31-2,37(м, 8Н), 3,52(с, 2Н), 7,48-7,57(м, 3Н), 7,87(д, 2Н), 8,01(м, 1Н), 8,33(с, 1Н). Масс спектр: М+Н+ 369.
Железный порошок добавляют к перемешиваемой смеси части (18,0 г) полученного соединения, этанола (500 мл), воды (50 мл) и уксусной кислоты (10 мл). Полученную смесь перемешивают и нагревают при температуре кипения с обратным холодильником в течение 5 часов. Добавляют воду (50 мл) и смесь подщелачивают добавлением карбоната натрия. Смесь фильтруют и фильтрат выпаривают досуха. Остаток растирают под водой и полученное твердое вещество выделяют и сушат в вакууме при температуре 40°С. Получают N-(5-амино-2-метилфенил)-3-(4-метипиперазин-1-илметил)бензамид (11,1 г). Спектр ЯМР: (ДМСОd6) 2,03(с, 3Н), 2,13(с, 3Н), 2,24-2,4(м, 8Н), 3,5(с, 2Н), 4,86(с, 2Н), 6,35(д, 1Н), 6,57(с, 1Н), 6,86(д, 1Н), 7,40-7,48(м, 2Н), 7,78-7,83(м, 2Н), 9,57(с, 1Н). Масс спектр: М+Н+ 339.
Оксалилхлорид (0,83 мл) добавляют к смеси 3-хлор-2-нитробензойной кислоты (1,45 г), метиленхлорида (30 мл) и нескольких капель ДМФ, охлажденной до температуры 0°С. Реакционную смесь перемешивают при температуре окружающей среды в течение 4 часов. Смесь выпаривают. Остаток растворяют в метиленхлориде (10 мл) и добавляют часть (5 мл) раствора к смеси N-(5-амино-2-метилфенил)-3-(4-метипиперазин-1-илметил)бензамида (1,01 г), триэтиламина (1 мл) и метиленхлорида (20 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Смесь выпаривают и остаток разделяют между метиленхлоридом и насыщенным водным раствором бикарбоната натрия. Органическую фазу сушат (MgSO4) и выпаривают. Получают N-{3-[3-(4-метилпиперазин-1-илметил) бензамидо] -4-метилфенил}-3-хлор-2-нитробензамид (1,69 г). Спектр ЯМР: (ДМСОd6) 2,15(с, 3Н), 2,2(с, 3Н), 2,2-2,4(м, 8Н), 3,5(с, 2Н), 7,2-7,3(м, 1Н), 7,4-7,5(м, 3Н), 7,7-7,95(м, 6Н), 9,9(с, 1Н), 10,78(с, 1Н). Масс спектр: М+Н+ 522.
Смесь полученного соединения и морфолина (2,71 мл) перемешивают и нагревают при температуре 105°С в течение 16 часов. Смесь охлаждают до температуры окружающей среды и выливают в воду. Осадок выделяют, промывают водой и распределяют между насыщенным водным раствором бикарбоната натрия и метиленхлоридом. Органическую фазу сушат (MgSO4) и выпаривают. Получают N-{3-[3-(4-метилпиперазин-1-илметил)бензамидо]-4-метилфенил}-2-нитро-3-морфолинобензамид (1,47 г). Спектр ЯМР: (ДМСОd6) 2,15(с, 3Н), 2,2(с, 3Н), 2,2-2,45(м, 8Н), 2,85-2,95(м, 4Н), 3,5(с, 2Н), 3,6-3,7(м, 4Н), 7,2(д, 1Н), 7,4-7,5(м, 3Н), 7,5-7,6(м, 1Н), 7,6-7,7(м, 2Н), 7,75(с, 1Н), 7,8-7,9(м, 2Н), 9,9(с, 1Н), 10,62(с, 1Н). Масс спектр: М+Н+ 573.
Смесь полученного соединения, железного порошка (1,435 г), этанола (25,7 мл), воды (2,57 мл) и ледяной уксусной кислоты (0,52 мл) перемешивают и нагревают при температуре 95°С в течение 8 часов. Полученную смесь охлаждают до температуры окружающей среды и подщелачивают до рН 9 добавлением бикарбоната натрия. Смесь фильтруют и фильтрат выпаривают. Остаток распределяют между этилацетатом и насыщенным водным раствором бикарбоната натрия. Органическую фазу сушат (MgSO4) и выпаривают. Полученный материал растворяют в этилацетате и осаждают добавлением изогексана. Твердое вещество выделяют. Получают N-{3-[3-(4-метилпиперазин-1-илметил)бензамидо]-4-метилфенил}-2-амино-3-морфолинобензамид (0,95 г). Спектр ЯМР: (ДМСОd6) 2,1(с, 3Н), 2,2(с, 3Н), 2,2-2,4(м, 8Н), 2,75-2,8(м, 4Н), 3,5(с, 2Н), 3,7-3,8(м, 4Н), 6,05(с, 2Н), 6,6(т, 1Н), 7,1(д, 1Н), 7,2(д, 1Н), 7,4-7,5(М, 4Н), 7,8(д, 1Н), 7,8-7,9(м, 2Н), 9,85(с, 1Н), 9,95(с, 1Н). Масс спектр: M+H+ 543.
b) Реакционную смесь нагревают до 70° в течение 48 часов. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,1(с, 3Н), 2,2(с, 3Н), 2,2-2,4(м, ПН), 3,5(с, 2Н), 3,7-3,85(м, 4Н), 7,2-7,3(м, 2Н), 7,3-7,5(м, 5Н), 7,65(д, 1Н), 7,8-7,9(м, 2Н), 10,0(с, 1Н). Масс спектр: M+H+ 567.
Пример 13
Используя методику, аналогичную методике примера 1 или примера 2, подходящий 2-аминобензамид подвергают взаимодействию с триэтилортоформиатом или триэтилортоацетатом с получением соединений, описанных в таблице VII. В каждом случае продукт реакции очищают хроматографией на ионообменной колонке isolute SCX, используя сначала метанол, а затем 99:1 смесь этанола и насыщенного водного раствора гидроксида аммония в качестве элюента.
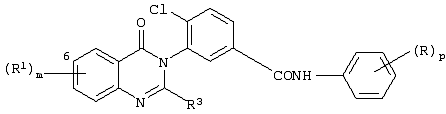
Таблица VII
| № |
(R1)m |
R3 |
(R)p |
Прим. |
| 1 |
6-(4-метилпиперазин-1-ил) |
метил |
3-фтор-5-морфолино |
а |
| 2 |
6-(4-метилпиперазин-1-ил) |
Н |
3-фтор-5-морфолино |
b |
| 3 |
6-[N-(3-диметиламинопропил)-N-метиламино] |
метил |
3-фтор-5-морфолино |
с |
| 4 |
6-[N-(3-диметиламинопропил)-N-метиламино] |
Н |
3-фтор-5-морфолино |
d |
| 5 |
6-(3- диметиламинопропиламино) |
метил |
3-фтор-5-морфолино |
е |
| 6 |
6-(3-диметиламинопропиламино) |
Н |
3-фтор-5-морфолино |
f |
| 7 |
6-[N-(3-метиламинопропил)-N-метиламино] |
метил |
3-фтор-5-морфолино |
g |
| 8 |
6-[N-(3-метиламинопропил)-N-метиламино] |
Н |
3-фтор-5-морфолино |
h |
Примечания
а) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 591.
3-[2-Амино-5-(4-метилпиперазин-1-ил)бензамидо]-4-хлор-N-(3-фтор-5-морфолинофенил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Смесь 3,5-дифторнитробензола (31,1 г) и морфолина (85,2 г) перемешивают и нагревают при температуре 100°С в течение 66 часов. Смесь выпаривают и остаток очищают хроматографией на колонке с силикагелем, используя 4:1 смесь изогексана и этилацетата в качестве элюента. Получают 3-фтор-5-морфолинонитробензол (33,3 г). Спектр ЯМР: (ДМСОd6) 3,2-3,3(м, 4Н), 3,6-3,8(м, 4Н), 7,25(м, 1Н), 7,37(м, 1Н), 7,5(м, 1Н).
Смесь полученного соединения, 10% палладия на углероде (3,3 г) и этанола (1400 мл) перемешивают при атмосферном давлении водорода в течение 16 часов. Смесь фильтруют и фильтрат выпаривают с получением 3-фтор-5-морфолиноанилина (27,5 г).
Спектр ЯМР: (ДМСОd6) 2,9-3,05(м, 4Н), 3,6-3,7(м, 4Н), 5,15(с, 2Н), 5,75-5,9(м, 3Н).
Раствор 4-хлор-3-нитробензоилхлорида (41,2 г) в метиленхлориде (120 мл) добавляют к смеси 3-фтор-5-морфолиноанилина (27 г), триэтиламина (52,6 мл) и метиленхлорида (600 мл), охлажденной на ледяной бане. Полученную смесь перемешивают при температуре окружающей среды в течение 16 часов. Смесь выпаривают. Добавляют метиленхлорид и насыщенный водный раствор бикарбоната натрия и полученный осадок отделяют, промывают диэтиловым эфиром и сушат в вакууме. Получают 4-хлор-3-нитро-N-(3-фтор-5-морфолинофенил)бензамид (36,1 г). Спектр ЯМР (ДМСОd6) 3,05-3,15(м, 4Н), 3,7-3,75(м, 4Н), 6,5-6,6(м, 1Н), 7,1-7,2(м, 2Н), 7,95(д, 1Н), 8,2-8,3(м, 1Н), 8,6(с, 1Н).
Смесь полученного соединения, порошка железа (50,6 г), ледяной уксусной кислоты (19 мл), воды (95 мл) и этанола (600 мл) перемешивают и нагревают при температуре кипения с обратным холодильником в течение 6 часов. Смесь охлаждают до температуры окружающей среды и добавляют воду. Смесь осторожно подщелачивают до рН 9 добавлением насыщенного водного раствора бикарбоната натрия и экстрагируют этилацетатом. Органическую фазу сушат над сульфатом магния и выпаривают с получением 3-амино-4-хлор-N-(3-фтор-5-морфолинофенил)бензамида (24,3 г). Спектр ЯМР: (ДМСОd6) 3,0-3,1(м, 4Н), 3,7-3,75 (м, 4Н), 5,6 (с, 1Н), 6,45-6,55(м, 1Н), 7,0-7,2(м, 3Н), 7,3-7,35(м, 2Н), 10,09(ш с, 1Н). Масс спектр: М+Н+ 350.
Оксалилхлорид (1,05 мл) по каплям добавляют к перемешиваемой смеси 5-хлор-2-нитробензойной кислоты (2,08 г), метиленхлорида (100 мл) и ДМФ (несколько капель), охлажденной до температуры 0°С. Смесь нагревают при температуре окружающей среды и перемешивают в течение 4 часов. Смесь выпаривают и остаток растворяют в метиленхлориде (10 мл) и по каплям добавляют к перемешиваемой смеси 3-амино-4-хлор-N-(3-фтор-5-морфолинофенил)бензамида (3,0 г) и пиридина (40 мл). Полученную смесь нагревают при температуре 80°С в течение 16 часов. Растворитель выпаривают и остаток растворяют в метиленхлориде (50 мл) и воде (50 мл) и перемешивают в течение 1 часа. Полученное твердое вещество фильтруют, промывают водой и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают 4-хлор-3-(5-хлор-2-нитробензамидо)-N-(3-фтор-5-морфолинофенил)бензамид (1,07 г). Спектр ЯМР: (ДМСОd6) 3,09-3,14(м, 4Н), 3,69-3,74(м, 4Н), 6,58(д, 1Н), 7,15-7,2(м, 2Н), 7,71(д, 1Н), 7,82-7,92(м, 3Н), 8,2(д, 1Н), 8,29(с, 1Н), 10,37(с, 1Н), 10,61(с, 1Н). Масс спектр: M+H+ 533 и 535.
Часть (0,8 г) полученного соединения растворяют в 1-метилпиперазине (3 мл) и смесь перемешивают и нагревают при температуре 100°С в течение 16 часов. Смесь охлаждают и выливают в воду. Полученное твердое вещество выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают 4-хлор-N-(3-фтор-5-морфолинофенил)-3-[5-(4-метилпиперазин-1-ил)- 2-нитробензамидо]бензамид (0,803 г). Спектр ЯМР: (ДМСОd6) 2,21(с, 3Н), 2,4-2,45(м, 4Н), 3,08-3,13(м, 4Н), 3,46-3,5(м, 4Н), 3,69-3,74(м, 4Н), 6,58(д, 1Н), 6,84(с, 1Н), 7,0-7,2(м, 4Н), 7,68(д, 1Н), 7,80(д, 1Н), 8,04(д, 1Н), 8,36 (с, 1Н). Масс спектр: M+H+ 597.
Порошок железа (0,726 г) добавляют к перемешиваемой суспензии 4-хлор-N-(3-фтор-5-морфолинофенил)-3-[5-(4-метилпиперазин-1-ил)-2-нитробензамидо]бензамида (0,76 г), воды (2 мл), уксусной кислоты (0,5 мл) и этанола (15 мл) и полученную смесь перемешивают и нагревают при температуре кипения с обратным холодильником в течение 1 часа. Смесь охлаждают до температуры окружающей среды. Добавляют воду (80 мл) и смесь подщелачивают добавлением карбоната натрия. Полученную смесь фильтруют через диатомовую землю и отделенные твердые вещества промывают последовательно метиленхлоридом и метанолом. Объединенные фильтраты выпаривают и остаток растирают под этилацетатом. Смесь фильтруют и фильтрат выпаривают с получением 3-[2-амино-5-(4-метилпиперазин-1-ил)бензамидо]-4-хлор-N-(3-фтор-5-морфолинофенил)бензамида (0,385 г). Масс спектр: М+Н+ 567.
b) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 577.
c) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,6-1,7(м, 2Н), 2,09 (с, 3Н), 2,11 (с, 6Н), 2,21(т, 2Н), 2,96(с, 3Н), 3,06-3,14(м, 4Н), 3,37-3,43(м, 2Н), 3,69-3,8(м, 4Н), 6,56(д, 1Н), 7,09(с, 1Н), 7,15-7,19(м, 2Н), 7,32-7,38(м, 1Н), 7,53(д, 1Н), 7,9(д, 1Н), 8,09(д, 1Н), 8,16 (с, 1Н), 10,31(с, 1Н). Масс спектр: М+Н+ 607.
3-{2-Амино-5-[N-(3-диметиламинопропил)-N-метиламино]бензамидо}-4-хлор-N-(3-фтор-5-морфолинофенил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Смесь 4-хлор-3-(5-хлор-2-нитробензамидо)-N-(3-фтор-5-морфолинофенил)бензамида (0,8 г) и N-(3-диметиламинопропил)-N-метиламина (3 мл) перемешивают и нагревают при температуре 100°С в течение 16 часов. Смесь охлаждают и выливают в воду. Полученное твердое вещество выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают 4-хлор-3-{5-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамидо}-N-(3-фтор-5-морфолинофенил)бензамид. Спектр ЯМР: (ДМСОd6) 1,62-1,74(м, 2Н), 2,12(с, 6Н), 2,21(т, 2Н), 3,08(с, 3Н), 3,1-3,13(м, 4Н), 3,52(т, 2Н), 3,71-3,74(м, 4Н), 6,68(д, 1Н), 6,78(с, 1Н), 6,84(д, 1Н), 7,16-7,20(м, 2Н), 7,68(д, 1Н), 7,82(д, 1Н), 8,04(д, 1Н), 8,31(с, 1Н). Масс спектр: M+H+ 613 и 615.
Используя методику, аналогичную методике последнего параграфа примечания а), представленного выше, в части, касающейся получения исходных материалов, 4-хлор-3-{5-[N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамидо}-N -(3-фтор-5-морфолинофенил)бензамид восстанавливают с получением 3-{2-амино-5-[N-(3-диметиламинопропил)-N-метиламино]бензамидо}-4-хлор-N-(3-фтор-5-морфолинофенил)бензамида. Спектр ЯМР: (ДМСОd6) 1,54-1,62(м, 2Н), 2,1(с, 6Н), 2,18-2,22(м, 2Н), 2,77(с, 3Н), 3,09-3,16(м, 4Н), 3,18-3,22(м, 2Н), 3,7-3,74(м, 4Н), 6,57(д, 1Н), 6,7(д, 1Н), 6,84(д, 1Н), 7,08-7,24(м, 3Н), 7,7(д, 1Н), 7,8(д, 1Н), 8,27 (с, 1Н). Масс спектр: M+H+ 583.
d) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 593.
е) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 593.
3-[2-Амино-5-(3-диметиламинопропиламино)бензамидо]-4-хлор-N-(3-фтор-5-морфолинофенил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Используя методику, аналогичную той, что описана в шестом параграфе части примечания а), представленного выше, относящейся к получению исходных материалов, 4-хлор-3-(5-хлор-2-нитробензамидо)-N-(3-фтор-5-морфолинофенил)бензамид подвергают взаимодействию с 3-диметиламинопропиламином с получением 4-хлор-3-[5-(3-диметиламинопропиламино)-2-нитробензамидо]-N-(3-фтор-5-морфолинофенил)бензамида с 76% выходом. Спектр ЯМР: (ДМСОd6) 1,62-1,74(м, 2Н), 2,12(с, 6Н), 2,27(т, 2Н), 3,08-3,13(м, 4Н), 3,18-3,22(м, 2Н), 3,69-3,74(м, 4Н), 6,58(д, 1Н), 6,67(м, 2Н), 7,15-7,2(м, 2Н), 7,42(т, 1Н), 7,69(д, 1Н), 7,68(д, 1Н), 7,82(д, 1Н), 8,04(д, 1Н), 8,26(с, 1Н), 10,32(с, 1Н). Масс спектр: М+Н+ 599.
Используя методику, аналогичную методике последнего параграфа примечания а), представленного выше, в части, касающейся получения исходных материалов, 4-хлор-3-[5-(3-диметиламинопропиламино)-2-нитробензамидо]-N-(3-фтор-5-морфолинофенил)бензамид восстанавливают с получением требуемого исходного соединения. Спектр ЯМР: (ДМСОd6) 1,62-1,78(м, 2Н), 2,15(с, 6Н), 2,33(т, 2Н), 2,99(т, 2Н), 3,09-3,13(м, 4Н), 3,69-3,74(м, 4Н), 6,56(д, 1Н), 6,66(с, 2Н), 6,94(с, 1Н), 7,15-7,22(м, 3Н), 7,68(Д, 1Н), 7,78(д, 1Н), 8,32(с, 1Н), 10,29 (с, 1Н). Масс спектр: М+Н+ 569.
f) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 579.
g) Соединение имеет следующие характеристики. Масс спектр: M+H+ 593.
3-{2-Амино-5-[N-(3-метиламинопропил)-N-метиламино]бензамидо}-4-хлор-N-(3-фтор-5-морфолинофенил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Используя методику, аналогичную той, что описана в шестом параграфе части примечания а), представленного выше, относящейся к получению исходных материалов, 4-хлор-3-(5-хлор-2-нитробензамидо)-N-(3-фтор-5-морфолинофенил)бензамид подвергают взаимодействию с N-(3-метиламинопропил)-N-метиламином с получением 4-хлор-3-(5-хлор-2-нитробензамидо)-N-(3-фтор-5-морфолинофенил)бензамида. Спектр ЯМР: (ДМСОd6) 1,62-1,74(м, 2Н), 2,25(с, 3Н), 2,46-2,49(м, 2Н), 3,07(с, 3Н), 3,12(т, 2Н), 3,55(т, 2Н), 3,69-3,74(м, 4Н), 6,58(д, 1Н), 6,79(с, 1Н), 6,86(д, 1Н), 7,16-7,2(м, 2Н), 7,69(д, 1Н), 7,82(д, 1Н), 8,12(с, 1Н). Масс спектр: M+H+ 599.
Используя методику, аналогичную методике последнего параграфа примечания а), представленного выше, в части, касающейся получения исходных материалов, 4-хлор-N-(3-фтор-5-морфолинофенил)-3-{5-[N-(3-метиламинопропил)-N-метиламино]-2-нитробензамидо}бензамид восстанавливают с получением 3-{2-амино-5-[N-(3-метиламинопропил)-N-метиламино]бензамидо}-4-хлор-N-(3-фтор-5-морфолинофенил)бензамида. Масс спектр: M+H+569 и 571.
h) Соединение имеет следующие характеристики. Масс спектр: М+Н+ 579.
Пример 14
3-{3-[N-(3-Фтор-5-морфолинофенил)карбамоил]ДМС]Od}-8-[N-(3-диметиламинопропил)-N-метиламино]-3,4-дигидрохиназолин-4-он
Используя методику, аналогичную методике примера 1, 3-{2-амино-3-[N-(3-диметиламинопропил)-N-метиламино]бензамидо}-N-(3-фтор-5-морфолинофенил)бензамид подвергают взаимодействию с триэтилортоформиатом. Продукт реакции очищают хроматографией на ионообменной колонке isolute SCX, используя сначала метанол, затем 99:1 смесь метанола и насыщенного водного раствора гидроксида аммония в качестве элюента. Получают указанное в заголовке соединение. Масс спектр: М+Н+ 559.
3-{2-Амино-3-[N-(3-диметиламинопропил)-N-метиламино]бензамидо}-N-(3-фтор-5-морфолинофенил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Оксалилхлорид (0,51 г) по каплям добавляют к перемешиваемой смеси 3-хлор-2-нитробензойной кислоты (0,694 г), метиленхлорида (50 мл) и ДМФ (несколько капель), охлажденной до температуры 0°С. Смесь нагревают при температуре окружающей среды и перемешивают в течение 4 часов. Смесь выпаривают и остаток растворяют в метиленхлориде (10 мл) и по каплям добавляют к перемешиваемой смеси 3-амино-4-хлор-N-(3-фтор-5-морфолинофенил)бензамида (1,0 г) и пиридина (20 мл). Полученную смесь нагревают при температуре 80°С в течение 16 часов. Растворитель выпаривают и остаток растворяют в метиленхлориде (50 мл) и воде (50 мл) и перемешивают в течение 1 часа. Полученное твердое вещество фильтруют, промывают водой и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают 4-хлор-3-(3-хлор-2-нитробензамидо)-N-(3-фтор-5-морфолинофенил)бензамид (1,07 г). Спектр ЯМР: (ДМСОd6) 3,09-3,13(м, 4Н), 3,5-3,74(м, 4Н), 6,48(д, 1Н), 7,14-7,21(м, 2Н), 7,63(д, 1Н), 7,7-7,77(м, 2Н), 7,89(д, 1Н), 8,04(д, 1Н), 8,14(с, 1Н), 10,27(с, 1Н), 10,8 (с, 1Н). Масс спектр: M+H+ 533 и 535.
Смесь 4-хлор-3-(3-хлор-2-нитробензамидо)-N-(3-фтор-5-морфолинофенил)бензамида (0,51 г) и N-(3-диметиламинопропил)-N-метиламина (2 мл) перемешивают и нагревают при температуре 100°С в течение 16 часов. Смесь охлаждают и выливают в воду. Полученное твердое вещество выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают 4-хлор-3-{3-(N-(3-диметиламинопропил)-N-метиламино]-2-нитробензамидо}-N-(3-фтор-5-морфолинофенил)бензамид (0,45 г) Спектр ЯМР: (ДМСОd6) 1,48-1,58 (м, 2Н), 2,07 (с, 6Н), 2,15(т, 2Н), 2,69(с, 3Н), 3,03(т, 2Н), 3,08-3,15(м, 4Н), 3,7-3,75(м, 4Н), 6,74(д, 1Н), 7,15-7,2(м, 2Н), 7,44(д, 1Н), 7,52-7,64(д, 2Н), 7,7(д, 1Н), 7,82(д, 1Н), 8,08(с, 1Н), 10,32(с, 1Н). Масс спектр: M+H+613 и 615.
Смесь части (0,25 г) полученного соединения, 10% палладия на углероде (0,025 г) и метанола (25 мл) перемешивают в атмосфере водорода. После прекращения поглощения водорода катализатор удаляют фильтрацией через диатомовую землю и фильтрат выпаривают. Продукт реакции очищают хроматографией на ионообменной колонке isolute SCX, используя сначала метанол, затем 99:1 смесь метанола и насыщенного водного раствора гидроксида аммония в качестве элюента. Получают 3-{2-амино-3-[N-(3-диметиламинопропил)-N-метиламино]бензамидо}-N-(3-фтор-5-морфолинофенил)бензамид (0,102 г). Спектр ЯМР: (ДМСОd6) 1,58-1,62(м, 2Н), 2,09(с, 6Н), 2,25(т, 2Н), 2,56(с, 3Н), 2,77(т, 2Н), 3,09-3,13(м, 6Н), 3,7-3,73(м, 4Н), 6,39(с, 1Н), 6,48-6,64(м, 3Н), 7,08-7,24(м, 4Н), 7,4-7,5(м, 1Н), 7,62(д, 1Н), 7,92(д, 1Н), 8,26(с, 1Н), 10,14(с, 1Н), 10,22(с, 1Н). Масс спектр: М+Н+ 549.
Пример 15
3-[5-(2-Хлорпирид-4-илкарбониламино)-2-метилфенил]-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он
Используя методику, аналогичную методике примера 5, 3-(5-амино-2-метилфенил)-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он подвергают взаимодействию с 2-хлорпиридин-4-карбонилхлоридом с получением указанного в заголовке соединения. Спектр ЯМР: (ДМСОd6) 1,84-1,96 (м, 2Н), 2,06(с, 3Н), 2,29(с, ЗН), 2,42-2,49(м, 2Н), 2,62-2,68(м, 2Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 7,22(д, 1Н), 7,34(м, 1Н), 7,44(м, 1Н), 7,58(д, 1Н), 7,73-7,78(м, 2Н), 7,82-7,86(м, 1Н), 7,96-7,98(м, 2Н), 8,50-8,62(м, 1H), 10,68(с, 1Н). Масс спектр: М+Н+ 503 и 505.
3-(5-Амино-2-метилфенил)-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он, используемый в качестве исходного соединения, получают следующим образом.
Смесь N-(2-метил-5-нитрофенил)-5-хлор-2-нитробензамида (5 г), N-метилгомопиперазина (9,28 мл) и ДМСО (4 мл) перемешивают и нагревают при температуре 80°С в течение 4 часов. Реакционную смесь охлаждают до температуры окружающей среды и выливают в воду. Полученный осадок отделяют, промывают водой и диэтиловым эфиром и сушат в вакууме при температуре 40°С. Получают N-(2-метил-5-нитрофенил)-5-(4-метилгомопиперазин-1-ил)-2-нитробензамид (5,42 г). Спектр ЯМР: (ДМСОd6) 1,82-1,96(м, 2Н), 2,26(с, 3Н), 2,38(с, 3Н), 2,42-2,52(м, 2Н), 2,61-2,65(м, 2Н), 3,59-3,63(м, 2Н), 3,67-3,71(м, 2Н), 6,84-6,93(м, 2Н), 7,52(д, 1Н), 7,98(д, 1Н), 8,05(д, 1Н), 8,55(с, 1Н), 10,13(с, 1Н); Масс спектр: M+H+ 414.
Смесь полученного соединения, катализатора 10% палладия на углероде (0,54 г) и метанола (150 мл) перемешивают в атмосфере водорода до тех пор, пока не прекратится поглощение водорода. Катализатор отфильтровывают и фильтрат выпаривают. Получают N-(5-амино-2-метилфенил)-2-амино-5-(4-метилгомопиперазин-1-ил)бензамид (3,64 г) Спектр ЯМР: (ДМСОd6) 1,8-1,92(м, 2Н), 2,04(с, 3Н), 2,25(с, 3Н), 2,42-2,48(м, 2Н), 2,57-2,60(м, 2Н), 3,34-3,39(м, 2Н), 3,4-3,45(м, 2Н), 4,85(с, 2Н), 5,46(с, 2Н), 6,37(д, 1Н), 6,62-6,74(м, 3Н), 6,84(д, 1Н), 6,94(с, 1Н), 9,46(д, 1Н). Масс спектр: М+Н+ 354.
Смесь полученного соединения, триэтилортоформиата (3,41 мл), ледяной уксусной кислоты (0,3 мл) и этанола (75 мл) перемешивают и нагревают при температуре 70°С в течение 16 часов. Добавляют 1N водный раствор соляной кислоты (20,6 мл) и смесь перемешивают при температуре 60°С в течение 3 часов. Полученную смесь выпаривают. Остаток растворяют в воде, подщелачивают добавлением бикарбоната натрия и экстрагируют метиленхлоридом. Органический экстракт выпаривают с получением 3-(5-амино-2-метилфенил)-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-она (3,78 г). Спектр ЯМР: (ДМСОd6) 1,86(с, 3Н), 1,89-1,92(м, 2Н), 2,24(с, 3Н), 2,44-2,49(м, 2Н), 2,6-2,63(м, 2Н), 3,49-3,53(м, 2Н), 3,58-3,62(м, 2Н), 5,14(с, 2Н), 6,46(с, 1Н), 6,6(д, 1Н), 7,01(д, 1Н), 7,22(с, 1Н), 7,32(д, 1Н), 7,55(д, 1Н), 7,86(д, 1Н). Масс спектр: M+H+ 364.
Пример 16
3-[5-(3,5-Дифторбензамидо)-2-метилфенил]-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он
Используя методику примера 5, 3-(5-амино-2-метилфенил)-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он подвергают взаимодействию с 3,5-дифторбензоилхлоридом с получением указанного в заголовке соединения. Спектр ЯМР: (ДМСОd6) 1,84-1,96(м, 2Н), 2,05(с, 3Н), 2,25(с, 3Н), 2,42-2,5(м, 2Н), 2,62-2,64(м, 2Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 7,24(д, 1Н), 7,38(м, 1Н), 7,40-7,44(м, 1Н), 7,48-7,54(м, 1Н), 7,58(д, 1Н), 7,64-7,67(м, 2Н), 7,75-7,78(м, 2Н), 7,96(с, 1Н), 10,49(с, 1Н). Масс спектр: М+Н+ 504.
Пример 17
Используя методику примера 10, подходящий 3-(5-амино-2-метилфенил)-3,4-дигидрохиназолин-4-он подвергают взаимодействию с подходящей карбоновой кислотой с получением соединений, описанных в таблице VIII.
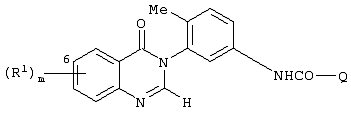
| Таблица VIII |
|
(R1)m |
Q |
Прим. |
| 1 |
6-(4-метилпиперазин-1-ил) |
1-флуоренил |
а |
| 2 |
6-(4-метилпиперазин-1-ил) |
3,4-метилендиоксифенил |
b |
| 3 |
6-(4-метилпиперазин-1-ил) |
3,4-триметилендиоксифенил |
с |
| 4 |
6-(4-метилпиперазин-1-ил) |
2,3-дигидробензофуран-7-ил |
d |
| 5 |
6-(4-метилпиперазин-1-ил) |
2-метил-2,3-дигидробензофуран-7-ил |
е |
| 6 |
6-(4-метилпиперазин-1-ил) |
2,2-диметилхроман-6-ил |
f |
| 7 |
6-(4-метилгомопиперазин-1-ил) |
дибензофуран-4-ил |
g |
| 8 |
6-(4-метилгомопиперазин-1-ил) |
1-флуоренил |
h |
| 9 |
6-(4-метилпиперазин-1-ил) |
5-(3-хлорфенил)фуран-2-ил |
i |
| 10 |
6-(4-метилпиперазин-1-ил) |
5-(4-хлорфенил)фуран-2-ил |
j |
| 11 |
6-(4-метилпиперазин-1-ил) |
5-(4-хлорфенил)тиен-2-ил |
k |
| 12 |
6-(4-метилпиперазин-1-ил) |
4-(4-хлорфенил)тиен-2-ил |
l |
| 13 |
6-(4-метилпиперазин-1-ил) |
4-(4-метоксифенил)тиен-2-ил |
m |
| 14 |
6-(4-метилпиперазин-1 -ил) |
3-фенилизотиазол-5-ил |
n |
| 15 |
8-(4-метилпиперазин-1-ил) |
дибензофуран-4-ил |
о |
| 16 |
8-(4-метилпиперазин-1-ил) |
1-флуоренил |
p |
| 17 |
6-пиперазин-1-ил |
1-флуоренил |
q |
| 18 |
6-пиперазин-1-ил |
дибензофуран-4-ил |
r |
Примечания
a) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,23(с, 3Н), 2,47-2,5(м, 4Н), 3,2-3,3(м, 4Н), 4,18(с, 2Н), 7,3-7,48(м, 4Н), 7,5-7,63(м, 4Н), 7,75(д, 1Н), 7,8(д, 1Н), 7,87(с, 1Н), 7,95(д, 1Н), 8,08-8,11(м, 2Н), 10,49(с, 1Н). Масс спектр: М+Н+ 542.
b) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,25(с, 3Н), 2,50(м, 4Н), 3,26(м, 4Н), 6,12(с, 2Н), 7,06(д, 1Н), 7,41(д, 1Н), 7,49(д, 2Н), 7,58(м, 1Н), 7,65(д, 2Н), 7,88(м, 2Н), 8,08(с, 1Н), 10,23(с, 1Н). Масс спектр: М+Н+ 498.
c) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05 (с, 3Н), 2,15(м, 2Н), 2,25 (с, 3Н), 2,5-3,35(м, 8Н), 4,2(м, 4Н), 7,6(д, 1Н), 7,4(д, 1Н), 7,48(с, 1Н), 7,55-7,65(м, 4Н), 7,76-7,85(м, 2Н), 8,1(с, 1Н), 10,26(с, 1Н).
Масс спектр: М+Н+ 526.
d) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,3(с, 3Н), 2,55(м, 4Н), 3,25(м, 2Н), 3,3(м, 4Н), 4,75(т, 2Н), 6,98(м, 1Н), 7,39-7,49(м, 3Н), 7,58-7, 65 (м, 3Н), 7,8(м, 2Н), 8,1 (с, 1Н), 9, 9 (с, 1Н). Масс спектр: М+Н+ 496.
e) 2-Метил-2,3-дигидробензофуран-7-карбоновую кислоту, используемую в качестве исходного соединения, получают, как описано в Monatschefte fur Chemie, 1990, 121, 883-891. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,50(м, 3Н), 2,05(с, 3Н), 2,25(с, 3Н), 2,55(м, 4Н), 3,28(м, 4Н), 3,39(м, 2Н), 5,12(м, 1Н), 6,98(с, 1Н), 7,41(д, 2Н), 7,49(c, 1H), 7,61(м, 3Н), 7,8(м, 2Н), 8,1(с, 1H), 9,87(с, 1Н). Масс спектр: М+Н+ 510.
f) 2,2-Диметилхроман-6-карбоновую кислоту, используемую в качестве исходного соединения, получают, как описано в Tetrahedron, 1982, 38, 3673-3677. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,30(м, 6Н), 1,79(м, 2Н), 2,05(с, 3Н), 2,25(с, 3Н), 2,5(м, 4Н), 2,8(м, 2Н), 3,3(м, 4Н), 6,8(д, 1Н), 7,38(м, 1Н), 7,46(м, 1Н), 7,62(м, 2Н), 7,69-7,98(м, 4Н), 8,09(с, 1Н), 10,18(с, 1Н). Масс спектр: М+Н+ 538.
g) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,84-1,94(м, 2Н), 2,07(с, 3Н), 2,25(с, 3Н), 2,42-2,5(м, 2Н), 2,62-2,66(м, 2Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 7,26(с, 1Н), 7,38(д, 1Н), 7,4-7,5(м, 2Н), 7,51-7,61(м, 3Н), 7,78-7,86(м, 4Н), 8,01(с, 1Н), 7,92-7,99(м, 2Н), 8,22(д, 1Н), 8,38(д, 1Н), 10,59(с, 1Н). Масс спектр: M+H+ 558.
h) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 1,86-1, 98 (м, 2Н), 2,06 (с, 3Н), 2,25 (с, 3Н), 2,42-2,5(м, 2Н), 2,62-2,66(м, 2Н), 3,53(т, 2Н), 3,58-3,64(м, 2Н), 4,12(с, 2Н), 7,24(с, 1Н), 7,32-7,43(м, 4Н), 7,52-7,61(м, ЗН), 7,72(д, 1Н), 7,8(д, 1Н), 7,85(с, 1Н), 7,92-7,99(м, 2Н), 8,18(д, 1Н), 10,49 (с, 1Н). Масс спектр: М+Н+ 556.
i) 5-(3-Хлорфенил)фуран-2-карбоновую кислоту, используемую в качестве исходного соединения, получают, как описано в Chem. Pharm. Bull., 1981, 29, 2420-2430. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05 (с, 3Н), 2,22(с, 3Н), 2,47-2,5(м, 4Н), 3,25-3,35(м, 4Н), 7,28(д, 1Н), 7,38-7,48(м, 5Н), 7,62(с, 2Н), 7,76(с, 1Н), 7,84(м, 1Н), 7,9(д, 1Н), 8,08(с, 2Н), 10,38(с, 1Н). Масс спектр: M+H+ 554 и 556.
j) 5-(4-Хлорфенил)фуран-2-карбоновую кислоту, используемую в качестве исходного соединения, получают, как описано в Chem. Pharm. Bull., 1981, 29, 2420-2430. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,22(с, 3Н), 2,47-2,5(м, 4Н), 3,2-3,3(м, 4Н), 7,2(д, 1Н), 7,39-7,48(м, 3Н), 7,54(д, 2Н), 7,63(с, 2Н), 7,75(с, 1Н), 7,84(м, 1Н), 7,98(м, 2Н), 8,08(с, 1Н), 10,34(с, 1Н). Масс спектр: М+Н+ 554 и 556.
k) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,04(с, 3Н), 2,46(с, 3Н), 2,47-2,5(м, 2Н), 3,2-3,3(м, 4Н), 7,41(д, 1Н), 7,48-7,51(м, 3Н), 7,6-7,65(м, 3Н), 7,73-7,8(м, 4Н), 8,01(д, 1Н), 8,07(с, 1Н), 10,5(с, 1Н). Масс спектр: М+Н+ 570 и 572.
l) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,22(с, 3Н), 2,47-2,5(м, 2Н), 3,2-3,3(м, 4Н), 7,38-7,53(м, 4Н), 7,61-7,65(м, 2Н), 7,72-7,8(м, 4Н), 8,08(с, 1Н), 8,22(с, 1Н), 8,47(с, 1Н), 10,5(с, 1Н). Масс спектр: M+H+ 570 и 572.
m) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,23(с, 3Н), 2,47-2,5(м, 2Н), 3,2-3,3(м, 4Н), 3,7(с, 3Н), 7,01(д, 2Н), 7,43(д, 1Н), 7,48(с, 1Н), 7,6-7,66(м, 4Н), 7,74-7,8(м, 2Н), 8,02(с, 1Н), 8,08(с, 1Н), 8,4 (с, 1Н), 10,41(с, 1Н). Масс спектр: М+Н+ 566.
n) 3-Фенилизотиазол-5-карбоновую кислоту, используемую в качестве исходного соединения, получают, как описано в Helv. Chim. Acta, 1966, 49, 2466-2469. Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,03(с, 3Н), 2,22(с, 3Н), 2,47-2,5(м, 4Н), 3,25-3,35(м, 4Н), 7,35(д, 1Н), 7,44-7,52(м, 5Н), 7,62(с, 1Н), 7,64-7,73(м, 2Н), 7,98(д, 2Н), 8,06(с, 1Н), 8,4(с, 1Н), 10,38(с, 1Н). Масс спектр: M+H+ 537.
о) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,2(с, 4Н), 7,3-7,35(м, 1Н), 7,4-7,6(м, 5Н), 7,75-7,9(м, 5Н), 8,2(д, 1Н), 8,3-8,4(м, 2Н), 10,6(с, 1Н). Масс спектр: М+Н+ 544.
р) Соединение имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,05(с, 3Н), 2,3 (с, 3Н), 2,5-2,65(м, 4Н), 4,18(с, 2Н), 7,3-7,65(м, 7Н), 7,7-7,8(м, 3Н), 7,9(с, 1Н), 7,95(д, 1Н), 8,1(д, 1Н), 8,3 (с, 1Н), 10,5(с, 1Н). Масс спектр: М+Н+ 542.
q) 3-(5-Амино-2-метилфенил)-6-(4-трет-бутоксикарбонилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он используют в качестве исходного соединения. Начальным продуктом реакции является 3-[5-флуорен-1-илкарбониламино-2-метилфенил]-6-(4-трет-бутоксикарбонилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он, который обрабатывают насыщенным раствором хлористого водорода в этаноле для отщепления трет-бутоксикарбонильной защитной группы. Полученный продукт имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,07(с, 3Н), 3,26(м, 4Н), 3,5(м, 4Н), 4,18(с, 2Н), 7,32-7,5(м, 4Н), 7,55-7,63(м, 3Н), 7,69-7,81(м, 4Н), 7,91-8,0(м, 3Н), 8,11(с, 1Н), 8,87(с, 1Н). Масс спектр: M+H+ 528.
3-(5-Амино-2-метилфенил)-6-(4-трет-бутоксикарбонилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он, используемый в качестве исходного соединения, получают следующим образом.
Смесь N-(2-метил-5-нитрофенил)-5-хлор-2-нитробензамида (5,02 г), пиперазина (5,13 г) и ДМСО (15 мл) перемешивают и нагревают при температуре 100°С в течение 2 часов. Смесь охлаждают до температуры окружающей среды и выливают в воду. Полученное твердое вещество выделяют, промывают последовательно водой и диэтиловым эфиром и сушат в вакууме при температуре 55°С. Получают N-(2-метил-5-нитрофенил)-2-нитро-5-пиперазин-1-илбензамид (4,88 г). Спектр ЯМР: (ДМСОd6) 2,38(с, 3Н), 2,8(м, 4Н), 3,43(м, 4Н), 7,04(м, 1Н), 7,14(д, 1Н), 7,52(д, 1Н), 8,01(м, 1Н), 8,06(д, 1Н), 8,53(д, 1Н), 10,14(с, 1Н). Масс спектр: М+Н+ 386.
2-(трет-Бутоксикарбонилоксиимино)фенилацетонитрил (2,55 г) добавляют к смеси N-(2-метил-5-нитрофенил)-2-нитро-5-пиперазин-1-илбензамида (2,5 г), триэтиламина (1,7 мл), воды (30 мл) и 1,4-диоксана (30 мл) и полученную смесь перемешивают при температуре окружающей среды в теченние 16 часов. Смесь разбавляют водой и полученное твердое вещество выделяют и промывают последовательно водой и диэтиловым эфиром. Получают N-(2-метил-5-нитрофенил)-5-(4-трет-бутоксикарбонилпиперазин-1-ил)-2-нитробензамид (2,85 г). Спектр ЯМР: (CDCl3) 1,48(с, 9Н), 2,37(с, 3Н), 3,48(м, 4Н), 3,61(м, 4Н), 6,77(м, 1Н), 6,87(м, 1Н), 7,33(д, 1Н), 7,56(с, 1Н), 7,95(м, 1Н), 8,04(д, 1Н), 8, 68 (с, 1Н). Масс спектр: M+H+ 484.
Полученное соединение гидрируют в присутствии катализатора 10% палладия на углероде, используя методику, аналогичную той, которая описана в третьем параграфе части примера 5, относящейся к получению исходных материалов. Получают N-(5-амино-2-метилфенил)-2-амино-5-(4-трет-бутоксикарбонилпиперазин-1-ил)бензамид с 96% выходом. Спектр ЯМР: (CDCl3) 1,5(с, 9Н), 2,21(с, 3Н), 3,0(м, 4Н), 3,6(м, 4Н), 3,65(с, 2Н), 4,98(с, 2Н), 6,47(м, 1Н), 6,73(д, 1Н), 7,01(м, 2Н), 7,11(д, 1Н), 7,41(д, 1Н), 7,8(с, 1Н). Масс спектр: M+H+ 426.
Смесь полученного соединения (2,12 г), триэтилортоформиата (1,7 мл), ледяной уксусной кислоты (0,07 мл) и этанола (50 мл) перемешивают и нагревают при температуре 70°С в течение 16 часов. Добавляют раствор гидроксида натрия (1М, 5,0 мл) и смесь перемешивают и нагревают при температуре 60°С в течение 16 часов. Добавляют другую порцию раствора гидроксида натрия (1М, 2,5 мл) и смесь опять нагревают при температуре 60°С в течение 16 часов. Полученную смесь охлаждают до температуры окружающей среды и выпаривают. Остаток растворяют в воде и экстрагируют метиленхлоридом. Органическую фазу сушат и выпаривают. Полученное соединение очищают хроматографией на колонке с двуокисью кремния, используя 20:1 смесь метиленхлорида и метанола. Получают 3-(5-амино-2-метилфенил)-6-(4-трет-бутоксикарбонилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он (1,51 г). Спектр ЯМР: (CDCl3) 1,5(с, 9Н), 2,06(с, 3Н), 3,27(м, 4Н), 3,62(м, 4Н), 3,72(с, 2Н), 6,58(д, 1Н), 6,74(м, 1Н), 7,15(д, 1Н), 7,44(м, 1Н), 7,68(м, 2Н), 7,86(с, 1Н). Масс спектр: М+Н+ 436.
г) 3-(5-Амино-2-метилфенил)-6-(4-трет-бутоксикарбонилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он используют в качестве исходного соединения. Начальным продуктом реакции является 3-[5-дибензофуран-4-илкарбониламино-2-метилфенил]-6-(4-трет-бутоксикарбонилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он, который обрабатывают насыщенным раствором хлористого водорода в этаноле для отщепления трет-бутоксикарбонильной защитной группы. Полученный продукт имеет следующие характеристики. Спектр ЯМР: (ДМСОd6) 2,07(с, 3Н), 3,29(м, 4Н), 3,5(м, 4Н), 7,42-7,6(м, 6Н), 7,67(м, 1Н), 7,8-7,9(м, 4Н), 7,95(с, 1Н), 8,20-8,27(м, 2Н), 8,36(д, 1Н), 8,85(с, 1Н). Масс спектр: M+H+ 530.
Пример 18
3-[2-Фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-6-(4 - метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он
Триэтилортоформиат (0,123 мл) добавляют к перемешиваемой смеси N-[2-фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-(4-метилпиперазин-1-ил)бензамида (0,31 г), ледяной уксусной кислоты (0,016 мл) и этанола (4 мл) и полученную смесь нагревают при температуре 76°С в течение 18 часов. Смесь выпаривают и остаток распределяют между метиленхлоридом и насыщенным водным раствором бикарбоната натрия. Органический раствор промывают водой и насыщенным водным раствором хлорида натрия, сушат (MgSO4) и выпаривают. Остаток очищают хроматографией на колонке с двуокисью кремния, использую смесь с увеличивающейся полярностью метиленхлорида и метанола в качестве элюента. Получают указанное в заголовке соединение (0,119 г). Спектр ЯМР: (ДМСОd6) 2,23 (с, 3Н), 3,22(м, 4Н), 3,72(м, 4Н), 6,99(д, 1Н), 7,12(д, 1Н), 7,29(с, 1Н), 7,47(м, 2Н), 7,63(с, 1Н), 7,89(м, 1Н), 7,97(м, 1Н), 8,18(с, 1Н), 10,44 (с, 1Н). Масс спектр: M+H+ 561.
N-[2-Фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-(4-метилпиперазин-1-ил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Оксалилхлорид (0,55 г) по каплям добавляют к перемешиваемой смеси 3-фтор-5-морфолинобензойной кислоты (6,36 г), ДМФ (несколько капель) и метиленхлорида (200 мл), охлажденной до температуры 0°С. Смеси дают нагреться до температуры окружающей среды и перемешивают в течение 4 часов. Смесь выпаривают. Остаток растворяют в метиленхлориде (100 мл) и по каплям добавляют к перемешиваемой смеси 4-фтор-3-нитроанилина (4,05 г), триэтиламина (12,0 мл) и метиленхлорида (100 мл). Полученную смесь перемешивают при температуре окружающей среды в течение 20 часов. Смесь выпаривают и остаток распределяют между метиленхлоридом и водой. Органическую фазу промывают насыщенным водным раствором хлорида натрия, сушат (MgSO4) и выпаривают. Получают N-(4-фтор-3-нитрофенил)-3-фтор-5-морфолинобензамид (7,06 г). Спектр ЯМР: (ДМСОd6) 3,24(м, 4Н), 3,73(м, 4Н), 7,0(м, 1Н), 7,13(д, 1Н), 7,3(с, 1Н), 7,58(т, 1Н), 8,11(м, 1Н), 8,63(м, 1Н), 10,56(с, 1Н). Масс спектр: М-Н- 362.
Смесь части (4,34 г) полученного соединения, 30% палладия на углероде (0,68 г) и метанола (500 мл) перемешивают в атмосфере водорода. После прекращения поглощения водорода катализатор удаляют фильтрацией и фильтрат выпаривают. Получают N-(3-амино-4-фторфенил)-3-фтор-5-морфолинобензамид (3,49 г).
Спектр ЯМР: (ДМСОd6) 3,22(м, 4Н), 3,75(м, 4Н), 5,12(с, 2Н), 6,81(м, 1Н), 6,89-6,96(м, 2Н), 7,08(д, 1Н), 7,24(м, 2Н), 9,92(с, 1Н). Масс спектр: M+H+ 334.
Диизопропиламин (3,13 мл) добавляют к смеси N-(3-амино-4-фторфенил)-3-фтор-5-морфолинобензамида (1,99 г), 5-хлор-2-нитробензойной кислоты (1,45 г), 2-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилуроний гексафторфосфата(V) (2,74 г) в ДМФ (12 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение 18 часов. Смесь выливают в воду и полученный осадок отделяют, промывают водой и сушат в вакууме при температуре 55°С. Получают N-[2-фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-5-хлор-2-нитробензамид (1,64 г). Спектр ЯМР: (ДМСОd6) 3,22(м, 4Н), 3,74(м, 4Н), 6,97(д, 1Н), 7,15(д, 1Н), 7,25-7,32(м, 2Н), 7,66(м, 1Н), 7,82(м, 2Н), 7,88(с, 1Н), 8,18(д, 1Н), 8,34(м, 1Н), 10,32(с, 1Н), 10,58(с, 1Н). Масс спектр: M+H+ 517 и 519.
Смесь части (0,55 г) полученного соединения и N-метилпиперазина (2 мл) перемешивают и нагревают при температуре 80°С в течение 18 часов. Реакционную смесь охлаждают до температуры окружающей среды и выливают в воду. Полученный осадок выделяют, промывают водой и сушат в вакууме при температуре 55°С. Получают N-[2-фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-5-(4-метилпиперазин-1-ил)-2-нитробензамид (0,55 г).
Спектр ЯМР: (ДМСОd6) 2,2(с, 3Н), 2,41(м, 3Н), 3,22(м, 4Н), 3,48(м, 4Н), 3,72(м, 4Н), 6,93(м, 2Н), 7,07(м, 1Н), 7,16(д, 1Н), 7,25(т, 1Н), 7,32(с, 1Н), 7,63(м, 1Н), 8,14(д, 1Н), 8,36(м, 1Н), 10,26(с, 1Н), 10,3(с, 1Н). Масс спектр: M+H+ 581.
Смесь полученного соединения, 30% палладия на углероде (0,075 г) и этанола (500 мл) перемешивают в атмосфере водорода. После прекращения поглощения водорода катализатор удаляют фильтрацией и фильтрат выпаривают. Получают N-[2-фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-(4-метилпиперазин-1-ил)бензамид (0,52 г). Спектр ЯМР: (ДМСОd6) 2,22(с, 3Н), 2,44(м, 4Н), 2,98(м, 4Н), 3,21(м, 4Н), 3,72(м, 4Н), 5,93(ш с, 1Н), 6,69(д, 1Н), 6,94-7,01(м, 2Н), 7,12(д, 1Н), 7,2-7,3(м, 3Н), 7,59(м, 1Н), 7,97(м, 1Н), 10,24(с, 1Н). Масс спектр: М+Н+ 551.
Пример 19
3-[2-Фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-6-(4-метилгомопиперазин-1-ил)-3,4-дигидрохиназолин-4-он
Используя методику примера 18, N-[2-фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-(4-метилгомопиперазин-1-ил)бензамид подвергают взаимодействию с триэтилортоформиатом с получением указанного в заголовке соединения с 63% выходом. Спектр ЯМР: (ДМСОd6) 1,92(м, 2Н), 2,25(с, 3Н), 2,46(м, 2Н), 2,64(м, 2Н), 3,21(т, 4Н), 3,53(т, 2Н), 3,6(м, 2Н), 3,72(т, 4Н), 6,99(д, 1Н), 7,12(д, 1Н), 7,23(м, 1Н), 7,3(с, 1Н), 7,36(м, 1Н), 7,48(т, 1Н), 7,58(д, 1Н), 7,87(м, 1Н), 7,96(м, 1Н), 8,06 (с, 1Н), 10,43 (с, 1Н). Масс спектр: M+H+ 575.
N-[2-Фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-(4-метилгомопиперазин-1-ил)бензамид, используемый в качестве исходного соединения, получают следующим образом.
Смесь N-[2-фтор-5-(З-фтор-5-морфолинобензамидо)фенил]-5-хлор-2-нитробензамида (0,55 г) и N-метилгомопиперазина (2 мл) перемешивают и нагревают при температуре 80°С в течение 18 часов. Реакционную смесь охлаждают до температуры окружающей среды и выливают в воду. Полученный осадок отделяют, промывают водой и сушат в вакууме при температуре 55°С. Получают N-[2-фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-5-(4-метилгомопиперазин-1-ил)-2-нитробензамид (0,58 г). Спектр ЯМР: (ДМСОd6) 1,89(м, 2Н), 2,25(с, 3Н), 2,44(м, 2Н), 2,63(м, 2Н), 3,22(т, 4Н), 3,59(т, 2Н), 3,66(м, 2Н), 3,74(т, 4Н), 6,72(д, 1Н), 6,87(м, 1Н), 6,97(д, 1Н), 7,16(д, 1Н), 7,23(т, 1Н), 7,31(с, 1Н), 7,63(м, 1Н), 8,02(д, 1Н), 8,34(м, 1Н), 10,3(с, 1Н). Масс спектр: М+Н+ 595.
Смесь полученного соединения, 30% палладия на углероде (0,08 г) и этанола (500 мл) перемешивают в атмосфере водорода. После прекращения поглощения водорода катализатор удаляют фильтрацией и фильтрат выпаривают. Получают N-[2-фтор-5-(3-фтор-5-морфолинобензамидо)фенил]-2-амино-5-(4-метилгомопиперазин-1-ил)бензамид (0,48 г). Спектр ЯМР: (ДМСОd6) 1,86(м, 2Н), 2,24(с, 3Н), 2,44(м, 2Н), 2,59(м, 2Н), 3,22(т, 4Н), 3,38(т, 2Н), 3,43(м, 2Н), 3,72(т, 4Н), 6,68(д, 1Н), 6,76(м, 1Н), 6,98(м, 2Н), 7,12(м, 1Н), 7,22-7,31(м, 2Н), 7,58(м, 1Н), 8,08(м, 1Н), 10,25(ш с, 1Н). Масс спектр: M+H+ 565.
Пример 20
Фармацевтические композиции
Далее проиллюстрированы примеры фармацевтических дозированных форм данного изобретения (активный ингредиент обозначен как «Соединение X») для терапевтического и профилактического применения человеком.
| (a) Таблетки I |
мг/таблетка |
| Соединение Х |
100 |
| Лактоза Ph.Eur. |
182,75 |
| Кросскармеллоза натрия |
12,0 |
| Паста кукурузного крахмала (5% мас./об паста) |
2,25 |
| Стеарат магния |
3,0 |
| (b) Таблетки II |
мг/таблетка |
| Соединение Х |
50 |
| Лактоза Ph.Eur. |
223,75 |
| Кросскармеллоза натрия |
6,0 |
| Кукурузный крахмал |
15,0 |
| Поливинилпирролидон (5% мас./об паста) |
2,25 |
| Стеарат магния |
3,0 |
| (c) Таблетки III |
мг/таблетка |
| Соединение Х |
1,0 |
| Лактоза Ph.Eur. |
93,25 |
| Кросскармеллоза натрия |
4,0 |
| Паста кукурузного крахмала (5% мас./об паста) |
0,75 |
| Стеарат магния |
1,0 |
| (d) Капсулы |
мг/капсула |
| Соединение Х |
10 |
| Лактоза Ph.Eur. |
488,5 |
| Магний |
1,5 |
| (e) Раствор для инъекций I |
(50 мг/мл) |
| Соединение Х |
5,0% мас./об |
| 1М раствор гидроксида натрия |
15,0% об/об |
| 0,1М соляная кислота для доведения рН |
до 7,6 |
| Полиэтиленгликоль 400 |
4,5% мас./об |
| Вода для инъекций до |
100% |
| (f) Раствор для инъекций II |
(10 мг/мл) |
| Соединение Х |
1,0% мас./об |
| Фосфат натрия ВР |
3,6% мас./об |
| 0,1М раствор гидроксида натрия |
15,0% об/об |
| Вода для инъекций до |
100% |
(g) Раствор для инъекций III (1 мг/мл, забуференный до рН 6)
| Соединение Х |
0,1% мас./об |
| Фосфат натрия ВР |
2,26% мас./об |
| Лимонная кислота |
0,38% мас./об |
| Полиэтиленгликоль 400 |
3,5% мас./об |
| Вода для инъекций до |
100% |
| (h) Аэрозоль I |
мг/мл |
| Соединение Х |
10,0 |
| Сорбитан триолеат |
13,5 |
| Трихлорфторметан |
910,0 |
| Дихлордифторметан |
490,0 |
| (i) Аэрозоль II |
мг/мл |
| Соединение Х |
0,2 |
| Сорбитан триолеат |
0,27 |
| Трихлорфторметан |
70,0 |
| Дихлордифторметан |
280,0 |
| Дихлортетрафторэтан |
1094,0 |
| (j) Аэрозоль III |
мг/мл |
| Соединение Х |
2,5 |
| Сорбитан триолеат |
3,38 |
| Трихлорфторметан |
67,5 |
| Дихлордифторметан |
1086,0 |
| Дихлортетрафторэтан |
191,6 |
| (k) Аэрозоль IV |
мг/мл |
| Соединение Х |
2,5 |
| Соевый лецитин |
2,7 |
| Трихлорфторметан |
67,5 |
| Дихлордифторметан |
1086,0 |
| Дихлортетрафторэтан |
191,6 |
| (l) Мазь |
мл |
| Соединение Х |
40 мг |
| Этанол |
300 мкл |
| Вода |
300 мкл |
| 1-Додецилазациклогептан-2-он |
50 мкл |
| Пропиленгликоль до |
1 мл |
Примечание
Представленные выше препаративные формы получают обычными методами, хорошо известными в области фармацевтики. Таблетки (а)-(с) могут иметь энтеросолюбильную оболочку, нанесенную обычными средствами, например, для получения оболочки из фталата ацетата целлюлозы. Аэрозольные препаративные формы (h)-(k) могут быть введены с помощью стандартных аэрозолей для ингаляций с дозирующим устройством, и супендирующие агенты сорбитан триолеат и соевый лецитин могут быть заменены альтернативным суспендирующим агентом, таким как сорбитан моноолеат, сорбитан сесквиолеат, полисорбат 80, полиглицерин олеат или олеиновая кислота.
Формула изобретения
1. Производное амида формулы Ia
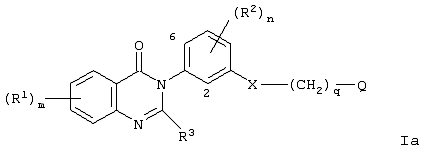
в которой Х является -NHCO- или -CONH-;
m равно 0, 1, 2 или 3;
R1 является галогеном, (1-6С)алкокси, N-(1-6С)алкил-ди[(1-6C)алкил]амино-(2-6С)-алкиламино
или R1 является гетероциклилом, гетероциклил-(1-6C)алкилом, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6С)алкил-гетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6C) -алкилгетероциклил-(1-6С)алкиламино, гетероциклилкарбониламино, гетероциклилсульфониламино, N-гетероциклилсульфамоилом, гетероциклил-(2-6С)алканоиламино, гетероциклил-(1-6C)алкокси-(1-6С)алкилом, гетероциклил-(1-6C)алкиламино-(1-6C)алкилом или N-(1-6С)алкилгетероциклил-(1-6C)алкиламино-(1-6C)алкилом,
и где любая гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из галогена, (1-6С)алкила и (1-6С)алкокси,
и где любая гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из оксо или тиоксогруппы;
n равно 0, 1 или 2;
R2 является галогеном или (1-6С)алкилом;
R3 является водородом, галогеном, (1-6С)алкилом или (1-6С)алкокси;
q равно 0, 1, 2, 3 или 4; и
Q является арилом, арилокси, арил-(1-6С)алкокси, ариламино, N-(1-6C)алкил-ариламино, арил-(1-6С)алкиламино, N-(1-6С)алкил-арил-(1-6С)алкиламино, (3-7С)циклоалкилом, гетероарилом, гетероарилокси, гетероарил-(1-6С)алкокси, гетероариламино, N-(1-6С)алкилгетероариламино, гетероарил-(1-6C)алкиламино, N-(1-6С)алкилгетероарил-(1-6C)алкиламино, гетероциклилом, гетероциклилокси, гетероциклил-(1-6С)алкокси, гетероциклиламино, N-(1-6C)алкилгетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6C)алкилгетероциклил-(1-6C)алкиламино, необязательно замещен 1, 2 или 3 заместителями, выбранными из гидрокси, галогена, трифторметила, циано, меркапто, нитро, амино, карбокси, карбамоила, формила, (1-6С)алкила, (2-6С)алкенила, (2-6С)алкинила, (1-6C)алкокси, (1-6С)алкилтио, (1-6C)алкилсульфинила, (1-6C)алкилсульфонила, (1-6C)алкиламино, ди-[(1-6C)алкил]амино, (1-6С)алкоксикарбонила, N-(1-6С)алкилкарбамоила, N,N-ди[(1-6С)алкил]карбамоила, (2-6С)алканоила, (2-6С)алканоилокси, (1-6C)алканоиламино, N-(1-6С)алкил-(1-6C)алканоиламино, N-(1-6C)алкилсульфамоила, N,N-ди-[(1-6C)алкил]сульфамоила, (1-6C)алкансульфониламино, N-(1-6С)алкил-(1-6C)алкансульфониламино, галоген-(1-6C)алкила, гидрокси-(1-6C)алкила, (1-6С)алкокси-(1-6С)алкила, циано-(1-6С)алкила, амино-(1-6С)алкила, (1-6С)алкиламино-(1-6С)алкила, ди-[(1-6С)алкил]амино-(1-6С)алкила, карбокси-(1-6С)алкила, (1-6C)алкоксикарбонил-(1-6С)алкила, карбамоил-(1-6С)алкила, N-(1-6С)алкилкарбамоил-(1-6С)алкила, N,N-ди-[(1-6С)алкил]-карбамоил-(1-6С)алкила, галоген-(2-6С)алкокси, гидрокси-(2-6С)алкокси, (1-6С)алкокси-(2-6С)алкокси, циано-(1-6С)алкокси, карбокси-(1-6С)алкокси, (1-6С)алкоксикарбонил-(1-6С)алкокси, карбамоил-(1-6С)алкокси, N-(1-6C)алкилкарбамоил-(1-6С)алкокси, N,N-ди-[(1-6C)алкил]карбамоил-(1-6C)алкокси, амино-(2-6С)алкокси, (1-6C)алкиламино-(2-6С)алкокси, ди-[(1-6C)алкил]амино-(2-6С)-алкокси, галоген-(2-6С)алкиламино, гидрокси-(2-6С)алкиламино, (1-6C)алкокси-(2-6С)алкиламино, циано-(1-6C)алкиламино, карбокси-(1-6C)алкиламино, (1-6C)алкоксикарбонил-(1-6C)алкиламино, карбамоил-(1-6C)алкиламино, N-(1-6C)алкилкарбамоил-(1-6C)-алкиламино, N,N-ди-[(1-6C)алкил]карбамоил-(1-6C)алкиламино, амино-(2-6С)алкиламино, (1-6C)алкиламино-(2-6С)алкиламино, ди-[(1-6C)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкилгалоген-(1-6С)алкиламино, N-(1-6C)алкилгидрокси-(2-6С)алкиламино, N-(1-6С)алкил-(1-6C)алкокси-(2-6С)алкиламино, N-(1-6С)алкилциано-(1-6С)алкиламино, N-(1-6C)алкилкарбокси-(1-6C)алкиламино, N-(1-6С)алкил-(1-6C)алкоксикарбонил-(1-6C)алкиламино, N-(1-6C)-алкилкарбамоил-(1-6C)алкиламино, N-(1-6С)алкил-N-(1-6C)алкилкарбамоил- (1-6C)алкиламино, N-(1-6C)алкил-N,N-ди-[(1-6C)алкил]-карбамоил-(1-6C)алкиламино, N-(1-6C)алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-(1-6C)алкиламино-(2-6С)алкиламино, N-(1-6С)алкил-ди-[(1-6C)алкил]амино-(2-6С)алкиламино, галоген-(2-6С)алканоиламино, гидрокси-(2-6С)алканоиламино, (1-6C)алкокси-(2-6С)алканоиламино, циано-(2-6С)алканоиламино, карбокси-(2-6С)алканоиламино, (1-6С)алкоксикарбонил-(2 -6С)алканоиламино, карбамоил-(2-6С)алканоиламино, N-(1-6C)алкилкарбамоил-(2-6С)-алканоиламино, N,N-ди-[(1-6C)алкил]карбамоил-(2-6С)алканоиламино, амино-(2-6С)алканоиламино, (1-6C)алкиламино-(2-6С)-алканоиламино, ди-[(1-6C)алкил]амино-(2-6С)алканоиламино, арила, арил-(1-6C)алкила, арил-(1-6C)алкокси, арилокси, гетероарила, гетероарил-(1-6C)алкила, гетероарилокси, гетероарил-(1-6C)-алкокси, гетероциклила, гетероциклил-(1-6C)алкила, гетероциклилокси и гетероциклил-(1-6C)алкокси,
или Q замещен (1-3С)алкилендиоксигруппой;
и где любая арильная, гетероарильная или гетероциклильная группа в заместителе радикала Q может необязательно иметь 1 или 2 заместителя, выбранных из гидрокси, галогена, (1-6С)алкила, (1-6С)алкокси;
и где Q, если он является гетероциклильной группой или содержит гетероциклильную группу, или любая гетероциклильная группа в заместителе радикала Q может необязательно иметь 1 или 2 оксо или тиоксозаместителя;
где арил, когда Q является арильной группой или содержит арильную группу, или когда арил является заместителем радикала Q, или содержится в заместителе радикала Q, представляет собой фенил, инденил, инданил, нафтил, тетрагидронафтил или флуоренил;
где гетероарил, когда Q является гетероарильной группой или содержит гетероарильную группу, или когда гетероарил представляет заместитель радикала Q, или содержится в заместителе радикала Q, представляет собой ароматический 5- или 6-членный моноцикл, 9- или 10-членную бициклическую систему или 13- или 14-членную трициклическую систему, которые могут иметь до 5 гетероатомов, выбранных из кислорода, азота и серы;
и где гетероциклил, когда R1 и Q являются гетероциклильной группой или содержат гетероциклильную группу, или когда гетероциклил представляет заместитель радикала Q, или содержится в заместителе радикала Q, представляет собой неароматический насыщенный или частично насыщенный от 3- до 10-членный моноцикл или бициклическую систему, которые могут иметь до 5 гетероатомов, выбранных из кислорода, азота и серы;
или его фармацевтически приемлемая соль или in vivo расщепляемый сложный эфир,
за исключением 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она.
2. Производное амида формулы Ib
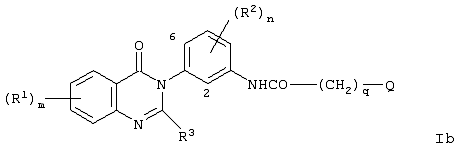
где m равно 0, 1, 2 или 3;
R1 является (1-6С)алкокси, N-(1-6С)алкил-ди[(1-6C)алкил]амино-(2-6С)-алкиламино,
или R1 является гетероциклилом, гетероциклил-(1-6C)алкилом, гетероциклилокси, гетероциклил-(1-6C)алкокси, гетероциклиламино, N-(1-6С)алкилгетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6C)-алкилгетероциклил-(1-6С)алкиламино, гетероциклилкарбониламино, гетероциклилсульфониламино, N-гетероциклилсульфамоилом, гетероциклил-(2-6С)алканоиламино, гетероциклил-(1-6C)алкокси-(1-6С)алкилом, гетероциклил-(1-6C)алкиламино-(1-6C)алкилом или N-(1-6С)алкилгетероциклил-(1-6C)алкиламино-(1-6C)алкилом,
и где любая гетероциклильная группа в заместителе R1 может необязательно иметь 1 или 2 заместителя, выбранных из галогена, (1-6С)алкила и (1-6С)алкокси,
n равно 0 или 1;
R2 является галогеном или (1-6С)алкилом;
R3 является водородом, галогеном, (1-6С)алкилом или (1-6С)алкокси;
q равно 0, 1, 2, 3 или 4; и
Q является арилом, арилокси, арил-(1-6С)алкокси, ариламино, N-(1-6C)алкил-ариламино, арил-(1-6С)алкиламино, N-(1-6С)алкиларил-(1-6С)алкиламино, (3-7С)циклоалкилом, гетероарилом, гетероарилокси, гетероарил-(1-6С)алкокси, гетероариламино, N-(1-6С)алкилгетероариламино, гетероарил-(1-6C)алкиламино, N-(1-6С)алкилгетероарил-(1-6C)алкиламино, гетероциклилом, гетероциклилокси, гетероциклил-(1-6С)алкокси, гетероциклиламино, N-(1-6C)алкилгетероциклиламино, гетероциклил-(1-6C)алкиламино, N-(1-6C)алкилгетероциклил-(1-6C)алкиламино,
и Q необязательно замещен 1, 2 или 3 заместителями, выбранными из гидрокси, галогена, трифторметила, циано, меркапто, нитро, амино, карбокси, карбамоила, формила, (1-6С)алкила, (2-6С)алкенила, (2-6С)алкинила, (1-6C)алкокси, (1-6С)алкилтио, (1-6C)алкилсульфинила, (1-6C)алкилсульфонила, (1-6C)алкиламино, ди-[(1-6C)алкил]амино, (1-6С)алкоксикарбонила, N-(1-6С)алкилкарбамоила, N,N-ди[(1-6С)алкил]карбамоила, (2-6С)алканоила, (2-6С)алканоилокси, (1-6C)алканоиламино, N-(1-6С)алкил-(1-6C)алканоиламино, N-(1-6C)алкилсульфамоила, N,N-ди-[(1-6C)алкил]сульфамоила, (1-6C)алкансульфониламино, N-(1-6С)алкил-(1-6C)алкансульфониламино, галоген-(1-6C)алкила, гидрокси-(1-6C)алкила, (1-6С)алкокси-(1-6С)алкила, циано-(1-6С)алкила, амино-(1-6С)алкила, (1-6С)алкиламино-(1-6С)алкила, ди-[(1 -6С)алкил]амино-(1-6С)алкила, карбокси-(1-6С)алкила, (1-6C)алкоксикарбонил-(1-6С)алкила, карбамоил-(1-6С)алкила, N-(1-6С)алкилкарбамоил-(1-6С)алкила, N,N-ди-[(1-6С)алкил]-карбамоил-(1-6С)алкила, галоген-(2-6С)алкокси, гидрокси-(2-6С)алкокси, (1-6С)алкокси-(2-6С)алкокси, циано-(1-6С)алкокси, карбокси-(1-6С)алкокси, (1-6С)алкоксикарбонил-(1-6С)алкокси, карбамоил-(1-6С)алкокси, N-(1-6C)алкилкарбамоил-(1-6С)алкокси, N,N-ди-[(1-6C)алкил]карбамоил-(1-6C)алкокси, амино-(2-6С)алкокси, (1-6C)алкиламино-(2-6С)алкокси, ди-[(1-6C)алкил]амино-(2-6С)-алкокси, галоген-(2-6С)алкиламино, гидрокси-(2-6С)алкиламино, (1-6C)алкокси-(2-6С)алкиламино, циано-(1-6C)алкиламино, карбокси-(1-6C)алкиламино, (1-6C)алкоксикарбонил-(1-6C)алкиламино, карбамоил-(1-6C)алкиламино, N-(1-6C)алкилкарбамоил-(1-6C)-алкиламино, N,N-ди-[(1-6C)алкил]карбамоил-(1-6C)алкиламино, амино-(2-6С)алкиламино, (1-6C)алкиламино-(2-6С)алкиламино, ди-[(1-6C)алкил]амино-(2-6С)алкиламино, N-(1-6С)алкилгалоген-(1-6С)алкиламино, N-(1-6C)алкилгидрокси-(2-6С)алкиламино, N-(1-6С)алкил-(1-6C)алкокси-(2-6С)алкиламино, N-(1-6С)алкилциано-(1-6С)алкиламино, N-(1-6C)алкилкарбокси-(1-6C)алкиламино, N-(1-6С)алкил-(1-6C)алкоксикарбонил-(1-6C)алкиламино, N-(1-6C)-алкилкарбамоил-(1-6C)алкиламино, N-(1-6С)алкил-N-(1-6C)алкилкарбамоил- (1-6C)алкиламино, N-(1-6C)алкил-N,N-ди-[(1-6C)алкил]-карбамоил-(1-6C)алкиламино, N-(1-6C)алкиламино-(2-6С)алкиламино, N-(1-6C)алкил-(1-6C)алкиламино-(2-6С)алкиламино, N-(1-6С)алкил-ди-[(1-6C)алкил]амино-(2-6С)алкиламино, галоген-(2-6С)алканоиламино, гидрокси-(2-6С)алканоиламино, (1-6C)алкокси-(2-6С)алканоиламино, циано-(2-6С)алканоиламино, карбокси-(2-6С)алканоиламино, (1-6С)алкоксикарбонил-(2-6С)алканоиламино, карбамоил-(2-6С)алканоиламино, N-(1-6C)алкилкарбамоил-(2-6С)-алканоиламино, N,N-ди-[(1-6C)алкил]карбамоил-(2-6С)алканоиламино, амино-(2-6С)алканоиламино, (1-6C)алкиламино-(2-6С)-алканоиламино, ди-[(1-6C)алкил]амино-(2-6С)алканоиламино, арила, арил-(1-6C)алкила, арил-(1-6C)алкокси, гетероарила, гетероарил-(1-6C)алкила, гетероарилокси, гетероциклила, гетероциклил-(1-6C)алкила и гетероциклилокси,
или Q замещен (1-3С)алкилендиоксигруппой,
и где любая арильная, гетероарильная или гетероциклильная группа в заместителе радикала Q может необязательно иметь 1 или 2 заместителя, выбранных из гидрокси, галогена, (1-6С)алкила, (1-6С)алкокси;
или его фармацевтически приемлемая соль или in vivo расщепляемый сложный эфир;
за исключением 3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она, 3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и 3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-З,4-дигидрохиназолин-4-она.
3. Производное амида формулы Ia по п.1, в котором Х является -NHCO- или -CONH-;
R3 является водородом, метилом или этилом; m равно 0, 1 или 2; R1 является метокси, этокси, N-(2-диметиламиноэтил)-N-метиламино, N-(2-диэтиламиноэтил)-N-метиламино, N-(3-диметиламинопропил)-N-метиламино, N-(3-диэтиламинопропил)-N-метиламино, 3-пирролинилом, пирролидинилом, пиперидинилом, гомопиперидинилом, морфолинилом, пиперазинилом, 4-метилпиперазинилом, 4-этилпиперазинилом, гомопиперазинилом, 4-метилгомопиперазинилом, 4-ацетилпиперазинилом, пирролидинилметилом, пиперидинилметилом, морфолинилметилом, пиперазинилметилом, 4-метилпиперазинилметилом, гомопиперазинилметилом, 4-метилгомопиперазинилметилом, 4-ацетилпиперазинилметилом, пирролидинилокси, 1-метилпирролидинилокси, пиперидинилокси, 1-метилпиперидинилокси, гомопиперидинилокси, 1-метилгомопиперидинилокси, 2-(пирролидинил)этокси, 3-(пирролидинил)пропокси, 2-(пиперидинил)этокси, 3-(пиперидинил)-пропокси, 2-(морфолинил)этокси, 3-(морфолинил)пропокси, 2-(пиперазинил)этокси, 3-(пиперазинил)пропокси, 2-(4-метилпиперазинил)этокси, 3-(4-метилпиперазинил)пропокси, 2-(4-ацетилпиперазинил)этокси, 3-(4-ацетилпиперазинил)пропокси, 3-диметиламинопропиламинометилом, 3-диметиламино-2,2-диметилпропиламинометилом, 2-(1-метилпирролидинилэтил)аминометилом, 3-пирролидинилпропиламинометилом, 2-морфолинилэтиламинометилом, 3-морфолинилпропиламинометилом, 2-пиперазинилэтиламинометилом, 3-(4-метилпиперазинилпропил)аминометилом, пиридилметокси, имидазолилметокси, тиазолилметокси и 2-метилтиазолилметокси; n равно 0 или 1; R2 является фтором, хлором, бромом, метилом или этилом; q равно 0; и Q является фенилом, инденилом, инданилом, тетрагидронафтилом, флуоренилом, фурилом, тиенилом, оксазолилом, изоксазолилом, имидазолилом, пиразолилом, тиазолилом, изотиазолилом, пиридилом, пиридазинилом, пиримидинилом, пиразинилом, бензофуранилом, индолилом, бензотиенилом, бензоксазолилом, бензимидазолилом, бензотиазолилом, индазолилом, бензофуразанилом, хинолилом, изохинолилом, хиназолинилом, хиноксалинилом, нафтиридинилом, карбазолилом, дибензофуранилом, дибензотиофенилом или ксантенилом, которые необязательно имеют 1 или 2 заместителя, выбранных из гидрокси, фтора, хлора, трифторметила, циано, амино, метила, этила, метокси, этокси, пропокси, изопропокси, циклопентокси, метилендиокси, метиламино, этиламино, диметиламино, диэтиламино, ацетамидо, пропионамидо, N-метилацетамидо, метансульфонамидо, N-метилметансульфонамидо, аминометила, метиламинометила, этиламинометила, диметиламинометила, диэтиламинометила, 2-гидроксиэтокси, 3-гидроксипропокси, 2-метоксиэтокси, 2-этоксиэтокси, 3-метоксипропокси, 3-этоксипропокси, 2-аминоэтокси, 3-аминопропокси, 2-метиламиноэтокси, 2-этиламиноэтокси, 3-метиламинопропокси, 3-этиламинопропокси, 2-диметиламиноэтокси, 2-диэтиламиноэтокси, 3-диметиламинопропокси, 3-диэтиламинопропокси, фенила, фурила, тиенила, пиридила, пиридилметила, пиридилметокси, азетидинила, 3-пирролинила, пирролидинила, пиперидинила, гомопиперидинила, морфолинила, пиперазинила, 4-метилпиперазинила, гомопиперазинила, 4-метилгомопиперазинила, 4-ацетилпиперазинила, пирролидинилметила, пиперидинилметила, морфолинилметила, пиперазинилметила, 4-метилпиперазинилметила, 4-ацетилпиперазинилметила, пирролидинилокси, 1-метилпирролидинилокси, пиперидинилокси, 1-метилпиперидинилокси, 2-(пирролидинил)этокси, 3-(пирролидинил)пропокси, 2-(пиперидинил)этокси, 3-(пиперидинил)пропокси, 2-(морфолинил)-этокси, 3-(морфолинил)пропокси, 2-(пиперазинил)этокси, 3-(пиперазинил)пропокси, 2-(4-метилпиперазинил)этокси, 3-(4-метилпиперазинил)пропокси, 2-(4-ацетилпиперазинил)этокси и 3-(4-ацетилпиперазинил)пропокси, и где любая фенильная, фурильная, тиенильная, пиридильная или гетероциклильная группа в заместителе радикала Q может необязательно иметь 1 или 2 заместителя, выбранных из фтора, хлора, метила и метокси; или его фармацевтически приемлемая соль.
4. Производное амида формулы Ib по п.2, в котором R3 является водородом или метилом; m равно 1 и R1 выбирают из пирролидин-1-ила, морфолино, пиперидино, пиперазин-1-ила, 4-метилпиперазин-1-ила, 4-этилпиперазин-1-ила, гомопиперазин-1-ила, 4-метилгомопиперазин-1-ила, пиперазин-1-илметила, 4-метилпиперазин-1-илметила, 4-метилгомопиперазин-1-илметила, морфолинометила, 3-аминопирролидин-1-илметила, 3-гидроксипирролидин-1-илметила, пирролидин-3-илокси, пиперидин-4-илокси, 2-пирролидин-1-илэтокси, 2-пиперидиноэтокси, 2-морфолиноэтокси, 3-диметиламинопропиламинометила, 3-диметиламино-2,2-диметилпропиламинометила, 2-(1-метилпирролидин-2-илэтил)аминометила, 3-пирролидин-1-илпропиламинометила, 2-морфолиноэтиламинометила, 3-морфолинопропиламинометила, 2-пиперазин-1-илэтиламинометила, 3-(4-метилпиперазин-1-илпропил)аминометила и 2-пиридилметокси; n равно 0 или 1; R2 является метилом; q равно 0 и Q является 3-пиридилом или 4-пиридилом, которые имеют заместитель, выбранный из пирролидин-1-ила, морфолино, пиперидино, пиперазин-1-ила и 4-метилпиперазин-1-ила; или его фармацевтически приемлемая соль.
5. Производное амида формулы Ib по п. 2, в котором R3 является водородом или метилом; m равно 1 и R1 выбирают из 3-пирролин-1-ила, пирролидин-1-ила, морфолино, пиперидино, гомопиперидин-1-ила, пиперазин-1-ила, 4-метилпиперазин-1-ила, 4-этилпиперазин-1-ила, гомопиперазин-1-ила, 4-метилгомопиперазин-1-ила, пиперазин-1-илметила, 4-метилпиперазин-1-илметила, гомопиперазин-1-илметила, 4-метилгомопиперазин-1-илметила, морфолинометила, 3-аминопирролидин-1-илметила, 3-гидроксипирролидин-1-илметила, пирролидин-3-илокси, N-метилпирролидин-3-илокси, пиперидин-4-илокси, N-метилпиперидин-4-илокси, гомопиперидин-4-илокси, N-метилгомопиперидин-4-илокси, 2-пирролидин-1-илэтокси, 2-пиперидиноэтокси, 2-морфолиноэтокси, 3-диметиламинопропиламинометила, 3-диметиламино-2,2-диметилпропиламинометила, 2-(1-метилпирролидин-2-илэтил)аминометила, 3-пирролидин-1-ил-пропиламинометила, 2-морфолиноэтиламинометила, 3-морфолинопропиламинометила, 2-пиперазин-1-илэтиламинометила, 3-(4-метилпиперазин-1-илпропил)аминометила, 2-пиридилметокси, 4-тиазолилметокси и 2-метилтиазол-4-илметокси; n равно 0 или 1; R2 является метилом; q равно 0 и Q является фенилом, который имеет 1 или 2 заместителя, выбранных из фтора, хлора, трифторметила, метокси, циклопентилокси, ацетамидо, N-метилметансульфонамидо, 2-фурила, азетидин-1-ила, 3-пирролин-1-ила, пирролидин-1-ила, морфолино, пиперидино, гомопиперидин-1-ила, пиперазин-1-ила, гомопиперазин-1-ила, 4-метилпиперазин-1-ила и 4-метилгомопиперазин-1-ила, или Q является 1-флуоренилом или 4-дибензофуранилом, или Q является 3-пиридилом или 4-пиридилом, которые имеют заместитель, выбранный из азетидин-1-ила, 3-пирролин-1-ила, пирролидин-1-ила, морфолино, пиперидино, гомопиперидино, пиперазин-1-ила, гомопиперазин-1-ила, 4-метилпиперазин-1-ила и 4-метилгомопиперазин-1-ила; или его фармацевтически приемлемая соль.
6. Производное амида формулы Ib по п. 2, в котором R3 является водородом или метилом; m равно 1 и R1 является 4-метилпиперазин-1-илом, 4-метилгомопиперазин-1-илом или N-(3-диметиламинопропил)-N-метиламино; n равно 0 или 1; R2 является 6-метилом; q равно 0 и Q является 2-пирролидин-1-илпирид-4-илом, 2-(3-пирролин-1-ил)пирид-4-илом, 2-пиперидинопирид-4-илом, 2-морфолинопирид-4-илом, 1-флуоренилом, дибензофуран-4-илом, 3-ацетамидофенилом или 3-(2-фурил)фенилом; или его фармацевтически приемлемая соль.
7. Производное амида формулы Ib по п.2, в котором R3 является водородом; m равно 1 и R1 является пиперазин-1-илом, 4-метилпиперазин-1-илом, 4-метилгомопиперазин-1-илом или N-(3-диметиламинопропил)-N-метиламино; n равно 0 или 1; R2 является 6-метилом или 6-фтором; q равно 0 и Q является 2-азетидин-1-илпирид-4-илом, 2-пирролидин-1-илпирид-4-илом, 2-(3-пирролин-1-ил)пирид-4-илом, 2-пиперидинопирид-4-илом, 2-морфолинопирид-4-илом, 1-флуоренилом, дибензофуран-4-илом, 5-(4-хлорфенил)фуран-2-илом, 4-(4-хлорфенил)-тиен-2-илом, 2-метоксифенилом, 3-этоксифенилом, 3-(1,1,2,2-тетрафторэтокси)фенилом, 3,4-метилендиоксифенилом, 3-ацетамидофенилом, 3-(4-фторфенил)фенилом, 3-(2-фурил)фенилом, 3-фтор-5-пирролидин-1-илфенилом, 3-фтор-5-пиперидинофенилом, 3-фтор-5-морфолинофенилом или 3-морфолино-5-трифторметилфенилом; или его фармацевтически приемлемая соль.
8. Производное амида формулы Ia по п.1, выбранное из группы, включающей 6-[N-(3-диметиламинопропил)-N-метиламино]-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
6-[N-(3-диметиламинопропил)-N-метиламино]-2-метил-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
6-[N-(3-диметиламинопропил)-N-метиламино]-3-[5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
6-(4-метилпиперазин-1-ил)-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
8-[N-(3-диметиламинопропил)-N-метиламино]-3-[2-метил-5-(2-морфолинопирид-4-илкарбониламино)фенил]-3,4-дигидрохиназолин-4-он,
3-[2-метил-5-(2-пирролидин-1-илпирид-4-илкарбониламино)-фенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-[2-метил-5-(2-пиперидинопирид-4-илкарбониламино)-фенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-{2-метил-5-[2-(3-пирролин-1-ил)пирид-4-илкарбониламино]-фенил}-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-[5-дибензофуран-4-илкарбониламино-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
3-{5-[3-(2-фурил)бензамидо]-2-метилфенил}-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он и
3-[5-(3-ацетамидобензамидо)-2-метилфенил]-6-(4-метилпиперазин-1-ил)-3,4-дигидрохиназолин-4-он,
или его фармацевтически приемлемая соль.
9. Способ получения производного амида формулы Ia или Ib, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира по п.1 или 2, который включает
взаимодействие N-фенил-2-аминобензамида формулы II
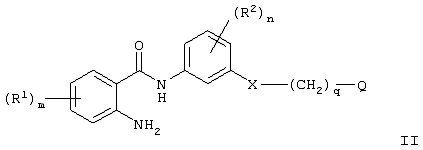
с карбоновой кислотой формулы III или ее реакционноспособным производным
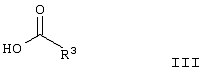
где X, R1, R2, R3, m, n, q и Q имеют значения, определенные в п.1, и где любая функциональная группа защищена при необходимости, и:
(i) удаление любых защитных групп и
(ii) необязательно образование или фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира.
10. Способ получения производного амида формулы Ia или Ib, или его фармацевтически приемлемой соли, или in vivo расщепляемого сложного эфира по п.1 или 2, который включает
взаимодействие анилина формулы Х
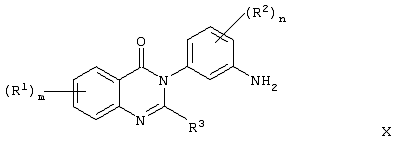
с карбоновой кислотой формулы VI или ее реакционноспособным производным,
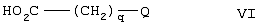
в условиях образования амидной связи,
где R1, R2, R3, m, n, q и Q имеют значения, определенные в п.1, и где любая функциональная группа защищена при необходимости, и
(i) удаление любых защитных групп и
(ii) необязательно образование фармацевтически приемлемой соли или in vivo расщепляемого сложного эфира.
11. Фармацевтическая композиция, ингибирующая продуцирование цитокинов посредством ингибирования действия фермента р38 киназы, которая содержит производное амида формулы Ia или Ib, или его фармацевтически приемлемую соль, или его in vivo расщепляемый сложный эфир, как определено в п.1 или 2, или производное амида, выбранное из
3-(5-бензамидо-2-метилфенил)-2-метил-3,4-дигидрохиназолин-4-она,
3-[5-(4-метилбензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она и
3-[5-(4-метоксибензамидо)-2-метилфенил]-2-метил-3,4-дигидрохиназолин-4-она,
в сочетании с фармацевтически приемлемым разбавителем или носителем.
12. Производное амида формулы Ia или Ib, или его фармацевтически приемлемая соль, или его in vivo расщепляемый сложный эфир, как определено в п.1 или 2, обладающие свойствами ингибитора продуцирования цитокинов посредством ингибирования действия фермента р38 киназы.
13. Способ ингибирования продуцирования цитокинов TNF посредством ингибирования действия фермента р38 киназы, который включает введение теплокровному животному эффективного количества производного амида формулы Ia или Ib, или его фармацевтически приемлемой соли, или его in vivo расщепляемого сложного эфира, как определено в п.1 или 2. посредством ингибирования действия фермента р38 киназы, который включает введение теплокровному животному эффективного количества производного амида формулы Ia или Ib, или его фармацевтически приемлемой соли, или его in vivo расщепляемого сложного эфира, как определено в п.1 или 2.
Приоритеты:
17.03.1999 - пп.2, 4, 8, 9-12;
11.11.1999 - пп.1, 3, 5, 6. |
|
|
|