
СПИСОК ПАТЕНТОВ С УПОМИНАНИЕМ ГИАЛУРОНОВОЙ КИСЛОТЫ
-
- 2017751 Способ получения гиалурона
- 2192150 БАД для профилактики йодной недостаточности
- 2112542 Препарат для лечения патологий соединительных тканей
- 2225206 Препарат для лечения рака молочной железы
- 2299733 Лечение опорно-двигательного аппарата
- 2299732 Способ лечения глаукомы
- 2299726 Противоинфекционная губная помада
- 2299725 Косметическое средство для ухода за кожей
- 2198878 Ароматическое соединение
- 2198702 Способ подготовки трофических язв к аутодермапластике
- 2198653 Вагинальные суппозитории
- 2197946 Композиция для ухода за волосами
- 2197923 Фармацевтическая композиция для лечения отеков роговицы
- 2298410 Биотрансплантант и способ лечения ревматических и аутоиммунных заболеваний
- 2197501 Фотоотверженный гель на основе сшитой гиалуроновой кислоты
- 2197228 Твердые лекарственные формы
- 2197222 Водная компазиция для ухода за волосами, лица и тела
- 2297425 Полипептиды
- 2297240 Композиция с гиалуроновой кислотой
- 2297230 Фармацевтическая компазиция с ксантоновой смолой
- 2196588 Глазные капли
- 2195955 Применение биологически активных веществ
- 2195926 Дерматологические композиции
- 2295954 Микрочастицы для доставки нуклеиновых кислот
- 2295951 Косметика для ухода за кожей лица и век
- 2195262 Фармакологическое средство на основе гиалуроновой кислоты
- 2194512 Способ профилактики и коррекции процесса старения кожи
- 2194478 Лечение экземы
- 2294716 Расширяемый стент
- 2194055 Сшитые сополимеры
- 2099350 Ассоциаты депротонированной гиалуроновой кислоты
- 2293557 Средство для лечения кожи и слизистых
- 2292878 Приготовление микроцастиц, содержащих метопропол
- 2292746 БАД
- 2192256 Защита кишечника
- 2191782 Получение модифицированной гиалуроновой кислоты
- 2292219 Паратиреоидный гормон человека
- 2291686 Микроцастицы
- 2191000 Косметическая маска
- 2290921 Фармацевтические и косметические средства против старения кожи
- 2290900 Модифицированный биоматериал для использования в офтальмологии
- 2290899 Получение биоматерьяла
- 2290397 Новые инданилиденовые соединения
- 2290186 Лечение сирингомиелии
- 2288702 Иррингационный раствор для офтальмологии
- 2288699 Гель для лечения стоматологических заболеваний
- 2188011 Активирующая остеогенез фармацевтическая композиция
- 2187327 Средство с антисептиком
- 2187325 Средство с радиопротекторным действием
- 2287330 Композиции миноксидила
- 2186786 Способ получения гиалуроновой кислоты
- 2186593 Лечение раненого процесса кожи
- 2286801 Очищение воды
- 2286781 Лечение ожогов пищевода у детей
- 2286764 Средство лечения воспалений полости рта
- 2185840 Лечение инфекционных заболеваний
- 2286151 Альфа-2-Дельта-Лиганда
- 2185149 Ранозаживляющий гель
- 2285527 Лечение ИЛ-6 заболеваний
- 2184448 Раствор хранения роговицы, включающий гиалуроновую кислоту
- 2090179 Крем для кожи
- 2183961 Способ лечения кожи
- 2284331 Соли алифотических аминов
- 2284187 Производные амида
- 2089191 Снизить внутрение давление
- 2283320 Получение гликозаминогликанов
- 2283129 Лечение опухолей
- 2283098 Косметические средства с Q
- 2182574 Ароматические соединения
- 2088257 Средство с гипохолестеролемическим действием
- 2088218 Состав для гигиенических салфеток
- 2088206 Способ получения препарата, создающего исскуственный загар
- 2282462 Противомикробные средства
- 2182008 Интровагинальная компазиция
- 2181999 Препарат с отсроченным высвобождением
- 2181998 Новые композиции липидов
- 2181995 Лечение болевого синдрома
- 2181295 Вирионная вакцина
- 2087144 Витамин Е
- 2379336 Способ стирки
- 2379052 Вакцинация
- 2180855Композиция в виде ионного комплекса
- 2379025 Противоинфекционный гель
- 2180825 Лечение травм роговицы
- 2281082 Способ коррекции эстетических и возрастных проблем кожи
- 2180576 Биоактивная добавка для косметических средств
- 2280459 Средство для изменения скорости роста или репродукции клеток
- 2179981 Соли переходного металла
- 2378010 Жидкие вакцины
- 2378008 Комбинированные вакцины
- 2378007 Анаболическое средство
- 2377973 Растительные экстракты
- 2280041 Способ получения водорастворимых комплексов гиалурил
- 2280038 Биополимеры
- 2323733 Йодный обмен
- 2377260 Гель
- 2178693 Противовирусное средство на основе гиалуроновой кислоты
- 2178692 Облегчающие зуд косметическое средство
- 2377022 Гемостатические спреи
- 2376982 Увлажняющая сыворотка для лица
- 2376974 Трансдермальный гель для лица
- 2362784 Гипо-и гиперацетилированные менингокковые капсульные сахариды
- 2177789 Устройство для доставки лекарства к шейке матки
- 2277954 Крем для лица омолаживающий
- 2376378 Способ получения метионина
- 2177332 Биоматериал для предотвращения послеоперационных спаек, с производной гиалуроновой кислотой
- 2177310 Способ получения таблеток
- 2376011 Средство для позвоночника
- 2277410 Косметическое средство
- 2323748 Медицинская повязка
- 2276998 Гидрогелевые композиции
- 2082416 Способ получения препарата с коллагенном из животного сырья
- 2375081 Адсорбирующее изделие
- 2375049 Охлаждающий пластырь
- 2346049 Способ получения гиалурона
- 2275913 Фармацевтические средства
- 2174985 Полисахарид с антиоксидантом
- 2373957 Носитель для лекарственных средств и биологически активных веществ
- 2373941 Способ коррекции возрастных и патологических изменений кожных покров
- 2174845 Композиции и способы доставки генетического материала
- 2174830 Средство для укрепления волос
- 2373769 Синбиотическая композиция
- 2274472 Лечение апорно-двигательного аппарата и болевых синдромов
- 2372929 Профилактическая композиция на основе веществ фенольной природы в липосомной форме
- 2173563 Способ нанесения на поверхность предметов покрытия на основе гиалуроновой кислоты, её производных и полусинтетических полимеров
- 2079304 фармацевтическая композиция, обладающая иммуносупрессорной и антимикробной активностью
- 2273645 Полипептид ожирения
- 2173154 Фракция кератансульфатолигосахаридов и содержащий ее фармацевтический препарат
- 2173136 Грязная мазь
- 2173128 Способ хирургического лечения центральных разрывов сечатки
- 2078561 Косметическое средство предотвращающее старение кожи
- 2172490 Способ прогнозирования воспалительных заболеваний молочной железы при эндопластике
- 2272645 Способ лечения ЦМВ-Инфекции у детей раннего возроста
- 2272636 Фармацевтическая композиция для местного лечения воспаления
- 2272635 Фармацевтически активная субстанция для офтальмологии
- 2272599 Биоматерьял для стабилизации прогрессирующей миопии "Коллаплант"
- 2172168 Средство для заживления ран на основе гиалуроновой кислоты
- 2371172 Фармацевтическая композиция для лечения нервной системы на основе стефаглабрина
- 2171470 Способ прогнозирования послеоперационной трансформации доброкачественных опухолей нервной системы
- 2077317 Состав для ванн
- 2271213 Комбинированные композиции, содержащие экстракты из растений и морских животных
- 2076872 Способ получения окрашенной гиалуроновой кислоты
- 2076671 Раствор для защиты роговицы
- 2370281 Конъюгаты гидроксиалкилкрахмал
- 2370275 Способ лечения (коррекции) косметических и возрастных дефектов кожи
- 2370258 Фармацевтическая композиция для парентальной доставки в форме лиофилизата
- 2270023 Способ экстракции и очистки протеогликана хрящего типа (варианты)
- 2369408 Гемостатическая композиция, включающая гиалуроновую кислоту
- 2369387 Фармацевтическая композиция для лечения нервной системы
- 2369379 Нетаблитированные жевательные формы для индивидуального введения
- 2169136 Производное коричной кислоты
- 70792 Медицинский аппликатор
- 20741717 Способ стабилизации аскорбиновой кислоты
- 2074712 Способ получения препарата, препятствующего преждевременной эякуляции
- 2367954 Способ прогнозирования развития кожной патологии у женщин с синдромом склерополикистозных яичников (СПКЯ)
- 2268075 Устройство для электрокинетической доставки
- 2268052 Средство для лечения воспалительных и дегенеративных заболеваний суставов
- 2167649 Способ получения твердой дисперсии умеренного водорастворимого лекарственного вещества
- 2167647 Гель для бритья
- 2073520 Лечение урологических инфекций
- 2367476 Биопластический материал
- 2367475 Мембрана для использования при направленной регенерации тканей
- 2367469 Фармацевтическая композиция на основе лизоамидазы
- 2367456 Фармацевтическая композиция обладающая антибактериальным и некролитическим действием
- 2367455 Фармацевтическая композиция обладающая некролитическим и антибактериальным действием
- 2267324 Применение антиадгезивных углеводов, препарат для уменьшения и /или блокирования адгезии патогенных веществ
- 2166934 Композиции включающие биологический агент
- 2166510 Псевдодипептиды
- 2366460 Композиции, имеющие высокую противовирусную и антибактериальную активность
- 2360901 Производные феноксиуксусной кислоты
- 2165749 Способ восстановления эндотелия роговицы
- 2265441 Способ укрепления склеры
- 2365382 Композиции и способы для регуляции развития сосудов
- 2070879 Соли гликозаминогликанов
- 2164914 Циклические и гетероциклические N - замещенные - иминогидроксамовые карбоновые кислоты
- 2264627 Хламидийный конъюктивит
- 2364399 Фармацевтический препарат на основе стефаглабрина
- 2264230 Препарат с замедленным высвобождением активного вещества
- 2363497 Фармацевтические композиции
- 2363496 Способ увеличения объема мягких тканей
- 2363473 Способ антифлогистической активации в эксперементе
- 2363461 Фармацевтический препарат на основе сигетина
- 2363459 Средства для введения в роговицу глаз для предотвращения офтальмологических нарушений
- 2363448 Фармацевтические композиции
- 2163123 Глазные капли
- 2162687 Усовершенствованнная лекарственная форма индуктора интерферана
- 2162343 Биосовместимый полимерный материал и способ его получения
- 2162327 Лечение рака
- 2067841 Способ получения ароматизатора
- 2161478 Способ консервированого лечения гонартроза
- 2361617 Вольфрамовые частицы в качестве рентгеноконтрастных веществ
- 2361552 Способы и устройства для дренирования жидкостей и понижения внутриглазного давления
- 2066996 Способ изготовления пленочного материала для офтальмохирургии
- 2361417 Корм с глюкозамином и экстрактом ивы для профилактики артроза у животных
- 2161002 Пищевой общеукрепляющий лечебно-профилактический продукт из хрящевой ткани акул
- 2360928 Комплексная матрица для медико-биологического применения
- 2160574 Способ лечения глаукомы
- 2360688 Способ лечения повреждений переферических нервов
- 2360670 Фармацевтическая композиция при климактерических расстройствах
- 2360646 Эндолюминальный протез
- 2260445 Способ усовершенствования транспортировки через легко прспосабливаемый полупроницаемый барьер
- 2260007 Производные амида
- 2359975 Способ получения модифицированных арабиногалактанов
- 2359974 Антигенные Пептиды
- 2159775 Псевдопептидный продукт
- 2259833 Фармацевтическая композиция для лечения роговицы глаза
- 2259816 Ранозаживляющее средство
- 2259815 Способ коррекции возрастных изменений, связанных с процессами старения кожи
- 2359706 Способ сохранения офтальмологических растворов
- 2359704 Антисептическое средство
- 2359662 Микрокапсулы
- 2159253 Катионные полимеры
- 2159111 Средство для ухода за кожей лица
- 2159105 Композиция для защиты кожи от опасных химических веществ Получение
- 2158593 Биосовместимый водный раствор
- 2358728 Способ лечения и предупреждения потери костной ткани
- 2258517 Способ хирургического лечения травмотических повреждений селезенки пленкой на основе гиалуроновой кислоты
- 2357968 Кристалические формы производной имидазола
- 2357957 Ингибиторы P38 и их применение
- 2157647 Пищевая добавка и ее получение
- 2357758 Препараты для чрескожной и чересслизистой добавки
- 2063244 Способ стабилизации растворов
- 2063140 Способ получения препарата для консервирования мяса
- 2157381 Способ получения гиалуроновой кислоты
- 2257198 Композиции микроцастиц
- 2356909 Белковый комплекс
- 2356570 Косметическая композиция
- 2256434 Способ закрытия перфорации барабанной перепонки
- 2356520 Способ лечения постконтузионного повреждения сечатки глаза
- 2156133 Гель
- 2255945 Полимерная композиция
- 2355761 Средства повторной дифференцировки
- 2061043 Способ повышения устойчивости урокиназы к нагреванию
- 2061005 Способ получения красителей для гистологических исследований
- 2355420 Зубная паста
- 2355385 Композиции пролонгированного действия с контролируемым высвобождением
- 2355240 Способ получения пищевого препарата хондропротекторного действия
- 2155057 Пихтово репейный бальзам
- 2354409 Способ производства высвобождающих лекарственные средчтва медицинских устройств
- 2254145 Раневое покрытие на основе коллаген-хитозанового комплекса
- 2254133 Лечение и профилактика ВИЧ-инфекции у человека
- 2253439 Фармацевтическая композиция для защиты и улучшения оптических свойств роговици при проведении эндовитреальных вмешательств
- 2253437 Способ омоложения кожи
- 2153352 Фармацевтическая композиция обладающая ранозаживляющим и противовоспалительным действием
- 2353354 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2252787 Способ получения искусственной матрицы кожи
- 2252767 Способ нормализации иммунобиохимического гомеостаза коров в предродовом и послеродовом периодах
- 2352583 Фармацевтическая композиция содержащая Fc-область иммуноглобулина в качестве носителя
- 2152403 Модифицированные полисахариды
- 2352356 Иммуногенная композиция
- 2352342 Исскусственный физиологический солевый раствор Способ его получения
- 2352330 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2352323 Фармацевтический препарат с модифицированным высвобождением
- 2152027 Способ подготовки ткани мозга для определения гликозаминогликанов
- 2251842 Интектицидный состав для борьбы с личинками оводов
- 2151580 Способ активации пролиферации эндотелия роговицы
- 2351648 Дифференцировка стромальных клеток, полученных из жировой ткани, в эндокринные клетки поджелудочной железы и их использование
- 2351595 N - гидроксиформамидные соединения в качестве ингибиторов металлопротеина
- 2251411 Косметическое средство в лиофилизированной фармацевтической форме
- 2251405 Косметика...ее композиции для косметических препаратов
- 2251367 Средство со сшитой гиалуроновой кислотой для наращивания тканей
- 2351359 Косметика для профилактики и лечения избыточной массы тела
- 2351322 Препарат на основе низкомолекулярного индуктора интерферона
- 2351153 Диета при остеортрите собак
- 2350958 Способ определения групповой принадлежности синовальной жидкости
- 2350625 Производные гиалуроновой кислоты с пониженной биодеградируемостью
- 2150266 Крем после бритья
- 2350354 Фармацевтическое средство содержащие антагонист и фактор некроза
- 2350340 Способ коррекции процессов регенерации
- 2350309 Способ лечения избыточной массы тела с помощью рефлексотерапии
- 2250047 Профилактический продукт из хрящевой ткани гидробионтов
- 2249467 Медицинский матерьял и изделия на его основе
- 2055079 Способ получения препарата гиалуроновой кислоты
- 2349599 Биоадгезив мидии
- 2054903 Способ лечения коллагеноза у бычков на откорме
- 2249210 Способ прогнозирования предрасположенности к развитию и тяжести течения деформирующего остеоартроза коленного сустава у взрослых
- 2349339 Средство для соединительной ткани
- 2148988 Человеческий интерферона
- 2148399 Лечение атеросклероза
- 2148396 Способ определения активного вещества в дифильных мазевых основах
- 2148375 Способ диагностики близорукости
- 2348415 Способ противоспаечной терапии после хирургического вмешательства
- 2348400 Препарат на основе низкомолекулярного индуктора интерферона
- 2348386 Способ непроникающего хирургического лечения первичной открытоугольной глаукомы
- 2248213 Лечение Галактозидальной А недостаточности
- 2347586 Микрофлюидизированные эмульсии типа "масло в воде" и вакцинные средства
- 2147243 Контрастное средство
- 2146526 Лечебный препарат дисбактериоза и урогенитальных инфекций
- 2146148 Терапевтическое применение фактора роста кератиноцитов (ФРК)
- 2146139 Способ повышения активности макрофагов и комбинации для его осуществления
- 2346277 Способ диагностики специфического синовита
- 2345793 Ультразвуковые контрастные вещества и их получение
- 2345782 Терапевтические комбинации на основе PORIFERA для лечения и предотвращения кожных заболеваний
- 2245131 Способ коррекции косметических недостатков кожи
- 2245130 Способ активации восстановительных процессов в коже
- 2144833 Хондроитиназа
- 2344809 Получение твердых дозированных форм с использованием сшитого нетермопластичного носителя
- 2244540 Косметический гель для ухода за кожей лица
- 2244536 Способ лечения дегенеративно-дистрофических заболеваний тазобедренного сустава
- 2344167 Хмелевый экстракт
- 2143884 Агент регулирования дифференциации клеток кожи, культурная среда для клеток или тканей и способ регулирования дифференциации клеток кожи
- 2343932 Способ получения обладающих пониженной растворимостью в воде пленночных материалов
- 2343903 Устройство доставки лекарств для контролируемого введения препаратов
- 2048817 Способ получения материала для лечения ожогов и гнойно - некронических ран
- 2048803 Гидратантный крем
- 2242974 Средства и способы лечения воспалительных заболнваний
- 2142816 Способ получения антигерпетической вакцины
- 2342923 Средство для обработки рук с увлажняющим эффектом
- 2142781 Косметика для макияжа ресниц и бровей и агент ингирирующий рост микроорганизмов в косметических средствах
- 2242251 Трансплантируемые стенты с биоактивными покрытиями
- 2142257 Способ обработки глазных имплантантов и контакных линз
- 2342389 Мононатриевая соль
- 2342107 Способ устранения западения верхнего века при анофтальме
- 2141828 Средство, пролонгирующее эффективность чесночного порошка
- 2241489 Косметическое средство матриксных протеинов для залечивания ран
- 2241443 Средство для лечения герпеса
- 2241414 Способ получения протезов кровеносных сосудов
- 2341539 Гидрогель
- 2141324 Регулятор скорости воздействия препарата для инъекций
- 2141312 Косметическое средство для ухода за кожей лица
- 2341296 Средства и способы покрытия медицинских имплантантов
- 2341272 Средство для неспецифической иммунотерапии
- 2341266 Стенты с нанесенным покрытием содержащим N - (5-(4-(4-
- 2341257 Иммуномодулирующее средство
- 2341255 Средство для лечения климактерических расстройств
- 2240821 Способ лечения урологических инфекций
- 2140786 Способ лечения лишая
- 2140243 Способ хирургического лечения диабетической ретинопатии и отслоек сечатной оболочки
- 2240140 Медицинская многослойная повязка и изделия на ее основе
- 2240135 Культура клеток, содержащая клетки - предшественники остеонегеза, имплантант на ее основе и его использование для восстановления целостности кости
- 2240123 Экзогенные биологически активные коньюгирующие вещества
- 2139886 Фотоотвержаемое производное гликозаминогликата, сшитое производное гликозаминогликата и способы их получения, способ предотвращения клеточной и тканевой адгезии
- 2139729 Вакцина. Способ стимулирования иммунной системы
- 2339386 Средство обладающее радио - и химиозащитным действием
- 2339369 Лечение офтальмологических нарушений с использованием мочевины и ее производных
- 2139041 Гидратантный регенерирующий крем и способ его получения
- 2139039 Косметический суперкрем для ухода за кожей
- 2139017 Способ получения боисовместимого материала
- 2138503 Производные камптотецина, способы их получения, уникальное средство
- 2338556 Средство содержащие антагонист Р2Х - рецептора и нестероидное противоспалительное лекарственное средство
- 2338514 Косметическое средство для профилактики старения кожи
- 2138297 Медицинские устройства, подверженные вызываемому разложению
- 2138295 Покрытие для ран
- 2337906 Ингибиторы цитозольной фосфолипазы А2 Применение физиологически допустимого корпускулярного ферримагнитного или ферромагнитного материала. Способ формирования магнитометрического изображения
- 2137501 Устройство формирования изображения
- 2137477 Способ лечения заболеваний характеризующихся аутоиммунной агрессией
- 2137467 Крем для кожи лица и тела
- 2137449 Способ коррекции дефектов преломления в глазу млекопитающего
- 2137402 Пищевая Добавка БАД
- 2336899 Способ стимуляции миелопоэза
- 2336862 Способ получения раствора для лечения роговицы
- 2336830 Способ восстановления костных структур челюсти
- 2136696 Новый полипептид и средство против ВИЧ - Инфекции
- 2336092 Биоадгезивное средство, по существу свободное от воды
- 2336089 Средство и способ лечения заболеваний периодонтальных и пульпы
- 2336074 Средства и способы лечения заднего сегмента глаза
- 2235548 Ранозаживляющее средство
- 2135186 Способ лечения рефлекторных синдромов при остеохондрозе
- 2234945 Стабилизатор водного раствора и водосодержащего сырья
- 2334762 Растворимая ассоциативная карбоксиметилцеллюлоза
- 2234514 Макропористые хитозановые гранулы и способ их получения. Способ культивирования клеток
- 2133615 Средство для лечения неврологических заболеваний
- 2233164 Способ профилактики развития послеоперационных спаек брюшной полости
- 2133127 Неткатный материал, способ его получения и способ лечения
- 2333223 Альдегидные производные сиаловой кислоты и средства на их основе
- 2333007 Полипептидные вакцины для широкой защиты против рядов поколений менингококов с повышенной вирулентностью
- 2332985 Дозированные формы анестезирующих средств с длительным высвобождением для обезболивания
- 2132677 Косметическая маска
- 38603 Пленочный аппликатор
- 2232594 Средство содержащие ингибирующие остеокластогенез фактор и полисахарид
- 2332238 Средство для прокладок, раневых повязок и других изделий, контактирующих с кожей
- 2331668 Стромальные клетки, получение из жировой ткани, для заживления дефектов роговицы и внутриглазных дефектов и их использование
- 2331438 Альфа - 2 - Дельта Лигант для лечения симптомов нижних мочевыводящих путей
- 2331411Электропряденые аморфные фармоцевтические средства
- 2331367 Способ профилактики образования спаек и их рецидива
- 2130767 Масло в воде для получения косметических и дерматологических средств, способ косметической обработки
- 2230752 Поперечносшитые гиалуроновые кислоты и их применение в медицине
- 2230558 Способ восстановления и сохранения здоровья скмьи
- 2230550 Средства длительного высвобождения, способ их получения и применения
- 2230458 Поддержания здоровья суставов
- 2330290 Способ определения состояния метаболических процессов в ткани суставного хряща
- 2230073 Способ поперечного сшивания карбоксилированных полисахаридов
- 2329059 Способ лечения полипозного риносинусита
- 2329037 Комбинированная терапия для лечения иммуновоспалительных заболеваний
- 2128666 Гиалуроновая кислота и ее соли, способ очистки гиалуроновой кислоты, способ получения гиалуроновой кислоты. Фармацевтический препарат с гиалуроновой кислотой и средства с гиалуроновой кислотой используемые в офтальмологии
- 2328740 Способ экспресс - оценки действия зубных паст
- 2128502 Косметический гель
- 2328272 Суппозитории индуктора интерферона
- 2328268 Косметика содержащая амфолитный сополимер
- 2128057 Композиционная мембрана, способ ее получения и способ направленной регенерации тканей с ее применением
- 2128055 Средство замедленного освобождения и способ его получения
- 2128049 Свечи
- 2227743 Полипептидные варианты с повышенной гепаринсвязывающей способностью
- 2326893 Ковалентное и нековалентное сшивание гидрофильных полимеров
- 2326697 Новый перевязочный материал для быстрого заживления раневой поверхности кожи
- 2126264 Фармацевтическое средство с гиалуроновой кислотой
- 2326137 Способ получения содержащих альгинат пористых формованных изделий
- 2325902 Способ выделения гликозаминогликанов из минерализованной соединительной ткани
- 2225195 Репелленты против насекомых
- 2325193 Сосудистый стент
- 2325184 Улучшенные везикулы наружной мембраны бактерий
- 2325153 Многокомпонентная фармацевтическая дозированная форма
- 2325152 Удерживаемая в желудке система регулируемой доставки лекарственного средства
- 2029955 Способ предоперационного определения помутнения задней капсулы хрусталика при экстракции катаракты
- 2324688 Производные бисбензизоселеназолонила с противоопухолевым, противовоспалительным и антитромбоническим действием
- 2323017 Устройство и способ контролируемый доставки активных веществ в кожу
- 2323011 Содержащий Коллаген I и Коллаген II способный к рассасыванию внеклеточный матрикс, предназначенный для реконструирования хряща
- 2322955 Способ изготовления имплантанта для пластики дефектов хрящевой ткани
- 2322454 Антитело против CCR5
- 2322263 Система продолжительного высвобождения растворимого лекарственного средства
- 2221561 Витамин Е и его сложные эфиры
- 2321634 Гены участвующие в метаболизме углерода и продуцировании энергии
- 2321597 Биоматерьял, способ его приготовления и его применение, медицинское средство, имплантант и вкладыш
- 2121340 Средство для похудения
- 2220737 Средство для улучшения состояния опорно-двигательного аппарата
- 2220729 Гель используемый в стоматологии
- 2320720 Способ культивирования фибропластов для заместительной терапии
- 2320378 Накожный аппликатор
- 2320369 Средства, содержащие Альфа - 2 - Дельта Лиганды и ингибиторы обратного захвата серотонина/норадреналина
- 2320362 Местные фармацевтические средства, содержащие проантоцианидины, для лечения дерматитов
- 2320322 Биоадгезивная доставка лекарств
- 2320318 Чувствительное к температуре изменяющие состояние средство гидрогеля
- 2025120 Способ получения препарата, содержащего Фактор /G-CSF/, стимулирующий рост колоний гранулоцитов
- 2319490 Средство для введения железа при лечении синдрома беспокойных ног
- 25995 Содержащее адгезив приспособление для фиксации зубных протезов в полости рта
- 2218907 Средство для ухода за кожей лица и веками
- 2318830 Способ получения модифицированного дерматансульфата
- 2118153 Косметика - туш для ресниц
- 2217441 Способ получения полимера
- 2317296 Изетионатная соль селективного ингибитора CDK4
- 2217171 Мембрана для использования при направленной регенерации тканей
- 2317095 Экстракты ECHINACEA ANGUSTIFOLIA
- 2216332 Препарат для лечения астроза
- 2216314 Крем - маска для обезвоженной кожи
- 2316333 Средство оздоровительно-восстановительных косметических панто-магниевых ванн
- 2021304 Способ получения биологически активного средства
- 2115662 Способ получения гиалуроновой кислоты
- 2315627 Впрыскиваемые имплантанты на керамической основе для заполнения морщин, кожных впадин, шрамов
- 2315623 Средство получаемое путем лиофилизации препарата
- 2114862 Способ получения гиалуроновой кислоты
- 2314791 Лечебно-Косметическое средство
- 2314791 Косметический крем-бальзам для ухода за кожей лица и шеи
- 2214600 Способ оценки эффективности лечения неврологических проявлений
- 2114602 Способ косметической обработки
- 2114587 Раствор для защиты роговицы
- 2214283 Имплантант для подкожного или внутрикожного введения
- 2313370 Медицинские протезы, имеющие улучшенную биологическую совместимость
- 2313356 Препарат для лечения демодекоза
- 2313338 Средство на основе этиллинолеата и триэтилцитрата для лечения себореи и угрей
- 2313328 Косметика содержащая тонкодисперный и пористый порошок
- 2212880 Способ получения препарата содержащего антибиотик, с замедленным высвобождением активного вещества
- 2312640 Способ лечения Блефароконьюнктивальной формы синдрома сухого глаза
- 2017751 Способ получения гиалуроновой кислоты
- 2312145 Гены CORYNEBACTERIUM GLUTAMICUM, кодирующие белки, участвующие в синтезе мембран и мембранном транспорте
- 2311458 Белки вызывающие измененную иммуногенную реакцию. Способ их получения и использования
- 2311183 Улучшенное разделение с использованием гталуроновой кислоты
- 2311177 Ингибиторы интегрина для лечения заболевания глаз
- 2300069 Косметическая маска
- 2211024 Уход за сухой кожей
- 2310440 Раствор для защиты роговицы от повреждений
- 2309684 Лечение межфалангового остеоатроза узелковой формы
- 2309406 Способ мониторинга фиброза печени у больных хроническим гепатитом с (ХГС)
- 2209088 Опосредованная рецепторами доставка генов с использованием векторов на основе бактериофагов
- 2308967 Уменьшение объема ткани
- 2308962 Средство для опорно-дигательного аппарата
- 2308957 Способ получения препарата для мезотерапии
- 2308954 Средство для лечения ран, содержащее плазму или сыворотку крови
- 2308951 Комплексный способ профилактики вагинальных дисбактериозов
- 2308937 Косметическая биологически активная добавка и косметический литофитокомплекс на ее основе
- 2208638 ДНК (варианты), способ получения белка
- 2207885 Способ подачи небольшого объема лечебного раствора к целевому месту
- 2207858 Лишенные побочных эффектов производные простагландинов для лечения глаукомы
- 2207845 Твердая лекарственная форма пролонгированного действия
- 2207844 Препарат для местного неинвазивного применения
- 2207841 Средства с антиферментативным действием
- 2306335 Стволовые клетки и решетки полученные из жировой ткани
- 2306140 Новые рецепторы для Helicobacter pylori и их применение
- 2205612 Способ эндотелизации IN VITRO протезов кровеносных сосудов
- 2105540 Депигментирующее средство
- 2304960 Косметическое средство для кожи
- 2304616 Гены участвующие в гомеостазе и адаптации
- 2204550Способ получения длинноцепочечной N-Ацилированной кислотой Аминокислот
- 2204415 Способ получения изображения
- 2204394 Средство для лечения грибковых инфекций, желудочных язв
- 2204366 Способ хирургического лечения глаукомы
- 2104034 Вагинальное увлажняющие средство, способ его получения
- 2303991 Биологически активная добавка
- 2303990 БАД
- 2303973 Адсорбирующее изделие
- 2203676 Средство обладающее иммунокорригирующим действием
- 2203672 Способ предупреждения беременности
- 2303635 Гены кодирующие белки резистентности и толерантности к стрессам
- 2303529 Способ фиксации альгинатного геля на твердой фазе, способ получения клеточного чипа на его основе
- 2203078 Способ лечения гнойных ран
- 2302412 Гидразоно-малонитрилы
- 2102400 Способ получения гиалуроновой кислоты
- 2202356 Способ стимуляции репаративных процессов длительно незаживающих ран и трофических язв
- 2202336 Средство для ухода за кожей
- 2302231 Глазные капли
- 2102082 Способ магнитометрического исследования тела человека или животного
- 2301814 Полиакриламидный гидрогель
- 2201765 Гибридные матричные имплантанты и эксплантанты
- 2301677 Биотрансплантант для лечения дегенеративных и трвматических заболеваний хрящевой ткани и способ его получения
- 2301676 Способ лечения ревматизма
- 2301674 Способ лечения больных с переломами нижней челюсти
- 2301661 Средство с регулируемым освобождением и способ его получения
- 2005488 Средство для лечения болезней соединительной ткани
- 2200001 Крем для кожи
|
РОССИЙСКАЯ ФЕДЕРАЦИЯ

ФЕДЕРАЛЬНАЯ СЛУЖБА
ПО ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ
ПАТЕНТАМ И ТОВАРНЫМ ЗНАКАМ
|
Патент №2358728 |
(54) СПОСОБ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ПОТЕРИ КОСТНОЙ ТКАНИ
(57) Реферат:
Изобретение относится к медицине и может быть использовано для идентификации соединений, которые обладают способностью увеличивать минеральную плотность костной ткани. Способ заключается в том, что соединение приводят в контакт с 15-липоксигеназой и определяют, обладает ли соединение активностью в отношении ингибирования 15-липоксигеназы. Изобретение позволяет расширить ассортимент лекарственных средств для лечения заболеваний, связанных с потерей костной ткани, таких как остеопороз, остеоартрит, болезнь Пэджета, и заболеваний периодонта, а так же переломов. 6 з.п. ф-лы, 4 табл., 9 ил.
Изобретение относится в целом к ингибиторам 15-липоксигеназы и их применению для лечения и предупреждения потери костной ткани. Конкретно изобретение относится к применению ингибиторов 15-липоксигеназы для уменьшения потери костной ткани и/или усиления образования сетчатой структуры костной ткани.
Липоксигеназы представляют собой ферменты, содержащие железо, не входящее в состав гема, которые присутствуют в растениях и животных и катализируют окисление определенных полиненасыщенных жирных кислот, например, входящих в состав липидов и липопротеинов. Известно несколько различных липоксигеназ, каждая из которых отличается по окислительной активности. Липоксигеназы млекопитающих обозначают по положению в молекуле арахидоновой кислоты, в котором происходит окисление. 5-липоксигеназа превращает арахидоновую кислоту в 5-гидропероксиэйкозатетраеновую кислоту (5-ГПЭТЕ). Это представляет собой первую стадию метаболизма, приводящего к образованию 5-гидроксиэйкозатетраеновой кислоты (5-ГЭТЕ) и лейкотриенов (ЛТ). Аналогично этому 12- и 15-липоксигеназы превращают арахидоновую кислоту в 12- и 15-ГПЭТЕ соответственно. Восстановление биохимическим путем 12-ГПЭТЕ приводит к образованию 12-ГЭТЕ, в то время как 15-ГЭТЕ является предшественником класса соединений, известных как липоксины.
Другой ряд биологических воздействий связан с продуктами, обладающими липоксигеназной активностью, многие из которых являются медиаторами различных болезненных состояний. ЛТ С4 и D4 являются сильными констрикторами человеческой бронхиальной гладкой мышцы; ЛТ В4 и 5-ГЭТЕ, обнаруженные в синовиальной жидкости пациентов, страдающих ревматоидным артритом, являются сильными хемотаксическими факторами воспалительных клеток, таких как полиморфонуклеарные лейкоциты (Green и Lambeth, Tetrahedron, 39, с.1687, 1983); были выявлены высокие уровни 12-ГЭТЕ в эпидермальной ткани пациентов, страдающих псориазом; было установлено, что липоксины стимулируют высвобождение присутствующего в лизосоме фермента и иона супероксида из нейтрофилов. Так, липоксигеназы играют важную роль в биосинтезе медиаторов астмы, аллергии, артрита, псориаза и воспаления, и ингибиторы этих ферментов прерывают путь биосинтеза, участвующий в развитии этих болезненных состояний.
Человеческая 15-липоксигеназа (15-ЛО) катализирует образование 15-S-гидроксиэйкозатетраеновой кислоты (15-S-ГЭТЕ) из арахидоновой кислоты (Kuhn и Borngraber, Lipoxygenases and Their Metabolites, изд-во Plenum Press, Нью-Йорк, 1999). У мышей синтез 15-8-ГЭТЕ осуществляется под воздействием 12/15-липоксигеназы (Alox15), которая представляет собой мышиный гомолог человеческой 15-ЛО. Мышиная 12/15-ЛО превращает арахидоновую кислоту в 12-(S)-гидроксиэйкозатетраеновую и 15-S-ГЭТЕ в соотношении 3:1 и, кроме того, она может превращать линолевую кислоту в 13-гидроксиоктадекадиеновую кислоту (13-ГОДЭ).
Ранее было установлено, что 15-липоксигеназа участвует в патогенезе некоторых заболеваний, включая атеросклероз (Harats и др., Arterioscler. Thromb. Vase. Biol., cc. 2100-2105, 2000), астму (Shannon и др., Am.Rev.Respir. Dis., 147, cc.1024-1028, 1993), рак (Shureiqi и др., JNCI, 92, cc.1136-1142, 2000) и гломерулонефрит (Montero и Badr, Exp. Neph., 8, cc.14-19, 2000). Были выявлены многочисленные классы соединений, которые обладают способностью ингибировать 15-липоксигеназу, в частности фенолы, гидроксамовые кислоты и ацетиленовые жирные кислоты (см. обзор Kuhn и Borngraber, Lipoxygenases and Their Metabolites, изд-во Plenum Press, Нью-Йорк, 1999). Эти агенты обладают различным спектром ингибирующей активности. Например, установлено, что нордигидрогвайаретовая кислота является ингибитором 5-и 15-липоксигеназы, установлено, что нафтилгидроксамовые кислоты ингибируют 5-, 12-и 15-липоксигеназу (US 4605669), и опубликованы данные о том, что бензофлуореновый ингибитор 15-липоксигеназы, PD 146176, обладает относительно специфичным действием в отношении 15-липоксигеназы (Sendobry и др., Br. J. Pharm., 120, cc.1199-1206, 1997). В опытах на мышах со специально созданной делецией гена Alox15 (Alox15 -/-) было установлено, что 15-липоксигеназа участвует в развитии атеросклероза. Первоначально было установлено, что такие мыши с дефицитом Alox15 обладают небольшим фенотипическими отличиями, включая повышенную активность присутствующей в них 5-ЛО (Sun и Funk, J. Biol. Chem., 271, cc.24055-24062, 1996). Однако нарушение Alox15 приводит к существенному уменьшению атеросклеротических повреждений у имеющих тенденцию к атеросклерозу мышей с дефицитом ароЕ (ароЕ -/-) (Cyrus и др., J. Clin Invest., 103, cc.1597-1604, 1999).
Хотя имеются данные о том, что 5-ЛО участвует в патогенезе некоторых заболеваний, биологическая функция мышиной или человеческой 15-липоксигеназы полностью не выявлена и не описано, что в клинических опытах установлена возможность применения ингибиторов 15-липоксигеназы для человека. В частности, до настоящего времени не описана возможность применения ингибиторов 15-липоксигеназы для лечения остеопороза и/или остеоартрита у человека.
Остеопороз обусловлен уменьшением плотности минерального компонента костной ткани (минеральной плотности костной ткани (МПК)) в зрелой кости и приводит к переломам после незначительной травмы. Заболевание является широко распространенным и наносит чрезвычайно большой экономический ущерб. Наиболее часто переломы происходят в позвоночнике, дистальном отделе лучевой кости и тазобедренном суставе. Оценки свидетельствуют о том, что одна треть женщин в возрасте свыше 65 лет может иметь переломы позвоночника, обусловленные, в частности, остеопорозом. Кроме того, в преклонном возрасте существует вероятность переломов тазобедренного сустава у приблизительно одной из трех женщин и у одного из шести мужчин.
Установлено, что имеются две различные фазы потери костной ткани. Одна представляет собой медленный связанный с возрастом процесс, который происходит у людей обоего пола и начинается в возрасте приблизительно 35 лет. Эта фаза протекает с приблизительно одинаковой скоростью у людей обоего пола и приводит к потере приблизительно одинаковых количеств кортикального слоя кости и губчатого вещества (спонгиозного или похожего на решетку слоя) кости. Кортикальный слой кости преобладает в добавочном скелете, в то время как губчатое вещество сконцентрировано в осевом скелете, прежде всего в позвоночнике, а также на концах длинных костей. Остеопороз, вызываемый связанной с возрастом потерей костной ткани, называют остеопорозом типа II.
Другой тип потери костной ткани происходит ускоренно, он проявляется у женщин в постменопаузальном периоде и обусловлен дефицитом эстрогена. На этой фазе происходит непропорциональная потеря губчатого вещества кости. Остеопороз, обусловленный истощением эстрогена, называют остеопорозом типа I. Основными клиническими последствиями остеопороза типа I являются переломы позвоночника, тазобедренного сустава и предплечья. Области скелета, для которых характерны такие повреждения, содержат большие количества трабекулярной костной ткани. Для остеопороза типа I, как правило, характерен высокий уровень обмена костной ткани. Резорбция костной ткани повышается, но компенсирующее образование костной ткани является неадекватным. Было установлено, что остеопороз связан с применением кортикостероидов, иммобилизацией или продолжительным нахождением в постельном режиме, алкоголизмом, диабетом, гонадотоксической химиотерапией, гиперпролактинемией, нервно-психической анорексией, первичной и вторичной аменореей, иммунодепрессией, связанной с введением трансплантата, и овариэктомией.
Предполагается, что механизм потери костной ткани при остеопорозе связан с дисбалансом процесса обновления скелета. Этот процесс называется ремоделированием костной ткани. Он происходит в ряде дискретных «карманах» активности. Эти карманы образуются спонтанно внутри костного матрикса на определенной поверхности костной ткани и представляют собой область резорбции костной ткани. Остеокласты (клетки, растворяющие костную ткань или ответственные за резорбцию костной ткани) осуществляют резорбцию части костной ткани, как правило, определенного постоянного размера. Затем после завершения этого процесса резорбции появляются остеобласты (костеобразующие клетки), которые заполняют полость, оставшуюся после остеокластов, новой костной тканью.
В организме здорового взрослого индивидуума остеокласты и остеобласты функционируют таким образом, что образование костной ткани и резорбция костной ткани сбалансированы. Однако при остеопорозе развивается дисбаланс в процессе ремоделирования костной ткани, в результате чего замена костной ткани происходит с меньшей скоростью, чем ее потеря. Хотя этот дисбаланс в определенной степени возникает у большинства индивидуумов в пожилом возрасте, он проявляется намного более серьезным образом и встречается в молодом возрасте при постменопаузальном остеопорозе, после овариэктомии или при ятрогенных (обусловленных применением лекарственных средств) состояниях, таких как состояния, вызванные применением кортикостероидов или иммунодепрессантов.
Для увеличения массы костной ткани у людей, страдающих остеопорозом, были предложены различные подходы, включая введение андрогенов, солей фтора и паратиреоидного гормона и модифицированных версий паратиреоидного гормона. Было предложено также применять для сохранения существующей массы костной ткани индивидуально или в сочетании друг с другом бисфосфонаты, кальцитонин, кальций, 1,25-дигидроксивитамин D3 и/или эстрогены.
Настоящее изобретение основано на открытии того, что ингибиторы 15-липоксигеназы обладают способностью увеличивать образование сетчатой структуры костной ткани и/или усиливать отложение костной ткани и ускорять заживление переломов. Такие молекулы можно вводить индивидуально или в сочетании с дополнительными агентами, которые обладают способностью ингибировать резорбцию костной ткани и/или усиливать образование костной ткани, в частности, с анаболиками.
Таким образом, одним из объектов изобретения является способ уменьшения потери костной ткани у индивидуума. Способ заключается в том, что индивидууму вводят фармацевтически эффективное количество ингибитора 15-липоксигеназы.
Другим объектом изобретения является способ повышения минеральной плотности костной ткани, заключающийся в том, что индивидууму вводят фармацевтически эффективное количество ингибитора 15-липоксигеназы.
Еще одним объектом изобретения является способ диагностики предрасположенности индивидуума к потере костной ткани, заключающийся в том, что осуществляют обнаружение полиморфизма человеческой хромосомы 17, прежде всего обнаружение полиморфизма гена 15-липоксигеназы.
Следующим объектом изобретения является способ отбора соединений, обладающих способностью уменьшать потерю костной ткани или увеличивать плотность минерального компонента костной ткани, заключающийся в том, что ингибиторы 15-липоксигеназы приводят в контакт с человеческими мезенхимальными стволовыми клетками и определяют клеточную дифференцировку клеток, участвующих в образовании костной ткани.
Эти и другие объекты настоящего изобретения более детально поясняются с помощью приведенного ниже подробного описания изобретения и прилагаемых чертежей. Кроме того, в настоящее описание полностью включены в качестве ссылки различные ссылки, в которых более подробно изложены определенные процедуры или композиции.
При осуществлении на практике настоящего изобретения можно применять, если не указано иное, стандартные методы химии протеинов, биохимии, методы рекомбинантной ДНК и фармакологии, известные специалистам в данной области. Такие методы подробно описаны в литературе (см., например, Т.Е. Creighton, Proteins: Structures and Molecular Properties (изд-во W.H. Freeman and Company, 1993); A.L. Lehninger, Biochemistry (изд-во Worth Publishers, Inc., последнее издание); Sambrook и др., Molecular Cloning: A Laboratory Manual (2-е изд., 1989); Methods In Enzymology (под ред. S. Colowick и N. Kaplan, изд-во Academic Press, Inc.); Remington's Pharmaceutical Sciences, 18-е изд. (Истон, шт.Пенсильвания: изд-во Mack Publishing Company, 1990); Carey и Sundberg Advanced Organic Chemistry, 3-е изд.. (изд-во Plenum Press), тома А и В (1992).
Все публикации, патенты и заявки на патент, процитированные выше или ниже в настоящем описании, полностью включены в настоящее описание в качестве ссылки.
При описании настоящего изобретения используются перечисленные ниже понятия, значения которых указаны ниже.
Понятие "потеря костной ткани" означает дисбаланс соотношения образования костной ткани и резорбции костной ткани, приводящий к меньшему, чем это необходимо, количеству костной ткани у пациента. Потеря костной ткани может происходить в результате остеопороза, остеотомии, периодонтита или обусловливаться неплотно прилегающим протезом. Потеря костной ткани может быть обусловлена также вторичным остеопорозом, который включает индуцированный глюкокортикоидами остеопороз, индуцированный гипертиреозом остеопороз, индуцированный иммобилизацией остеопороз, индуцированный гепарином остеопороз или индуцированный иммунодепрессантами остеопороз. Можно осуществлять мониторинг потери костной ткани, например, путем описанных ниже измерений плотности минерального компонента костной ткани.
Понятия "эффективное количество" или "фармацевтически эффективное количество" обозначает количество агента, которое не вызывает токсического действия, но является достаточным для обеспечения требуемого биологического результата. Таким результатом может являться уменьшение и/или облегчение признаков, симптомов или причин заболевания или любое другое требуемое изменение биологической системы. Например, "эффективное количество" с точки зрения терапевтического применения обозначает количество композиции, содержащей действующее вещество, необходимое для обеспечения клинически значимого повышения скорости заживления при лечении перелома; реверсии потери костной ткани при остеопорозе; реверсии повреждений или нарушений хрящевой ткани; предупреждения или замедления начала остеопороза; стимуляции и/или усиления образования костной ткани при несращиваемых переломах и остеогенеза при растяжении; увеличения и/или ускорения роста костной ткани в применяемых в качестве протеза устройствах; и восстановления дефектов зубов. Специалист в данной области может определить соответствующее "эффективное" количество в каждом отдельном случае с помощью стандартных экспериментов.
Понятие "увеличение отложения костной ткани" означает, что накопление костной ткани у индивидуума, которому вводят ингибиторы 15-липоксигеназы, предлагаемые в изобретении, увеличивается по сравнению с накоплением костной ткани у индивидуума, с которым производится сравнение и которому не вводят ингибитор 15-липоксигеназы. Такое увеличенное отложение костной ткани, как правило, определяют согласно настоящему изобретению путем измерения минеральной плотности костной ткани (МПК). Например, увеличение отложения костной ткани можно определять на модели с использованием животных, таких как подвергнутые овариэктомии мыши, собаки и т.п. Животному вводят тестируемое соединение и измеряют минеральную плотность костной ткани (МПК) в костях, которые, как правило, истощаются при остеопорозе типа I или типа II, таких как кости добавочного и/или осевого скелета, прежде всего позвоночного столба, включая позвонки, а также концевые части длинных костей, таких как бедренная кость, средний отдел и дистальный отдел лучевой кости. В данной области техники известны несколько методов определения МПК. Например, можно осуществлять измерения МПК с помощью двойной абсорбциометрии энергии рентгеновских лучей или количественной компьютерной томографии и т.п. (см. примеры). Аналогично этому с помощью методов, хорошо известных в данной области, можно определять увеличение образования костной ткани. Например, можно проводить динамические измерения скорости костеобразования (КОС) на меченных с помощью тетрациклина образцах губчатой кости из поясничного отдела позвоночного столба и дистального метафиза бедренной кости с помощью количественной компьютерной морфометрии (см., например. Ling и др., Endocrinology 140: cc.5780-5788, 1999. В альтернативном варианте можно оценивать маркеры образования костной ткани, такие как активность щелочной фосфатазы и уровни остеокальцина в сыворотке, для определения косвенным путем того, происходит ли образование костной ткани (см. Looker и др., Osteoporosis International 11(6): cc.467-480, 2000).
Понятие "увеличенное образование костной ткани" означает, что количество образующейся костной ткани у индивидуума, которому вводят ингибиторы 15-липоксигеназы, предлагаемые в изобретении, увеличивается по сравнению со скоростью образования костной ткани у индивидуума, которому не вводят ингибитор 15-липоксигеназы. Такое увеличенное образование костной ткани определяют согласно настоящему изобретению с помощью, например, количественной компьютерной морфометрии, а также с помощью описанных выше других маркеров образования костной ткани.
Понятие "ингибитор 15-липоксигеназы" обозначает соединение, которое ингибирует 15-липоксигеназу и характеризуется значением IC50 менее чем 1 мкМ, предпочтительно менее чем 100 нМ. Значения IC50 можно определять стандартными методами. Одним из конкретных методов является колориметрический анализ, согласно которому предполагаемый ингибитор предварительно инкубируют в течение примерно 10 мин с 15-липоксигеназой, после чего добавляют субстрат, представляющий собой линолевую кислоту, и выдерживают еще в течение 10 мин. Продукт, т.е. 13-HPODE, оценивают количественно методом, основанным на сочетании восстановления гидроксипероксилированного липида и окисления N-бензоиллейкометиленового синего в присутствии гемина при рН 5. Поглощение окисленного метиленового синего прямо пропорционально количеству 13-HPODE, образованного с помощью 15-липоксигеназы, и его можно измерять в присутствии ингибитора и без него. Этот конечный анализ описан более подробно у Bruce J. Auerbach, John S. Kiely и Joseph A. Cornicelli, A Spectrophotometric Microtiter-Based Assay for the Detection of Hydroperoxy Derivatives of Linoleic Acid, Analytical Biochemistry, 201, cc.375-380, 1992. Другие методы анализа включают методы, в которых начальную скорость ферментативной реакции измеряют спектрофотометрически путем измерения при 234 нм количества образовавшегося конъюгированного диена.
В контексте настоящего описания понятия "лечить" или "лечение" используются взаимозаменяемо и применяются для обозначения замедления развития симптомов потери костной ткани и/или уменьшения серьезности таких симптомов, которые развиваются или развитие которых предполагается. Кроме того, понятия включают предупреждение дополнительных симптомов, облегчение или предупреждение обусловливающих симптомы метаболических факторов и/или стимулирование роста костной ткани.
"Фармацевтически приемлемый" или "фармакологически приемлемый" обозначает продукт, который не является нежелательным ни с биологической, ни с иной точки зрения, т.е. продукт, который можно вводить индивидууму, не вызывая никаких нежелательных биологических действий или вредных взаимодействий с любыми компонентами композиции, в которую он входит.
"Физиологическое значение рН" или "значение рН, находящееся в диапазоне физиологических значений", означает значение рН в диапазоне примерно от 7,2 до 8,0 включительно, более предпочтительно в диапазоне примерно от 7,2 до 7,6 включительно.
В контексте настоящего описания понятие "пациент" обозначает млекопитающих и животных, не относящихся к млекопитающим. Примеры млекопитающих включают (но, не ограничиваясь ими) любого представителя класса млекопитающих: человека, приматов кроме человека, таких как шимпанзе и других видов человекообразных обезьян и обезьян; сельскохозяйственных животных, таких как крупный рогатый скот, лошади, овцы, козы, свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, в том числе грызунов, таких как крысы, мыши и морские свинки, и т.п. Примеры животных, не относящихся к млекопитающим, включают (но, не ограничиваясь ими) птиц, рыб и т.п. Понятие не обозначает конкретный возраст или пол.
В контексте настоящего описания "полиморфизм" обозначает наличие в популяции двух или большего количества генетически детерминированных альтернативных последовательностей или аллелей. Полиморфный маркер или сайт представляет собой локус, в котором происходит дивергенция. Предпочтительные маркеры представляют собой по меньшей мере два аллеля, каждый из которых встречается в рассматриваемой популяции с частотой более чем 1%, более предпочтительно более чем 10 или 20%. Полиморфизм может представлять собой замены, инсерцию, повтор или делецию одного или нескольких оснований. Полиморфный локус может представлять собой всего лишь одну пару оснований. Полиморфные маркеры включают полиморфизмы длин рестрикционных фрагментов, варьиабельное количество тандемных повторов (ВКТП), гипервариабельные участки, минисателлиты, динуклеотидные повторы, тринуклеотидные повторы, тетрануклеотидные повторы, простые повторы последовательности и инсерционные элементы.
Однонуклеотидный полиморфизм (SNP) возникает в полиморфном сайте, занятом одним нуклеотидом, который представляет собой сайт вариации аллельных последовательностей. Как правило, перед сайтом и после него расположены высококонсервативные последовательности аллеля (например, последовательности, которые варьируются менее чем у 1/100 или 1/1000 представителей популяций). Однонуклеотидный полиморфизм, как правило, возникает в результате замены одного нуклеотида другим в полиморфном сайте. Транзиция представляет собой замену одного пуринового основания на другое пуриновое основание или одного пиримидинового основания на другое пиримидиновое основание. Трансверсия представляет собой замену пуринового основания на пиримидиновое основание, или наоборот. Однонуклеотидный полиморфизм может возникать также в результате делеции нуклеотида или инсерции нуклеотида в аллель, которые отсутствуют в аллеле, с которым производится сравнение.
В контексте настоящего описания понятие "клетка-предшественник" обозначает клетку, которая еще не полностью дифференцировалась или перешла на стадию (путь) дифференцировки и которая, как правило, не экспрессирует маркеры или не обладает функциями, присущими зрелой полностью дифференцированной клетке.
В контексте настоящего описания понятие "мезенхимальные клетки" или "мезенхимальные стволовые клетки" обозначает мультипатентные клетки-предшественники, которые обладают способностью к многократному делению и потомство которых образует скелетные ткани, включая хрящевую ткань, костную ткань, сухожилия, связки, строму костного мозга и соединительную ткань (см. A. Caplan, J. Orthop.Res. 9: cc.641-650, 1991).
В контексте настоящего описания понятие "остеогенные клетки" обозначает остеобласты и клетки-предшественники остеобластов.
В контексте настоящего описания понятие "локус количественного признака" (КПЛ) обозначает меру фенотипического признака, такую как минеральная плотность костной ткани, который является непрерывно распределенным и может определяться несколькими генами. КПЛ представляет собой сайт на хромосоме, аллели которой влияют на количественный признак.
Соединения, предлагаемые в настоящем изобретении, представляют собой соединения, которые обладают способностью ингибировать или уменьшать активность 15-липоксигеназы. В этом контексте ингибирование и уменьшение активности фермента означает уменьшение уровня измеренной активности по сравнению с контрольным экспериментом, в котором фермент, клетку или индивидуум не подвергают обработке тестируемым соединением. В конкретных вариантах осуществления изобретения ингибирование или уменьшение измеренной активности составляет по меньшей мере 10%. Специалисту в данной области должно быть очевидно, что для конкретных случаев применения может быть предпочтительным уменьшение или ингибирование измеренной активности по меньшей мере на 20, 50, 75, 90 или 100% или на любое целое число процентов от 10 до 100%. Как правило, ингибиторы 15-липоксигеназы, предлагаемые в настоящем изобретении, характеризуются значением IC50 менее чем 1 мкМ, предпочтительно менее чем 100 нМ.
Настоящее изобретение основано, в частности, на открытии того факта, что 15-липоксигеназа представляет собой важный модулятор массы костной ткани. В частности, геномное сканирование 100 микросателлитных маркеров у мышей позволило выявить локусы чувствительности к нарушению, связанному с потерей костной ткани, которые расположены на хромосомах 1, 2, 4 и 11. Различия в экспрессии генов, прежде всего генов, кодируемых на хромосоме 11, обусловливают существенные различия в экспрессии гена, кодирующего 15-липоксигеназу, что свидетельствует о наличии связи между экспрессией 15-липоксигеназы и уменьшением минеральной плотности костной ткани.
Полная масса костной ткани является основным критерием риска, обусловленного остеопорозом перелома. На основе семейных исследований и исследований, проведенных на близнецах, было установлено, что минеральную плотность костной ткани (МПК) регулируют генетические факторы (см. обзор Stewart и Ralston, J. Endocr., 166: cc.235-245, 2000). При создании изобретения применяли модель с использованием генов мыши для идентификации локусов, контролирующих МПК. Для идентификации областей генома, которые регулируют минеральную плотность костной ткани, применяли метод, включающий две стадии. Сначала применяли компьютерный метод и микросателлитные маркеры для сканирования базы данных однонуклеотидного полиморфизма (SNP) животного, в результате чего были предсказаны области хромосом, которые участвуют в накоплении и поддержании скелетной массы (пример 1). Затем применяли модели с использованием животных для идентификации и оценки мутаций в генах, участвующих в накоплении и поддержании скелетной массы (пример 2), и для установления того факта, что нарушение гена 15-липоксигеназы приводит к увеличению МПК (пример 4), что свидетельствует о том, что ген 15-липоксигеназы участвует в регуляции массы костной ткани.
Соединения, которые ингибируют активность 15-липоксигеназы и предупреждают резорбцию костной ткани или стимулируют образование костной ткани, являются наиболее предпочтительными для лечения остеопороза. Соединения, которые ингибируют активность 15-липоксигеназы, можно применять в способе лечения остеопороза или остеоартрита, основанном на ингибировании резорбции костной ткани остеокластами или стимуляции дифференцировки, приводящей к образованию остеобластов, и формирования новой костной ткани. В примере 3 продемонстрирована способность ингибиторов 15-липоксигеназы стимулировать дифференцировку человеческих мезенхимальных стволовых клеток в остеобласты in vitro. В примере 4 продемонстрировано, что полное нарушение гена 15-липоксигеназы in vivo приводит к увеличению МПК. В примере 5 на модели in vivo продемонстрирована способность ингибиторов 15-липоксигеназы стимулировать образование костной ткани.
Согласно настоящему изобретению ингибитор 15-липоксигеназы можно применять для приготовления лекарственного средства, которое содержит эффективное количество указанного ингибитора 15-липоксигеназы, предназначенного для уменьшения потери костной ткани у млекопитающего. Так, в настоящем изобретении предложен способ уменьшения потери костной ткани у млекопитающего, который заключается в том, что индивидууму вводят эффективное количество ингибитора 15-липоксигеназы. Предпочтительно потеря костной ткани связана с остеопорозом, остеоартритом, болезнью Пэджета или заболеваниями периодонта. Более предпочтительно потеря костной ткани связана с остеопорозом.
Кроме того, согласно настоящему изобретению ингибитор 15-липоксигеназы можно применять для приготовления лекарственного средства, предназначенного для увеличения минеральной плотности костной ткани у млекопитающего, которое содержит эффективное количество указанного ингибитора 15-липоксигеназы. Таким образом, в настоящем изобретении предложен также способ увеличения минеральной плотности костной ткани у млекопитающего, заключающийся в том, что млекопитающему вводят эффективное количество ингибитора 15-липоксигеназы.
Согласно настоящему изобретению ингибитор 15-липоксигеназы можно применять для приготовления лекарственного средства, содержащего эффективное количество ингибитора 15-липоксигеназы, которое предназначено для лечения остеопороза у млекопитающего. Таким образом, в настоящем изобретении предложен способ лечения остеопороза у млекопитающего, заключающийся в том, что млекопитающему вводят эффективное количество ингибитора 15-липоксигеназы.
Кроме того, ингибитор 15-липоксигеназы можно применять для приготовления лекарственного средства, предназначенного для стимуляции дифференцировки линии мезенхимальных стволовых клеток у человека в остеобласты, которое содержит количество указанного ингибитора 15-липоксигеназы, эффективное для увеличения количества остеобластов в организме человека. Таким образом, в настоящем изобретении предложен способ стимуляции дифференцировки линии мезенхимальных стволовых клеток у человека в остеобласты, заключающийся в том, что человеку вводят количество ингибитора 15-липоксигеназы, эффективное для увеличения количества остеобластов в организме человека. Предпочтительно ингибитор 15-липоксигеназы характеризуется значением IC50 менее 1 мкМ.
Лечение с помощью ингибитора 15-липоксигеназы можно применять для заживления переломов кости и остеоэктомий, включая как сращиваемые, так и не сращиваемые переломы. Типы переломов, которые можно лечить с помощью способов, предлагаемых в изобретении, включают переломы, вызываемые как травмой, так и остеопорозом, например переломы тазобедренного сустава, шейки бедра, запястья, позвонков, позвоночного столба, ребер, грудины, гортани и трахей, лучевой/локтевой кости, большеберцовой кости, коленной чашечки, ключицы, таза, плечевой кости, нижней части голени, пальцев руки и пальцев стопы, лица и лодыжки. С помощью способов, предлагаемых в настоящем изобретении, можно увеличивать скорость заживления, а также стимулировать сращивание в случае переломов, которые в противном случае остаются несращиваемыми. Профилактическое лечение пациента, для которого установлено, что он имеет риск возникновения переломов, может также снижать риск возникновения переломов у этого пациента.
Следовательно, ингибитор 15-липоксигеназы можно применять для приготовления лекарственного средства, которое содержит эффективное количество ингибитора 15-липоксигеназы, предназначенного для уменьшения количества случаев переломов у млекопитающего. Таким образом, в настоящем изобретении предложен способ уменьшения количества случаев переломов у млекопитающего, заключающийся в том, что млекопитающему вводят эффективное количество ингибитора 15-липоксигеназы.
Кроме того, ингибитор 15-липоксигеназы можно применять для приготовления лекарственного средства, которое содержит эффективное количество ингибитора 15-липоксигеназы, предназначенного для заживления переломов у млекопитающего. Таким образом, в настоящем изобретении предложен способ заживления переломов у млекопитающего, заключающийся в том, что млекопитающему вводят эффективное количество ингибитора 15-липоксигеназы.
Предпочтительно млекопитающее в указанных в описании способах и применениях представляет собой человека. Более предпочтительно описанный выше ингибитор 15-липоксигеназы характеризуется значением IC50 менее чем 1 мкМ.
Известны несколько ингибиторов 15-липоксигеназы, которые можно применять согласно способам, предлагаемым в настоящем изобретении. К таким ингибиторам относятся синтетические органические молекулы, растительные экстракты и другие природные продукты, а также антитела к 15-липоксигеназе. Репрезентативные примеры (не ограничивающие объем изобретения) описаны у Cornicelli JA, Trivedi BK., 15-lipoxygenase and its inhibition: a novel therapeutic target for vascular disease, [обзор] [113 ссылок]. Current Pharmaceutical Design; 5(1): cc.11-20, 1999 (описаны различные производные кофеиновой кислоты, простые пропаргиловые эфиры, катехолы и бензотиопираноиндолы); Cornicelli JA. 15-lipoxygenase inhibitors as antiatherosclerotic agents. Idrugs, 1(2): cc.206-213, 1998; Fleischer R., Frohberg P., Buge A., Nuhn P., Wiese M. QSAR analysis of substituted 2-phenylhydrazonoacetamides acting as inhibitors of 15-lipoxygenase. Quant Struct - Act Relat; 19(2): cc.162-172, 2000; Kuhn H. Inhibitors of 12/15-lipoxygenase are potential anti-atherosclerotic drugs. Curr Opin Anti-Inflammatory Immunomodulatory Invest Drugs; 1(3): cc.227-237, 1999; Mogul R., Johansen E., Holman T.R. Oleyl sulfate reveals allosteric inhibition of soybean lipoxygenase-1 and human 15-lipoxygenase. Biochemistry; 39(16): cc.4801-4807, 2000; Sexton К., Roark W.H., Sorenson R., Cornicelli J., Sekerke C., Welch K., Thiourea inhibitors of 15- lipoxygenase. Abstracts of Papers American Chemical Society; 218(1-2), 1999: MEDIO; Tait B.D., Dyer R.D., Auerbach B.J., Bornemeier D., Guilds-Zamarka L., Oxender M. и др. Catechol based inhibitors of 15-lipoxygenase. Bioorganic & Medicinal Chemistry Letters, том 6(1): cc.93-96, 1996; Moreau R.A., Agnew J., Hicks K.B., Powell M.J., Modulation of lipoxygenase activity by bacterial hopanoids. JouPHKl of Natural Products, том; 60(4): cc.397-398, 1997; 219th National Meeting of the American Chemical Society (2000), Poster BIOL-15. авторы: E-N-Jonsson и T-R-Holman. University of California, Santa Cruz, CA (описаны ингибиторы 15-липоксигеназы, выделенные из морских губок; и Lyckander I.M., Malterud K.E. Lipophilic flavonoids from Orthosiphon spicatus as inhibitors of 15-lipoxygenase. Acta Pharm Nord; 4(3): cc.159-166, 1992. Кроме того, согласно способам, предлагаемым в настоящем изобретении, можно применять производные тиомочевины и бензамида, описанные в U.S. No. 6268387 на имя Conner и др. (представителем которых является 3-амино-N-(3,4-дихлорфенил)-4-метоксибензамид, т.е. соединение 3), которые являются ингибиторами 15-липоксигеназы, а также 2-фенилбензо[d]изоселеназол-3-он (эбселен), 6,11-дигидро-5-тиа-11-азабензо[а]флуорин (обозначенный в настоящем описании как соединение 2), и фенилацетиленовые производные, представителем которых является 3-(2-окт-1-инилфенил)акриловая кислота, т.е. соединение 4. Можно применять также соединения, описанные в WO 01/96298 (включенный в настоящее описание в качестве ссылки), включая соединение 6, т.е. изобутиловый эфир [[[5-(5,6-дифтор-1Н-индол-2-ил)-2-метоксифенил]амино]сульфонил]карбаминовой кислоты.
К другим ингибиторам 15-липоксигеназы относятся перечисленные ниже соединения:
1)
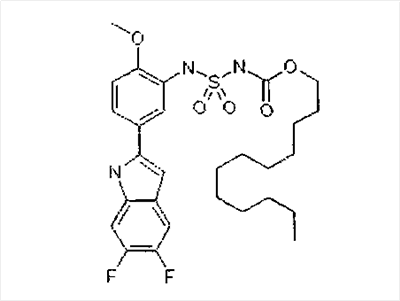
описанное в материалах 222-го National Meeting of the American Chemical Society, Чикаго, шт.Иллинойс, США, 26-30 августа 2001 г. постер, MEDI 270.
2)PD 148104
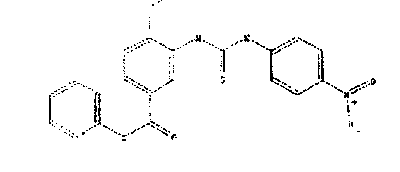
описанное в материалах 218-го ACS (Нью-Орлеан), 1999, MEDI 200.
3) PD 146176, разработанное фирмой Parke Davis (в настоящее время Pfizer)
4) А 78773 (фирма Abbott), описанное в WO 92/1682
5) QA-208-199 (фирма Novartis)
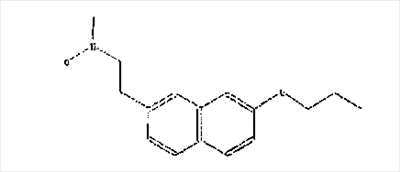
описанное в материалах 6-ой Int Conf Prostaglandins (Флоренция), 1986, 328 Связанный с этим объект настоящего изобретения относится к методам совместной терапии с использованием ингибиторов 15-липоксигеназы для увеличения образования костной ткани и других действующих веществ, таких как бисфосфонаты, эстроген, ИМРЭ (избирательные модуляторы рецептора эстрогена), кальцитонины или с использованием анаболиков. Примерами бисфосфонатов являются алендронат, ибандронат, памидронат, этидронат и ризедронат. Примерами ИМРЭ являются ралоксифен, дигидроралоксифен и лазофоксифен. Кальцитонины включают человеческий и лососевый кальцитонин. В качестве анаболиков можно применять паратиреоидные гормоны (РТН), например, hPTH(1-34), PTH(1-84), и протеин, связанный с паратиреоидным гормоном (РТНгР), и его аналоги. Конкретные аналоги PTHrP описаны в "Mono- and Bicyclic Analogs of Parathyroid Hormone-Related Protein. 1. Synthesis and Biological Studies," Michael Chorev и др. Biochemistry, 36: ее. 3293-3299, 1997 и "Cyclic analogs of РТН and PTHrP," в WO 96/40193 и U.S. No. 5589452 и WO 97/07815. Другое действующее вещество можно вводить одновременно, до или после введения ингибитора 15-липоксигеназы и его можно вводить с помощью другого метода введения. Предпочтительно сначала вводят ингибитор 15-липоксигеназы. Продолжительность такого введения может быть любой, но, как правило, она составляет от 6 до 24 месяцев. После этого лечения осуществляют лечение с помощью антирезорбтивного агента, например бисфосфоната, ИМРЭ, кальцитонина или с использованием гормонзаместительной терапии.
Так, предпочтительно можно применять композицию, содержащую описанный выше ингибитор 15-липоксигеназы и дополнительное действующее вещество. Таким образом, в описанном выше способе предпочтительно применяют дополнительное действующее вещество. Более предпочтительно указанное действующее вещество, которое используют или применяют согласно способу, предлагаемому в изобретении, является активным регулятором резорбции кальция из костной ткани. Наиболее предпочтительно указанное действующее вещество представляет собой вещество, выбранное из ряда, включающего эстроген, кальцитонин, бисфосфонат и IGF.
В предпочтительном варианте осуществления изобретения ингибитор 15-липоксигеназы, используемый в способах или применениях, изложенных в настоящем описании, выбирают из ряда, включающего синтетические органические молекулы, природные продукты и антитела к 15-липоксигеназе. В наиболее предпочтительном варианте осуществления изобретения ингибитор 15-липоксигеназы выбирают из ряда, включающего 3-(2-нон-1-инилфенил)пропионовую кислоту, 6,11-дигидро-5-тиа-11-азабензо[а]флуорен, 3-амино-N-(3,4-дихлорфенил)-4-метоксибензамид, транс-3-(2-окт-1-инилфенил)акриловую кислоту и изобутиловый эфир [[[5-(5,6-дифтор-1Н-индол-2-ил)-2-метоксифенил]амино]сульфонил]карбаминовой кислоты.
Согласно одному из вариантов осуществления изобретения способ, предлагаемый в изобретении, заключается в том, что осуществляют введение терапевтически эффективного количества антисмыслового олигонуклеотида, имеющего последовательность, которая обладает способностью специфически связываться с любыми последовательностями молекулы геномной ДНК или мРНК, кодирующей 15-липоксигеназу, вследствие чего предотвращается транскрипция или трансляция мРНК 15-липоксигеназы. Понятие "антисмысловой" относится к композиции, которая содержит нуклеотидную последовательность, комплементарную "смысловой" цепи конкретной нуклеотидной последовательности. После интродукции в клетку комплементарные нуклеотиды объединяются с эндогенными последовательностями, продуцируемыми клетками, в результате чего образуются дуплексы и происходит блокирование либо транскрипции, либо трансляции (см., например, Antisense Therapeutics, Humana Press Inc., под ред. Agrawal S., 1996, Totawa N.J.; Alama и др. Pharmacol. Res. 36: cc.171-178, 1997; Crooke S.T. Adv. Pharmacol. 40: cc.1-49, 1997; и Lavrosky и др. Biochem. Mol. Med. 62(1): cc.11-22, 1997). Антисмысловые последовательности могут представлять собой любые нуклеотидные последовательности, включая ДНК, РНК или любые миметики или аналоги нуклеиновых кислот (см., например, Rossi и др. Antisense Res. Dev. 1: cc.285-288, 1991; Pardridge и др. Proc. Nat. Acad. Sci. 92: cc.5592-5596, 1995; Nielsen и Haaima Chem. Soc. Rev. 96: cc.73-78, 1997; и Lee и др. Biochemistry 37: cc.900-1010, 1998). Введение антисмысловых последовательностей можно осуществлять различными путями, например, путем введения в клетку с помощью рекомбинантного вектора.
Как правило, предпочтительно используют антисмысловые олигонуклеотиды, состоящие из примерно 15-25 нуклеотидов, поскольку их легко синтезировать и они обладают способностью оказывать требуемое ингибирующее действие. Для этой цели можно применять также молекулярные аналоги антисмысловых олигонуклеотидов, что может давать дополнительные преимущества в отношении стабильности, распределения или снижения токсичности фармацевтического продукта. Кроме того, к антисмысловым олигонуклеотидам можно присоединять группы, обладающие химической реакционной способностью, такие как связанная с железом этилендиаминтетрауксусная кислота (ЭДТК-Fe), что приводит к расщеплению РНК в сайте гибридизации. Эти и другие методы ингибирования in vitro трансляции генов с использованием антисмысловых последовательностей хорошо известны в данной области (см., например, Marcus-Sakura, Anal. Biochem. 172: с.289, 1988).
Хотя многие ингибиторы 15-липоксигеназы являются известными и они указаны в настоящем описании, следует понимать, что в способах, предлагаемых в изобретении, можно использовать многие другие ингибиторы. Подразумевается, что в представленных в настоящем описании способах можно применять как известные в настоящее время ингибиторы 15-липоксигеназы, так и те, которые будут выявлены позднее. Представленные в настоящем описании методы анализа и другие методы, известные специалисту в данной области, позволяют легко идентифицировать и получать другие ингибиторы 15-липоксигеназы, которые можно применять для предупреждения или лечения потери костной ткани.
Как проиллюстрировано в примерах, генетические аномалии или алдели были обнаружены в хромосоме 11 и положение аллеля соответствует положению гена 15-липоксигеназы. Таким образом, ингибирование или индукцию 15-липоксигеназы можно применять в различных ситуациях. Возможно, что путем внутриклеточного ингибирования 15-липоксигеназы можно уменьшать обмен костной ткани и тем самым увеличивать минеральную плотность костной ткани и качество костной ткани. Таким образом, ингибирование 15-липоксигеназы можно использовать в способе лечения или предупреждения избыточной резорбции костной ткани, которая происходит при остеопорозе и остеоартрите.
Ингибиторы 15-липоксигеназы, предлагаемые в настоящем изобретении, можно применять также для стимулирования роста костеобразующих (остеогенных) клеток или их предшественников или для индукции дифференцировки предшественников костеобразующих клеток либо in vitro, либо ex vivo. Более конкретно ингибиторы 15-липоксигеназы можно применять для стимулирования популяции клеток, включающей мезенхимальные клетки костного мозга, увеличивая тем самым количество остеогенных клеток в популяции клеток. В предпочтительном варианте способа гематопоэтические клетки удаляют из популяции клеток либо до, либо после обработки ингибиторами 15-липоксигеназы. С помощью таких методов можно размножать остеогенные клетки. Размноженные остеогенные клетки можно вводить путем инфузии (или повторной инфузии) позвоночному животному, нуждающемуся в этом. Например, мезенхимальные стволовые клетки из организма самого индивидуума можно подвергать воздействию ех vivo соединений, предлагаемых в изобретении, и образовавшиеся остеогенные клетки можно вводить путем инфузии или непосредственно в требуемую область тела индивидуума, где дальнейшая пролиферация и/или дифференцировка остеогенных клеток может происходить без иммунного отторжения. В альтернативном варианте популяция клеток, подвергаемая действию ингибиторов 15-липоксигеназы, может представлять собой иммортализованные остеобластные или остеогенные клетки эмбриона человека. Если такие клетки вводят путем инфузии или имплантации в организм позвоночного животного, то может оказаться целесообразным для обеспечения иммунной защиты этих неаутологичных клеток или иммунной супрессии (предпочтительно местной) реципиента для повышения эффективности трансплантации и восстановления костной ткани или хряща.
Эффективность лечения можно оценивать путем мониторинга эффективности применения и способов, представленных выше в настоящем описании, для индивидуума, которые заключаются в измерении уровня 15-липоксигеназы в организме индивидуума, который также является объектом настоящего изобретения.
Можно применять также различные методы для идентификации классов ингибиторов 15-липоксигеназы, которые могут предупреждать потерю костной ткани и/или стимулировать образование костной ткани. Один из методов, которые можно применять для идентификации соединений, ингибирующих активность 15-липоксигеназы, заключается в том, что клетки, ткани или предпочтительно экстракт клеток или иной препарат, содержащий 15-липоксигеназу, приводят в контакт с несколькими известными концентрациями тестируемого соединения в буфере, не оказывающего влияния на активность 15-липоксигеназы. Уровень активности 15-липоксигеназы для каждой концентрации тестируемого соединения измеряют путем количественной оценки полученного в результате ферментативной реакции продукта и с помощью стандартных методов определяют значения IC50 (концентрация тестируемого соединения, при которой обнаруживаемая активность образца препарата уменьшается на половину от ее исходного или контрольного значения). Специалисту в данной области известны другие методы определения концентрации соединения, предлагаемого в изобретении, при которой происходит ингибирование 15-липоксигеназы, и, как это следует из приведенного описания, их можно применять для этой цели. Конкретные методы анализа, которые можно применять для идентификации ингибиторов 15-липоксигеназы, описаны в US  626887B1 и 5958950 (анализ, основанный на использовании кроличьих ретикулоцитов) и US 626887B1 и 5958950 (анализ, основанный на использовании кроличьих ретикулоцитов) и US  4623661 (анализ, основанный на использовании радиоактивномеченной арахидоновой кислоты в клетках линии RBL-1). 4623661 (анализ, основанный на использовании радиоактивномеченной арахидоновой кислоты в клетках линии RBL-1).
Например, как правило, антагонисты можно выявлять, если известна структура лиганда. В настоящее время благодаря разработке высокоавтоматизированных методов анализа с использованием клеток, дающих физиологический ответ, можно осуществлять тестирование потенциальных аналогов лигандов. В частности, с помощью представленных в настоящем описании методов скрининга можно выявлять новые агонисты и антагонисты.
Согласно другому способу для идентификации соединений, трехмерная структура которых комплементарна активному сайту 15-липоксигеназы, можно применять научно-обоснованное создание лекарственного средства на основе структурных исследований молекулярных форм хемокинов, других эффекторов или аналогов. Такие соединения можно выявлять различными методами, включая молекулярно-механические расчеты, молекулярно-динамические расчеты, молекулярно-динамические расчеты с учетом ограничений, где ограничения определяют на основе ЯМР-спектроскопии, дистанционной геометрии, где дистанционную матрицу частично определяют с помощью методов ЯМР-спектроскопии, дифракции рентгеновских лучей или дифракции нейтронов. При использовании всех этих методов структуру можно определять на основе сравнения данных, полученных в присутствии любого из лигандов, который, как известно, обладает способностью взаимодействовать с 15-липоксигеназой, или без него.
Такие компьютерные программы включают (но, не ограничиваясь ими) AMBER (которую можно получить из Калифорнийского университета (University of California), Сан-Франциско), CHARMM (Chemistry at HARvard Molecular Mechanics, которую можно получить из Гарвардского университета (Harvard University)), MM2, SYBYL (фирма Trypos Inc.), CHEMX (фирма Chemical Design), MACROMODEL, GRID (фирма Molecular Discovery Ltd) и Insight II (фирма Accelryl). Подразумевается, что такие программы можно применять для оценки химического взаимодействия между двумя молекулами, либо изолированными, либо находящимися в окружении молекул растворителя, таких как молекулы воды, или для расчетов, основанных на приблизительном учете влияния сольватации взаимодействующих молекул. Относительную ориентацию двух молекул можно определять вручную путем визуального наблюдения или с использованием других компьютерных программ, которые генерируют многочисленные возможные ориентации. Примерами компьютерных программ (но, не ограничиваясь ими) являются DOCK и AutoDOCK. С помощью компьютерных программ каждую ориентацию можно тестировать в отношении степени ее комплементарности. Таким путем можно создавать новые соединения, обладающие способностью ингибировать 15-липоксигеназу.
Другой способ идентификации соединений, обладающих способностью ингибировать 15-липоксигеназу, заключается в применении таких методов, как спектроскопия в УФ-лучах или видимом спектре, полариметрия, цифровая спектроскопия кристаллов (ЦС) или цифровая рамановская спектроскопия (ЦРС), инфракрасная спектроскопия или спектроскопия комбинационного рассеяния (Рамановская спектроскопия), спектроскопия ядерного магнитного резонанса, флуоресцентная спектроскопия, ЖХВР, гель-электрофорез, капиллярный гель-электрофорез, диализ, рефрактометрия, кондуктометрия, микроскопия на основе атомного взаимодействия, полярография, диэлектрометрия, калориметрия, измерение растворимости, ЭПР (электронный парамагнитный резонанс)- или масс-спектроскопия. Эти методы можно применять непосредственно для прямой оценки взаимодействия соединений с 15-липоксигеназой или косвенным образом, когда определенный агент, обладающий спектроскопическими свойствами, используют в качестве зонда для оценки способности других соединений связываться с 15-липоксигеназой; например, на основе замещения или тушения флуоресценции.
Таким образом, в настоящем изобретении предложен способ идентификации соединений, которые повышают минеральную плотность костной ткани, заключающийся в том, что соединение приводят в контакт с 15-липоксигеназой и определяют, ингибирует ли соединение активность 15-липоксигеназы. Предпочтительно, чтобы, кроме того, в способе было предусмотрено тестирование соединения с помощью функционального анализа для оценки действия соединения в отношении образования костной ткани. Более конкретно функциональный анализ заключается в том, что соединение приводят в контакт с человеческими мезенхимальными стволовыми клетками и определяют дифференцировку клеток в костеобразующие клетки. В другом более предпочтительном варианте осуществления изобретения функциональный анализ заключается в том, что соединение вводят животному, кроме человека, и измеряют индекс образования костной ткани. В наиболее предпочтительном варианте осуществления изобретения измеряемый индекс представляет собой минеральную плотность костной ткани. В другом наиболее предпочтительном варианте осуществления изобретения индекс представляет собой биомеханический параметр костной ткани.
В другом наиболее предпочтительном варианте осуществления изобретения функциональный анализ заключается в том, что соединение приводят в контакт с человеческими мезенхимальными стволовыми клетками и оценивают дифференцировку в костеобразующие клетки путем анализа активности щелочной фосфатазы, анализа содержания кальция, анализа общей ДНК в препаратах или их комбинаций.
В еще одном варианте осуществления изобретения предложен способ идентификации соединений, которые обладают способностью увеличивать минеральную плотность костной ткани, где способ заключается в том, что ингибитор 15-липоксигеназы приводят в контакт с человеческими мезенхимальными стволовыми клетками и оценивают дифференцировку клеток в клетки, образующие костную ткань. Предпочтительно оценку дифференцировки клеток осуществляют путем анализа активности щелочной фосфатазы, анализа содержания кальция, анализа общей ДНК в препаратах или их комбинаций
Идентифицированные или созданные таким образом ингибиторы 15-липоксигеназы можно затем тестировать в отношении их способности предупреждать потерю костной ткани и/или стимулировать образование костной ткани. В одном из вариантов осуществления изобретения применяют описанные выше компьютерные методы. В другом варианте способа соединения тестируют с точки зрения их способности воздействовать на известные мишени, связанные с потерей костной ткани, такие, например, как рецепторы эстрогена, рецептор фактора некроза опухоли, рецептор интегрина и т.п. Согласно еще одному варианту способа соединения тестируют в отношении их способности дифференцировать стволовые клетки в клетки костной ткани.
Согласно способам, представленным в настоящем описании, фармацевтические композиции, содержащие описанные выше молекулы, применяют в сочетании с одним или несколькими фармацевтически приемлемыми носителями и необязательно другими терапевтическими и/или профилактическими ингредиентами. Такими носителями являются жидкости, такие как вода, физиологический раствор, глицерин, полиэтиленгликоль, гиалуроновая кислота, этанол и т.д. Специалисту в данной области известны также пригодные носители для композиций не жидкого типа. В композициях, предлагаемых в настоящем изобретении, можно применять фармацевтически приемлемые соли, которые включают, например, соли минеральных кислот, такие как гидрохлориды, гидробромиды, фосфаты, сульфаты и т.п.; и соли органических кислот, такие как ацетаты, пропионаты, малонаты, бензоаты и т.п. Подробное описание фармацевтически приемлемых эксципиентов и солей можно найти в Remington's Pharmaceutical Sciences, 18-е изд. (Истон, шт.Пенсильвания, изд-во Mack Publishing Company, 1990).
Кроме того, в составе таких носителей могут присутствовать вспомогательные вещества, такие как смачивающие или эмульгирующие агенты, биологические забуферивающие вещества, поверхностно-активные вещества и т.п. Биологический буфер может представлять собой практически любой раствор, который является фармакологически приемлемым и с помощью которого обеспечивают требуемое значение рН композиции, т.е. значение рН в физиологически приемлемом диапазоне. Примерами буферных растворов являются физиологический раствор, забуференный фосфатом физиологический раствор, забуференный трис физиологический раствор, забуференный соляной раствор Хэнкса и т.п.
В зависимости от предполагаемого пути введения фармацевтические композиции могут представлять собой твердые, полутвердые или жидкие лекарственные формы, такие, например, как таблетки, суппозитории, пилюли, капсулы, порошки, жидкости, суспензии, кремы, мази, лосьоны или т.п., предпочтительно в виде стандартных доз, предназначенных для однократного введения точной дозы. Композиции должны содержать эффективное количество требуемого лекарственного средства в сочетании с фармацевтически приемлемым носителем и, кроме того, могут содержать другие фармацевтические агенты, адъюванты, разбавители, буферы и т.д.
Для твердых композиций стандартными нетоксическими твердыми носителями являются, например, имеющие фармацевтическую чистоту маннит, лактоза, крахмал, стеарат магния, сахарин натрия, тальк, целлюлоза, глюкоза, сахароза, карбонат магния и т.п. Вводимые жидкие фармацевтические композиции можно приготавливать, например, путем растворения, диспергирования и т.д. указанного в настоящем описании действующего вещества и необязательных фармацевтических адъювантов в эксципиенте, таком, например, как вода, физиологический раствор, водная декстроза, глицерин, этанол и т.п., получая раствор или суспензию. При необходимости предназначенная для введения фармацевтическая композиция может содержать также небольшие количества нетоксичных вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, забуферивающие агенты для регулирования значения рН и т.п., например ацетат натрия, сорбитанмонолаурат, триэтаноламинацетат натрия, триэтаноламинолеат и т.д. Применяемые на практике методы получения таких лекарственных средств являются известными или они очевидны специалистам в данной области (см., например, цитированный выше справочник).
Предназначенная для орального введения композиция, как правило, находится в форме таблетки, капсулы, мягкой гелевой капсулы или может находиться в форме водного или неводного раствора, суспензии или сиропа. Предпочтительными формами для орального введения являются таблетки и капсулы. Таблетки и капсулы для орального введения, как правило, содержат один или несколько стандартных носителей, таких как лактоза и кукурузный крахмал. Как правило, добавляют замасливатели, такие как стеарат магния. Если применяют жидкую суспензию, то действующее вещество можно объединять с эмульгирующими и суспендирующими агентами. При необходимости можно добавлять также корригенты, красители и/или подслащивающие вещества. Другие необязательные компоненты, которые могут входить в оральную композицию, включают (но, не ограничиваясь ими) консерванты, суспендирующие агенты, загустители и т.п.
Парентеральные композиции можно приготавливать в стандартных формах либо в виде жидких растворов или суспензий, твердых форм, пригодных для солюбилизации или суспендирования перед инъекцией, либо в виде эмульсий. Предпочтительно с помощью методов, известных в данной области, приготавливают стерильные суспензии для инъекции с использованием пригодных носителей, диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильная композиция для инъекции может представлять собой также стерильный раствор или суспензию для инъекции в нетоксическом приемлемом для парентерального введения разбавителе или растворителе. К приемлемым носителям и растворителям, которые можно применять, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителей или суспендирующих сред, как правило, применяют стерильные жирные масла, эфиры жирных кислот или полиолы. Кроме того, парентеральное введение можно осуществлять с использованием системы с замедленным высвобождением или пролонгированным высвобождением так, чтобы поддерживать постоянный уровень дозы лекарственного средства.
В альтернативном варианте фармацевтические композиции, предлагаемые в изобретении, можно вводить в форме суппозиториев для ректального введения. Их можно приготавливать путем смешения действующего вещества с пригодным не вызывающим раздражения эксципиентом, который находится в твердом состоянии при комнатной температуре, но превращается в жидкость при температуре в прямой кишке и поэтому расплавляется в прямой кишке с высвобождением лекарственного средства. К таким материалам относятся кокосовое масло, пчелиный воск и полиэтиленгликоли.
Фармацевтические композиции, предлагаемые в изобретении, можно вводить также с помощью назального аэрозоля или путем ингаляции. Такие композиции получают с помощью методов, хорошо известных в области приготовления фармацевтических композиций и их можно приготавливать в виде растворов в физиологическом растворе с использованием бензилового спирта или других приемлемых консервантов, стимуляторов абсорбции для повышения биологической доступности, пропеллентов, таких как фторированные углеводороды или азот, и/или других стандартных солюбилизирующих или диспергирующих агентов.
Предпочтительными композициями для местного применения лекарственного средства являются мази и кремы. Мази представляют собой полутвердые препараты, как правило, на основе вазелина или других петролейных производных. Кремы, содержащие выбранное действующее вещество, как известно в данной области, представляют собой вязкую жидкость или полутвердые эмульсии либо типа масло-в-воде, либо типа вода-в-масле. Основы кремов могут смываться водой и, как правило, они содержат масляную фазу, эмульгатор и водную фазу. Масляная фаза, которую иногда называют также "внутренней" фазой, как правило, состоит из вазелина и жирного спирта, такого как цетиловый или стеариловый спирт; водная фаза, как правило, хотя это и не является необходимым, превосходит по объему масляную фазу и, как правило, содержит увлажнитель. Эмульгатор в композиции в виде крема, как правило, представляет собой неионогенное, анионогенное, катионогенное или амфотерное поверхностно-активное вещество. В качестве конкретной основы, предназначенной для приготовления мази или крема, как это должно быть очевидно специалистам в данной области, следует применять такой продукт, который обеспечивает оптимальное введение лекарственного средства. Так же, как и другие носители или наполнители, основа для приготовления мази должна быть инертной, стабильной, не вызывать раздражение и сенсибилизацию.
Композиции для буккального введения представляют собой таблетки, пастилки, гели и т.п. В альтернативном варианте буккальное введение можно осуществлять с использованием известной специалистам в данной области системы введения через слизистую оболочку. Соединения, предлагаемые в изобретении, можно вводить также через кожу или слизистую ткань с помощью стандартных систем трансдермального введения лекарственного средства, т.е. трансдермальных "бляшек", в которых действующее вещество, как правило, содержится в ламинированной структуре, служащей в качестве устройства для введения лекарственного средства, которую прикрепляют к поверхности тела. В такой структуре композиция лекарственного средства, как правило, содержится в слое или "резервуаре", расположенном под верхним защитным слоем. Ламинированное устройство может содержать один резервуар или оно может содержать несколько резервуаров. В одном из вариантов осуществления изобретения резервуар представляет собой полимерный матрикс из фармацевтически приемлемого обеспечивающего контакт адгезива, который служит для прикрепления системы к коже в процессе введения лекарственного средства. Примерами пригодных обеспечивающих контакт с кожей адгезивов являются (но, не ограничиваясь ими) полиэтилены, полисилоксаны, полиизобутилены, полиакрилаты, полиуретаны и т.п. В альтернативном варианте содержащий лекарственное средство резервуар и обеспечивающий контакт с кожей адгезив представляют собой раздельные и имеющие различную структуру слои, причем адгезив, который находится под резервуаром, в этом случае может представлять собой описанный выше полимерный матрикс или может представлять собой содержащий жидкость или гель резервуар, или может иметь какую-то иную форму. Защитный слой в таких слоистых конструкциях, который служит в качестве верхней поверхности устройства, играет роль основного структурного элемента ламинированной структуры и придает устройству основную часть гибкости. Материал, который выбирают для защитного слоя, должен быть практически непроницаемым для действующего вещества и других присутствующих продуктов.
Пациенту следует вводить фармацевтически или терапевтически эффективное количество композиции. Точное эффективное количество должно варьироваться от индивидуума к индивидууму и должно зависеть от вида, возраста, размеров индивидуума и его состояния здоровья, природы и серьезности подлежащего лечению состояния, рекомендаций лечащего врача и лекарственных средств или комбинации лекарственных средств, выбранных для лечения. Эффективное количество в конкретной ситуации можно выбирать с помощью стандартных экспериментов. Для цели настоящего изобретения терапевтическое количество, как правило, составляет от примерно 0,05 до примерно 40 мг/кг веса тела, более предпочтительно от примерно 0,5 до примерно 20 мг/кг, в виде по меньшей мере одной дозы. Для крупных млекопитающих показанные суточные дозы могут составлять от примерно 1 до 100 мг, которые вводят один или несколько раз в день, более предпочтительно от примерно 10 до 50 мг. Индивидууму можно вводить такое количество доз, которое требуется для уменьшения и/или облегчения признаков, симптомов или причин рассматриваемого нарушения или для любого иного требуемого изменения биологической системы.
Введение полинуклеотидов, например введение антисмысловых олигонуклеотидов 15-липоксигеназы можно осуществлять с использованием любой описанной выше композиции или с использованием рекомбинантных экспрессионных векторов с применением в качестве носителей вирусов или частиц или без них. Такие методы известны в данной области (см., например, U.S.  6214804; 6147055; 5703055; 5589466; 5580859; Slater и др., J._Allergy Clin. Immunol. 102: cc.469-475, 1998). Например, введение полинуклеотидных последовательностей можно осуществлять с помощью различных вирусных векторов, включая ретровирусные и аденоассоциированные вирусные векторы (см., например. Miller A.D., Blood 76: с.271, 1990; и Uckert и Walther, Pharmacol. Ther. 63: cc.323-347, 1994). Векторы, которые можно применять для антисмысловой генной терапии, включают (но, не ограничиваясь ими) аденовирусы, вирусы герпеса, вирус коровьей оспы или предпочтительно РНК-овые вирусы, такие как ретровирусы. Другие механизмы введения генов, которые можно применять для введения полинуклеотидных последовательностей в клетки-мишени, включают коллоидную дисперсию и системы на основе липосом, искусственные вирусные оболочки и другие системы, доступные специалисту в данной области (см., например, Rossi, J.J., Br. Med. Bull. 51: cc.217-225, 1995; Morris и др., Nucl. Acids Res. 25: cc.2730-2736, 1997; и Boado и др., J. Pharm. Sci. 87: cc.1308-1315, 1998). Например, в качестве систем введения можно применять комплексы макромолекул, нанокапсулы, микросферы, гранулы и основанные на липидах системы, включая эмульсии типа масло-в-воде, мицеллы, смешанные мицеллы и липосомы. 6214804; 6147055; 5703055; 5589466; 5580859; Slater и др., J._Allergy Clin. Immunol. 102: cc.469-475, 1998). Например, введение полинуклеотидных последовательностей можно осуществлять с помощью различных вирусных векторов, включая ретровирусные и аденоассоциированные вирусные векторы (см., например. Miller A.D., Blood 76: с.271, 1990; и Uckert и Walther, Pharmacol. Ther. 63: cc.323-347, 1994). Векторы, которые можно применять для антисмысловой генной терапии, включают (но, не ограничиваясь ими) аденовирусы, вирусы герпеса, вирус коровьей оспы или предпочтительно РНК-овые вирусы, такие как ретровирусы. Другие механизмы введения генов, которые можно применять для введения полинуклеотидных последовательностей в клетки-мишени, включают коллоидную дисперсию и системы на основе липосом, искусственные вирусные оболочки и другие системы, доступные специалисту в данной области (см., например, Rossi, J.J., Br. Med. Bull. 51: cc.217-225, 1995; Morris и др., Nucl. Acids Res. 25: cc.2730-2736, 1997; и Boado и др., J. Pharm. Sci. 87: cc.1308-1315, 1998). Например, в качестве систем введения можно применять комплексы макромолекул, нанокапсулы, микросферы, гранулы и основанные на липидах системы, включая эмульсии типа масло-в-воде, мицеллы, смешанные мицеллы и липосомы.
Как указано выше, фармацевтические композиции могут содержать одно или несколько действующих веществ, обладающих способностью эффективно регулировать гомеостаз кальция. Дополнительное действующее вещество может представлять собой (но, не ограничиваясь ими) эстроген, кальцитонин, бисфосфонат (например, алендронат, резидронат, золендронат и ибандронат), витамин D3 или его аналог, андроген, соль фтора, паратиреоидный гормон или его аналог, или IGF, агенты, которые изменяют регуляцию транскрипции встречающихся в естественных условиях регуляторов гормонов, которые участвуют в метаболизме костной ткани, и их комбинации. Такое дополнительное действующее вещество можно вводить индивидууму до, одновременно или после введения ингибитора 15-липоксигеназы, предлагаемого в настоящем изобретении.
Другой объект настоящего изобретения основан на открытии корреляции между полиморфизмом гена 15-липоксигеназы и минеральной плотностью костной ткани, причем было установлено, что наличие определенных полиморфизмов коррелирует с уменьшенной минеральной плотностью костной ткани. Еще один объект изобретения заключается в том, что генотип коррелирует с предрасположенностью к остеопорозу. Преимуществом изобретения является то, что путем скрининга в отношении наличия определенного генотипа можно выявлять индивидуумов, которые, по-видимому, имеют такую генетическую предрасположенность. Таким образом, следующим объектом изобретения является способ терапевтического лечения, заключающийся в том, что осуществляют скрининг в отношении предрасположенности индивидуума к потере костной ткани и, если предрасположенность выявлена, то такого индивидуума лечат с целью замедления или уменьшения или предупреждения потери костной ткани.
Согласно способу диагностики и прогнозирования, предлагаемому в настоящем изобретении, выявляют изменения, включая делеции, инсерции и точечные мутации в кодирующих и некодирующих областях локуса 15-липоксигеназы дикого типа. Так, например, у мышей предпочтительно выявляют изменения на хромосоме 11, тогда как у людей выявляют изменения на хромосоме 17. Кроме того, способ можно осуществлять путем выявления локуса 15-липоксигеназы дикого типа и подтверждения отсутствия предрасположенности к нарушениям, обусловливающим потерю костной ткани, которые вызываются локусом 15-липоксигеназы. Наличие таких мутаций у индивидуумов может как сопровождаться симптомами потери костной ткани, так и не сопровождаться ими. Кроме того, могут существовать различия в реакции на лекарственное средство или прогнозе симптомов у индивидуумов, которые несут мутации в локусе 15-липоксигеназы, по сравнению с теми, которые не имеют таких мутаций.
Таким образом, одним из объектов изобретения является способ диагностики, заключающийся в том, что определяют генотип гена 15-липоксигеназы. Как правило, согласно способу определяют, является ли индивидуум гомозиготным или гетерозиготным в отношении полиморфизма гена 15-липоксигеназы. Как правило, способ, предлагаемый в изобретении, осуществляют путем анализа in vitro клеток индивидуума с целью определения генотипа, указанного индивидуума в локусе гена 15-липоксигеназы.
Диагностические методы, которые можно применять, включают (но, не ограничиваясь ими) анализ микрорядов, флуоресцентную гибридизацию in situ (FISH), непосредственное секвенирование ДНК, PFGE-анализ, анализ методом Саузерн-блоттинга, одноцепочечный конформационный анализ (SSCA), анализ защиты от РНКазы, анализ с использованием аллель-специфического олигонуклеотида (АСО), анализ методом дот-блоттинга и ПЦР-SSCP, которые известны в данной области.
Предрасположенность к заболеванию, сопровождающемуся потерей костной ткани, можно оценивать путем тестирования любой ткани индивидуума, такого как больной человек, в отношении мутаций гена 15-липоксигеназы. Например, индивидуум, несущий врожденную мутацию 15-липоксигеназы в зародышевой линии, может быть предрасположен к развитию заболевания, сопровождающегося потерей костной ткани. Это можно определять путем тестирования ДНК из любой ткани организма индивидуума. Наиболее просто отбирать образцы крови и экстрагировать ДНК из клеток крови. Кроме того, можно осуществлять пренатальный диагноз путем тестирования клеток эмбриона, клеток плаценты или амниотических клеток в отношении мутации гена 15-липоксигеназы. С помощью любого из изложенных в настоящем описании методов можно обнаруживать изменение аллеля 15-липоксигеназы дикого типа, обусловленные, например, точечной мутацией или делецией.
Существует несколько методов, которые можно применять для обнаружения вариации последовательности ДНК. Вариацию последовательности можно обнаруживать прямым секвенированием ДНК, либо секвенированием, осуществляемым вручную, либо автоматизированным флуоресцентным секвенированием. Другим подходом является одноцепочечный конформационный анализ (SSCA), в котором секвенируют фрагменты со смещенной подвижностью на гелях для SSCA для определения истинной природы вариации последовательности ДНК. Другие подходы, основанные на обнаружении участка с неспаренными основаниями для двух комплементарных цепочек ДНК, включают пульсирующий денатурирующий градиентный гель-электрофорез (CDGE), анализ гетеродуплексов (НА) и химическое расщепление в сайтах ошибочных нуклеотидов (CMC). Если мутация известна, то для быстрого скрининга большого количества образцов в отношении именно этой мутации можно использовать специфичный в отношении аллеля метод обнаружения, такой как гибридизация аллель-специфических олигонуклеотидов (АСО) (см., например, Saiki и др., Proc. Nad. Acad. Sci. USA 86: cc.6230-6234, 1989).
Обнаружение точечных мутаций можно осуществлять путем молекулярного клонирования аллеля(ей) 15-липоксигеназы и секвенирования аллеля(ей) с помощью известных в данной области методов. В альтернативном варианте последовательности генов можно амплифицировать с помощью известных методов непосредственно с использованием препаратов геномной ДНК из ткани. Затем можно определять последовательность ДНК амплифицированных последовательностей. Присутствие аллеля можно подтверждать с помощью одноцепочечного конформационного анализа (SSCA), денатурирующего градиентного гель-электрофореза (DGGE или CDGE), анализа защиты от РНКазы, использования аллель-специфических олигонуклеотидов (АСО), аллель-специфической ПЦР или анализа удлинения на один нуклеотид, известных в данной области.
Согласно предпочтительному методу аллели идентифицируют с помощью метода микрочипов. Согласно этому методу тысячи различных олигонуклеотидных зондов или генов можно синтезировать (U.S. No. 5412087 на имя McGall и др.) или наносить рядами в виде капель (U.S. No. 6110426 на имя Shalon и др.) на силиконовый или стеклянный чип. Предназначенную для анализа нуклеиновую кислоту, как правило флуоресцентно метят и гибридизуют с зондами на чипе. В качестве других меток могут служить 32Р и биотин. С использованием таких рядов микрорядов капель можно изучать также взаимодействия нуклеиновая кислота-протеин. С помощью этого метода выявляют наличие мутаций в гене 15-липоксигеназы.
Присутствие измененного (или мутантного) гена 15-липоксигеназы коррелирует с повышенным риском заболевания, связанного с потерей костной ткани. Для обнаружения мутации гена 15-липоксигеназы приготавливают биологический образец и анализируют в отношении различия между последовательностью подлежащего анализу аллеля 15-липоксигеназы и последовательностью аллеля 15-липоксигеназы дикого типа. Затем мутантные аллели можно подвергать секвенированию для идентификации специфических мутаций конкретного мутантного аллеля. После этого мутации гена 15-липоксигеназы, конкретно на хромосоме 11 мыши и хромосоме 17 человека используют в методах диагностики и прогнозирования, предлагаемых в настоящем изобретении.
Таким образом, объектом настоящего изобретения является также способ диагностики предрасположенности к потере костной ткани у индивидуума, заключающийся в том, что выявляют полиморфизм человеческой хромосомы 17, где полиморфизм является критерием предрасположенности к потере костной ткани. В предпочтительном варианте осуществления изобретения для обнаружения используют генотипирование. В более предпочтительном варианте осуществления изобретения генотипирование включает использование микросателлитных маркеров или одного или нескольких однонуклеотидных полиморфизмов.
Другим объектом настоящего изобретения является способ диагностики предрасположенности к потере костной ткани у индивидуума, заключающийся в том, что у индивидуума выявляют полиморфизм гена 15-липоксигеназы.
В настоящем изобретении предложены ингибиторы 15-липоксигеназы для применения в качестве терапевтических действующих веществ для предупреждения потери костной ткани. Объектом изобретения являются также соединения, идентифицированные с помощью описанных выше способов. Кроме того, предложена фармацевтическая композиция, предназначенная, в частности, для предупреждения потери костной ткани, которая содержит описанное выше соединение и носитель. Предложен также набор для диагностики предрасположенности к потере костной ткани, содержащий по меньшей мере один олигонуклеотид, предназначенный для обнаружения полиморфизма гена 15-липоксигеназы, связанного с потерей костной ткани.
Наконец, объектами изобретения являются также соединения, способы, применения, композиция и набор, в основном представленные в настоящем описании, прежде всего в предшествующих примерах.
На фиг.1 проиллюстрировано сравнение основанного на генотипировании SNP пулированных образцов ДНК с полученными микросателлитным генотипированием образцами ДНК для обнаружения полиморфизмов, связанных с минеральной плотностью костной ткани. Статистическую значимость каждого различия встречаемости аллеля рассчитывали с использованием z-критерия и строили график зависимости логарифма отношения вероятностей (LOD) для всех хромосом. Штриховая линия, соответствует величине LOD 3,3, которая была выбрана в качестве предельного значения для определения статистически достоверного различия геномов.
На фиг.2 - количественная оценка экспрессии гена Alox15 в почке мыши, полученная на основе анализа полной РНК почки, где экспрессию гена анализировали с использованием микрорядов.
На фиг.3 - количественная оценка экспрессии гена ALox15 в первичных мышиных остеобластах в зависимости от возрастающих концентраций IL-4, вводимого in vitro.
На фиг.4 - положение полиморфизмов отдельного нуклеотида (SNP), идентифицированных в гене ALox15 мышей.
На фиг.5 - количественная оценка активности щелочной фосфатазы в человеческих мезенхимальных стволовых клетках (hMSC) при воздействии ингибиторов 15-липоксигеназы, представляющих собой соединение 1 или соединение 2, в сравнении с воздействием только растворителя (ДМСО).
На фиг.6 - количественная оценка активности щелочной фосфатазы в hMSC при использовании ингибиторов 15-липоксигеназы соединения 3 или соединения 2 и в качестве контролей ДМСО или 1,25-витамина D3.
На фиг.7 - количественная оценка содержания общего кальция в hMSC при использовании ингибиторов 15-липоксигеназы соединения 3 или соединения 2 и в качестве контролей ДМСО или 1,25-витамина D3.
На фиг.8 - количественная оценка активности щелочной фосфатазы в hMSC после культивирования в течение 9 дней в присутствии ингибиторов 5-ЛО Zileuton, AA-861 и Rev-5901 в сравнении с одним растворителем (ДМСО), применяемым в качестве контроля. Отсутствие реакции представляет собой характерное отличие от случаев применения ингибиторов 15-липоксигеназы.
На фиг.9 - количественная оценка содержания общего кальция в hMSC при культивировании в течение 16 дней в присутствии ингибиторов 5-ЛО Zileuton, AA-861 и Rev-5901 в сравнении с одним растворителем (ДМСО) или 1,25-витамина D3 в качестве контролей. В отличие от случаев применения ингибиторов 15-липоксигеназы реакция отсутствует.
Ниже описаны конкретные примеры осуществления настоящего изобретения. Примеры приведены только с целью иллюстрации и никоим образом не направлены на ограничение объема настоящего изобретения.
Соединение  |
Структура |
IC50 для 15-ЛО |
| 1 |
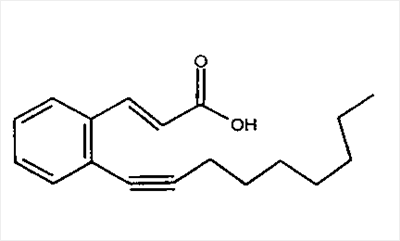 |
1-3 мкМ |
| 2 |
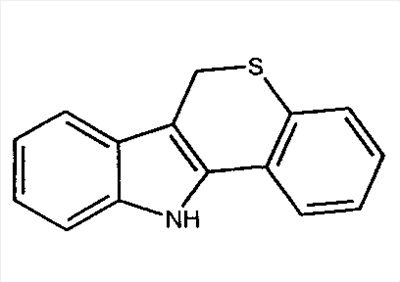 |
~200 нМ |
| 3 |
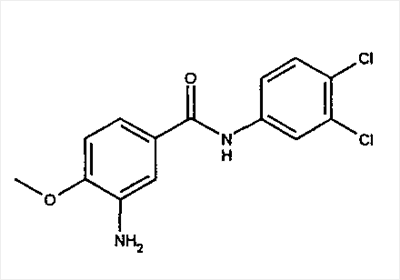 |
~10 нМ |
| 4 |
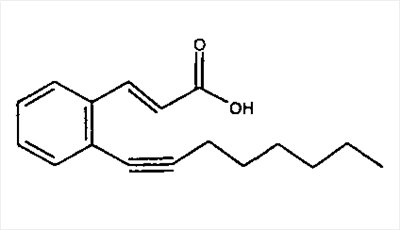 |
1-3 мкМ |
| 5 |
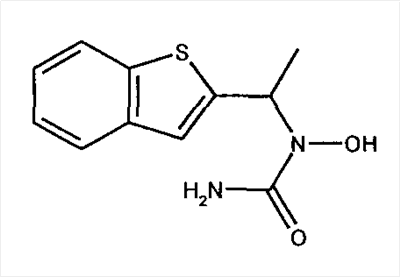 |
Отрицательный контроль |
| 6 |
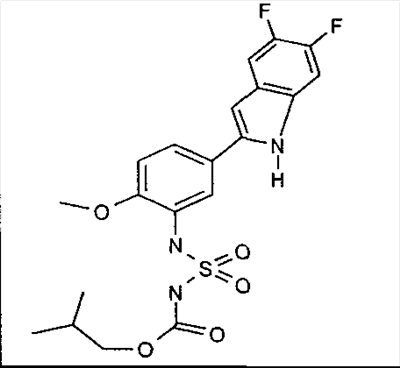 |
25-83 нМ |
Соединение 1, представляющее собой 3-(2-нон-1-инилфенил)пропионовую кислоту, описанное в U.S.  5972980. 5972980.
Соединение 2, представляющее собой 6,11-дигидо-5-тиа-11-аза-бензо[а]флуорен, описанное в WO 97/12613.
Соединение 3, представляющее собой 3-амино-N-(3,4-дигидрофенил)-4-метоксибензамид, описанное в WO 99/32433.
Соединение 4, представляющее собой транс-3-(2-окт-1-инилфенил)акриловую кислоту, описанное в U.S.  4713486. 4713486.
Соединение 5, представляющее собой Zilueton, описанное в U.S.  4873259. 4873259.
Соединение 6, представляющее собой изобутиловый эфир [[[5-(5,6-дифтор-1Н-индол-2-ил)-2-метоксифенил]амино]сульфонил]карбаминовой кислоты, описанное в WO 01/96298.
Были предприняты усилия для обеспечения точности указанных в описании численных значений (например, количеств, температур и т.д.), однако, конечно, следует иметь в виду, что допустимы некоторые экспериментальные погрешности и отклонения.
Пример 1
Модели генотипирования полиморфизма отдельного нуклеотида (SNP).
Микросателлиты (которые называют также полиморфизмами одиночного тандемного повтора или одиночными полиморфизмами длины последовательности) представляют собой наиболее изученную категорию генетических маркеров. Они включают малые ряды тандемных повторов небольших последовательностей (ди-, три-, тетра-нуклеотидные повторы), которые обладают большой степенью полиморфизма длины, что обеспечивает высокий уровень информации. В человеческом геноме расположено немного более 5000 микросателлитов, которые легко типировать с помощью методов на основе ПЦР (Dib и др., Nature 380: cc.152, 1996).
Как правило, применяют метод, описанный Grupe и др., Science 292: cc.1915-1918, 2001. Для идентификации генетических факторов, регулирующих МПК, осуществляли сканирование генома на 1000 представителях поколения F2 интеркросса C57BL/6 × DBA/2 (фирма Jackson Labs, Бар Харбор, шт.Мэн) 16-недельного возраста. Поколение F2 имело не сцепленное с полом нормальное распределение МПК (Grupe и др., Science, 292, cc.1915-1918, 2001). Обладающих экстремальным фенотипом представителей потомства F2 с наибольшим (n=145) и наименьшим (n=149) МПК (в пределах 15% от высшей и низшей оценок) подвергали полному сканированию генома для выявления связи МПК путем генотипирования индивидуальных образцов ДНК с использованием 100 микросателлитных маркеров. Кроме того, путем отбора равных количеств ДНК из представителей потомства F2 с высокой и низкой величиной МПК получали два пула. Для 109 SNP, обнаруженных в базе данных mSNP, измеряли с помощью аллель-специфической кинетической ПЦР частоты встречаемости аллелей в образцах, входящих в пулы. Для каждого маркера оценивали разницу в частоте встречаемости аллелей в двух экстремальных пулах. Если маркер не связан с МПК, то его ожидаемая частота составляет 50% для обоих экстремальных пулов. Статистическую значимость каждой разницы частоты встречаемости аллеля рассчитывали с использованием z-критерия и строили график зависимости логарифма отношения вероятностей (LOD) (фиг.1). Для четырех областей, расположенных на хромосомах 1, 2, 4 и 11, с помощью методов, основанных на использовании микросателлитов и генотипирования SNP, была выявлена статистически значимая связь (балл LOD>3,3).
Таким образом, с помощью метода SNP-генотипирования выявляли гены-кандидаты, которые могут обусловливать МПК.
Пример 2
Модели с использованием животных
Для идентификации гена внутри выявленной области на хромосоме 11, который регулирует МПК, осуществляли с использованием микрорядов анализ разницы экспрессии гена в организме мышей штамма DBA/2, C57BL6/J (фирма Jackson Labs, Бар Харбор, Майн) и конгенного штамма мышей (D2.B6chr11, полученного от Oregon Health Sciences University). Конгенные мыши линии D2.B6chr11 несли участок от сМ20 до сМ50 хромосомы 11 C57BL/6J, интрогрессированный в основу геномной линии DBA2/J. Микроряды, содержащие гены мышиного генома, гибридизовали с меченой кРНК, полученной из целых почек, культивированных первичных остеобластов и первичных хондроцитов. Гибридизацию осуществляли с кРНК, полученной из мышей индивидуальных линий DBA/2J, C57BL/6J и конгенных мышей линии B6.D2chr11. Осуществляли выделение мРНК (2х ро1у(А)+), синтез кРНК и гибридизацию. Дифференциальную экспрессию оценивали путем парного сравнения мышей линий DBA/2J и C57BL/6 и путем парного сравнения мышей линии DBA/2J и конгенной линии B6.D2chr11.
Для дальнейшего определения характеристик выбирали дифференцирование экспрессируемые гены, кодируемые внутри интервала сМ20-сМ50 на хромосоме 11. Было установлено существенное различие экспрессии индивидуального гена (ALox15, расположенный в сМ 40 на хромосоме 11) двумя изученными линиями (фиг.2). Для линии DBA/2J были характерны повышенные уровни экспрессии ALox15 по сравнению с линией D2.B6chr11 и мышами линии C57BL/6J, а также пониженный уровень МПК по сравнению с обеими другими линиями. Таким образом, повышенная экспрессия ALox15 у мышей линии DBA/2J связана с пониженной минеральной плотностью костной ткани.
Дифференциальную экспрессию мРНК ALox15 в остеобластах оценивали с помощью ПЦР в реальном времени. Клетки получали из мышей линий DBA/2J, C57BL/6J и D2.B6chr11 (фиг.3). Общую РНК обрабатывали ДНКазой I для удаления примеси геномной ДНК. РНК выдерживали при 65°С в течение 10 мин для инактивации ДНКазы I. Все ПЦР осуществляли в объеме 100 мкл. РНК (100 нг) подвергали ОТ-ПЦР с использованием ДНК-полимеразы rTh (2 единицы) (фирма Perkin Elmer) в реакционной смеси, содержащей 5×EZ-буфер, Mn(ОАс) (3 мМ), этидийбромид (1 мкг/мкл), дНТФ (200 мкМ), прямой праймер (200 нМ) и обратный праймер (200 нМ). кДНК получали путем инкубации образцов в течение 30 мин при 60°С. После этого осуществляли 60 циклов ПЦР (95°С, 20 с; 58°С, 20 с) и затем инкубировали в течение 20 мин при 72°С. Флуоресценция на каждом цикле связана с количеством образовавшегося продукта и ее измеряли с помощью кинетической термоячейки и анализировали с использованием имеющегося программного обеспечения (Germer и Higuchi, Genome Research, 9, cc.72-78, 1999). Кроме клеток почек остеобласты мышей линии DBA/2J продуцировали также повышенные уровни мРНК ALox15 по сравнению с мышами линии C57BL/6J. РНК ALox15 индуцировалась с помощью IL-4 в остеобластах мышей линии C57BL/6 в большей степени, чем у мышей линии DBA/2 (фиг.3).
Для выявления молекулярной основы штаммоспецифической разницы экспрессии ALoxl5 осуществляли с помощью методов, известных в данной области, секвенирование геномной ДНК гена ALox15 мышей линий DBA/2J и C57BL6/J. Были выявлены 14 полиморфизмов последовательности ДНК, характеризующих различия двух штаммов (представлены в виде диаграммы на фиг.4 и в таблице 1 ниже). Ген Ensembi 15LO обозначен как ENSMUSG000000 18924. Генная последовательность, простирающаяся от положения 70929619 до 70937482 мышиного генома, представлена в Seq ID  1. Первый SNP в таблице 1, имеющий положение 70938498 в последовательности мышиного генома, локализован в положении 541 последовательности, помещенной в Genbank под регистрационным номером 1. Первый SNP в таблице 1, имеющий положение 70938498 в последовательности мышиного генома, локализован в положении 541 последовательности, помещенной в Genbank под регистрационным номером  U04332, которая представлена в Seq ID U04332, которая представлена в Seq ID  2. 2.
| Таблица 1 |
| Сравнение SNP Alox15, идентифицированных у мышей линии DBA/2J, с мышами линии C57BL/6J. |
| Положение SNP в мышином геноме (пары оснований) |
Замена нуклеотида C57BL/6J_DBA2/J |
Интрон/экзон |
Положение аминокислот |
| 70938498 |
C_G |
~1 т.п.н. против хода транскрипции относительно ТАТА-бокса в 5' utr |
| 70937181 |
A_G |
Интрон 1 |
 |
| 70936977 |
Т_С |
Интрон 1 |
 |
| 70936975 |
A_T |
Интрон 1 |
 |
| 70936918 |
С_Т |
Интрон 1 |
 |
| 70936336 |
T_C |
Экзон 2 |
62/Phe(TTT)_Phe(TTC) |
| 70936248 |
G_A |
Экзон 2 |
91/Ser(TCG)_Ser(TCA) |
| 70936136 |
G_A |
Интрон 2 |
 |
| 70935775 |
G_A |
Интрон 3 |
 |
| 70935765 |
С_Т |
Интрон 3 |
 |
| 70931174 |
А_G |
Интрон 10 |
 |
| 70930258 |
А_G |
Интрон 13 |
 |
| 70930156 |
С_Т |
Экзон 14 |
616/Pro(CCA)_Ser(TCA) |
| 70930151 |
C_T |
Экзон 14 |
617/Asn(AAC)_.Asn(AAT) |
| 70929999 |
Делец. Т в DBA/2J DBA/2J |
11-е основание 3' utr |
Пример 3
Способность ингибиторов 15-липоксигеназы увеличивать образование костной ткани
Для определения способности ингибиторов 15-липоксигеназы стимулировать образование костной ткани и накопление костной ткани в опытах in vitro оценивали способность ингибиторов 15-ЛО увеличивать уровень дифференцировки стволовых клеток в костеобразующие клетки (остеобласты). В частности, с помощью измерения двух маркеров дифференцировки в остеобласты, активности клеточной щелочной фосфатазы и содержания кальция в культуре оценивали способность трех ингибиторов, а именно соединения 1-3-(2-нон-1-инилфенил)пропионовая кислота), соединения 2 (6,11-дигидро-5-тиа-11-азабензо [а]флуорен) и соединения 3 (3-амино-N-(3,4-дихлорфенил)-4-метоксибензамид), полученных согласно методам, описанным в литературе, стимулировать дифференцировку человеческих мезенхимальных стволовых клеток в остеобласты.
В целом метод заключался в том, что человеческие мезенхимальные клетки (hMSC, линия Poietics  РТ-2501, фирма Bio Whittaker) культивировали в 12-луночных покрытых коллагеном планшетах с плотностью 3100 клеток на 1 см2 в 1 мл культуральной среды (фирма Clonetics, каталожный номер РТ-4105), дополненной индукторами остеобластов (100 нМ Dex, 0,05 мМ L-аскорбиновая кислота-2-фосфат, 10 мМ бетаглицеринфосфат). К каждой культуре добавляли индивидуально три ингибитора 15-ЛО за исключением контрольных лунок, в которые добавляли 0,1% ДМСО (отрицательный контроль) или 1 нМ 1,25-витамин D3 (положительный контроль). Использовали следующие концентрации ингибиторов: для соединения 1 - 3 и 30 мкМ; для соединения 2 - 0,1, 0,2, 0,3 или 1,0 мкМ и для соединения 3 - 3, 10 или 30 мкМ. Для каждого уровня дозы приготавливали от 4 до 8 независимых репликативных культур. По окончании эксперимента выращенные клетки собирали путем соскабливания из лунок и вносили в соответствующую среду для проведения дальнейшего анализа либо активности щелочной фосфатазы (фирма Sigma, набор РТ-2501, фирма Bio Whittaker) культивировали в 12-луночных покрытых коллагеном планшетах с плотностью 3100 клеток на 1 см2 в 1 мл культуральной среды (фирма Clonetics, каталожный номер РТ-4105), дополненной индукторами остеобластов (100 нМ Dex, 0,05 мМ L-аскорбиновая кислота-2-фосфат, 10 мМ бетаглицеринфосфат). К каждой культуре добавляли индивидуально три ингибитора 15-ЛО за исключением контрольных лунок, в которые добавляли 0,1% ДМСО (отрицательный контроль) или 1 нМ 1,25-витамин D3 (положительный контроль). Использовали следующие концентрации ингибиторов: для соединения 1 - 3 и 30 мкМ; для соединения 2 - 0,1, 0,2, 0,3 или 1,0 мкМ и для соединения 3 - 3, 10 или 30 мкМ. Для каждого уровня дозы приготавливали от 4 до 8 независимых репликативных культур. По окончании эксперимента выращенные клетки собирали путем соскабливания из лунок и вносили в соответствующую среду для проведения дальнейшего анализа либо активности щелочной фосфатазы (фирма Sigma, набор  104-LL), либо содержания клеточного кальция (фирма Sigma, набор 104-LL), либо содержания клеточного кальция (фирма Sigma, набор  587-М). Культуры, предназначенные для анализа щелочной фосфатазы, собирали путем соскабливания клеток и ресуспендировали в 250 мкл забуференного Трис 0,1%-ного тритона Х-100 и затем подвергали анализу либо в свежем виде, либо после оттаивания замороженных культур. Отдельно отбирали культуры, предназначенные для анализа содержания общего кальция и ресуспендировали в 250 мкл 0,5М HCL. Результаты этих анализов стандартизовали по отношению к содержанию общей клеточной ДНК, стандартизуя тем самым различия пролиферации клеток. Одновременно путем соскабливания клеток собирали раздельно репликативные культуры, предназначенные для анализа щелочной фосфатазы и кальция, и ресуспендировали их в 250 мкл сбалансированного солевого раствора Хэнкса и оценивали количество клеток с помощью ДНК (набор DNeasy Tissue Kit, фирма Qiagen, каталожный номер 69506). 587-М). Культуры, предназначенные для анализа щелочной фосфатазы, собирали путем соскабливания клеток и ресуспендировали в 250 мкл забуференного Трис 0,1%-ного тритона Х-100 и затем подвергали анализу либо в свежем виде, либо после оттаивания замороженных культур. Отдельно отбирали культуры, предназначенные для анализа содержания общего кальция и ресуспендировали в 250 мкл 0,5М HCL. Результаты этих анализов стандартизовали по отношению к содержанию общей клеточной ДНК, стандартизуя тем самым различия пролиферации клеток. Одновременно путем соскабливания клеток собирали раздельно репликативные культуры, предназначенные для анализа щелочной фосфатазы и кальция, и ресуспендировали их в 250 мкл сбалансированного солевого раствора Хэнкса и оценивали количество клеток с помощью ДНК (набор DNeasy Tissue Kit, фирма Qiagen, каталожный номер 69506).
Количественная оценка дифференцировки в остеобласты in vitro.
Для количественной оценки активности щелочной фосфатазы приготавливали ингибиторы в 0,1% ДМСО и добавляли к культурам в день 1 и после этого в течение 14-16 дней через каждые 2-3 дня. Проводили три различные серии экспериментов.
В первой серии экспериментов в качестве ингибиторов использовали соединение 1 или соединение 2 (0,2 или 1 мкМ) и растворитель (ДМСО) в качестве отрицательного контроля, и для каждого уровня дозы приготавливали по четыре независимые репликативные культуры. Планшеты культивировали в течение 14 дней. Стандартизованная по ДНК активность щелочной фосфатазы представлена в виде графика на фиг.5.
Во второй серии экспериментов использовали по восемь репликативных культур и соединение 3 (3, 10 и 30 мкМ) или соединение 2 (0,1, 0,3, 1,0 мкМ) в качестве ингибиторов 15-ЛО. Ингибиторы добавляли либо в день 1, либо в день 11. В качестве отрицательного контроля использовали ДМСО, а 1,25-витамин D3 в качестве положительного контроля индукции дифференцировки в остеобласты. Стандартизованная активность щелочной фосфатазы и содержание кальция представлены в виде графиков на фиг.6 и 7 соответственно. Соединение 2 обладало наиболее высокой эффективностью при его добавлении в день 1, а соединение 3 обладало наибольшей эффективностью при его добавлении в день 11.
Для контроля специфичности ингибирования 15-ЛО в отношении индукции дифференцировки в остеокласты in vitro, в третьей серии экспериментов исследовали 8 образцов стандартных ингибиторов липоксигеназы, которые, как было установлено, обладают большей специфичностью в отношении фермента 5-ЛО, чем в отношении фермента 15-ЛО. Каждые 2-3 дня приготавливали свежие препараты Zileuton (1, 10, 50 мкМ, который получали от фирмы Roche), представляющий собой соединение 5, АА-861 (1, 10, 50 мкМ, фирма Sigma,  А3711) и Rev-5901 (15 мкМ, фирма Sigma, А3711) и Rev-5901 (15 мкМ, фирма Sigma,  R5523) и тестировали с использованием человеческих клеток-предшественников остеобластов. Было установлено, что ингибиторы 5-ЛО теряли способность индуцировать активность щелочной фосфатазы на день 9 или отложение кальция в культуре после культивирования в течение 16 дней, что проиллюстрировано на фиг.8 и 9 соответственно. R5523) и тестировали с использованием человеческих клеток-предшественников остеобластов. Было установлено, что ингибиторы 5-ЛО теряли способность индуцировать активность щелочной фосфатазы на день 9 или отложение кальция в культуре после культивирования в течение 16 дней, что проиллюстрировано на фиг.8 и 9 соответственно.
Результаты количественной оценки маркеров дифференцировки в остеобласты в культурах hMSC, стимулированных в отношении дифференцировки в остеобласты, проведенной как путем определения активности щелочной фосфатазы, так и содержания кальция в культуре, продемонстрировали, что специфические ингибиторы 15-липоксигеназы стимулируют дифференцировку человеческих костеобразующих клеток in vitro.
Кроме того, проводили оценку способности ингибиторов 15-липоксигеназы стимулировать образование костной ткани и отложение костной ткани с помощью клоногенных анализов, в которых определяли клоногенный потенциал клеток-предшественников клеток костного мозга. Клетки остеобластов и остеокластов обрабатывали ингибиторами 15-липоксигеназы. Согласно одному из методов клетки и ингибиторы инкубировали in vitro. В другом методе млекопитающему вводили ингибитор, выделяли клетки-предшественники клеток костного мозга и высевали. В обоих методах измеряли колониеобразующие единицы, образовавшиеся из этих клеток костного мозга. Можно осуществлять скрининг соединений в отношении их способности увеличивать минеральную плотность костной ткани, если установлено, что они увеличивают клоногенный потенциал костного мозга в отношении остеобластов или снижают клоногенный потенциал костного мозга в отношении остеокластов.
Пример 4
Нарушение гена 15-липоксигеназы приводит к увеличению минеральной плотности костной ткани бедренной кости
Первоначально было выявлено, что у мышей с дефицитом 15-ЛО имеются небольшие фенотипические изменения, но затем на модели с использованием таких же мышей было установлено, что они частично защищены от к атеросклеротических повреждений (Sun и Funk, J. Biol. Chem., 271, cc.24055-24062, 1996; Cyrus и др., J. Clin. Invest, 103, cc.1597-1604, 1999). При этом у мышей с дефицитом 15-ЛО не измеряли МПК. Для исследования влияния генетического нарушения 15-ЛО на минеральную плотность костной ткани, мышей с дефицитом ("knock-out") 15-ЛО (15-ЛО-КО) сравнивали с исходной линией мышей с точки зрения минеральной плотности костной ткани. Измерения минеральной плотности костной ткани проводили методом двойной абсорбциометрии энергии рентгеновских лучей (DEXA). Все исследования проводили с использованием денситометра типа Lunar PIXImus (фирма Lunar Corp., Мэдисон, шт.Висконсин). Денситометрические анализы всего тела проводили на анестезированных мышах возрастом 4 месяца, когда заканчивалось накопление массы зрелой кости. Глобальное окно представляло собой изображение всего тела за исключением свода черепа, нижней челюсти и зубов. После умерщвления правую бедренную кость тщательно выделяли и перед осуществлением DEXA-сканирования очищали от присоединенных к ней тканей. Не было обнаружено существенных различий минеральной плотности костной ткани всего тела у мышей линии 15-ЛО-KO и исходной линии мышей C57BL/6 (49,8+/-0,6 мг/см2 по сравнению с 49,5+/-0,4 мг/см2). Однако важно, что МПК бедренной кости оказалась существенно большей у мышей с дефицитом 15-ЛО по сравнению с исходной линией C57BL/6 (54,0+/-1,2 мг/см2 по сравнению с 49,7+/-0,7 мг/см2). Эти результаты демонстрируют, что нарушение 15-ЛО приводит к увеличению минеральной плотности костной ткани бедренной кости.
Пример 5
Ингибиторы 15-липоксигеназы стимулируют образование костной ткани in vivo
Способность ингибиторов 15-липоксигеназы стимулировать образование костной ткани in vivo оценивали путем измерения способности ингибиторов улучшать параметры костной ткани при моделировании остеопороза на мышах. Конститутивная экспрессия трансгена интерлейкина-4 под контролем промотора гена Lck (Lck-IL4) в мышах линии C57BL/6 приводила к фенотипу костной ткани, имитирующему серьезный остеопороз (Lewis и др., Proc. Natl. Acad. Sci., 90, cc.11618-11622, 1993), и таких мышей использовали для демонстрации влияния обработки ингибиторами 15-ЛО на массу костной ткани.
Четыре группы, на которых проводили эксперимент, представлены в таблице 2. В период отъема от грудного молока мышам линии дикого типа C57BL/6 или трансгенной линии Lck-IL4 вводили ежедневно дважды в день вместе с кормом в течение 84 дней по 150 мг/кг соединения 2 PD 146176 (корм 5001: 23% протеина, 10% жира, 0,95% кальция и 0,67% фосфора; фирма PMI Feeds, Inc., Сент-Луис, шт.Миссури). Мышам дважды в день приблизительно с 12-часовыми интервалами давали доступ к половине суточного рациона и ежедневно наблюдали за приемом корма. Они имели доступ к воде без ограничения. Контрольным группам давали такой же корм, не содержащий соединение 2. Животные во всех группах в процессе эксперимента поглощали корм одинаковым образом.
| Таблица 2 |
| C57BL/6 |
Трансгенная линия Lck-IL4 |
| контроль |
Соединение 2 |
контроль |
соединение 2 |
| n=17 (8F/9M) |
n=18 (9F/9M) |
n=20 (11F/9M) |
n=22 (11F/11M) |
Таблица 2. Экспериментальные группы, на которых проводили исследование ингибитора in vivo. После отъема (приблизительно в возрасте 28 дней), мышам в течение 84 дней давали корм, содержащий ингибитор 15-ЛО (соединение 2), или без него. Количество самок (F) и самцов (М) в группах было примерно одинаковым.
Влияния сверхэкспрессии IL4 ингибирования 15-ЛО на общие параметры тела, МПК бедренной кости и ее геометрию и биомеханические характеристики бедренной кости представлены в таблице 3. Сверхэкспрессия IL4 приводила к существенному уменьшению МПК всего тела, массы тела и гематокрита и увеличению процентного содержания жира в организме. Сверхэкспрессия IL4 приводила также к уменьшению МПК бедренной кости, кортикальной площади, момента инерции и кортикальной толщины по сравнению с мышами линии C57BL/6 дикого типа. Установлено, что увеличение площади костного мозга у мышей линии Lck-IL4 коррелировала с уменьшенным гематокритом и связанной с этим анемией. Кроме того, сверхэкспрессия IL4 оказывала существенное влияние на биомеханические характеристики бедренной кости, включая уменьшение нагрузки, приводящей к перелому, жесткости кости и прочности кости (таблица 3). У мышей, которым вводили ингибитор 15-ЛО (соединение 2), выявлена частичная реверсия разрушительных воздействий на костную ткань всего тела и бедренную кость (таблица 3). У обработанных лекарственным средством мышей было выявлено существенное увеличение МПК всего тела, гематокрита, МПК бедренной кости и кортикальной толщины по сравнению с контрольными мышами, несущими трансген Lck-IL4. Важно, что у обработанных ингибитором 15-ЛО мышей было выявлено существенное увеличение биомеханических характеристик бедренной кости, включая нагрузку, приводящую к перелому, жесткость и прочность. Это имеет особенное значение для остеопороза, поскольку уровень прочности кости и нагрузки, приводящей к перелому, являются важными детерминантами для пациентов, для которых возрастает вероятность возникновения переломов. В целом результаты, полученные на модели остеопороза с использованием животных, свидетельствуют о том, что ингибирование 15-ЛО in vivo приводит к более высоким уровням МПК и более высокой прочности костной ткани.
| Таблица 3 |
| Все тело |
 |
 |
 |
 |
| фенотип |
Влияние сверхэкспрессии IL-4 |
Значение р |
Влияние сверхэкспрессии IL-4 + соединения 2 |
Значение p |
| Вес тела |
-7% |
0,042 |
н.о. |
ns |
| Содержание жира в организме, % |
+19% |
0,007 |
н.о. |
ns |
| гематокрит |
-25% |
2×10-9 |
+20% |
2×10-5 |
| BMD всего тела |
-11% |
2×10-9 |
+5% |
7×10-5 |
 |
 |
 |
 |
 |
| BMD и геометрия бедренной кости |
 |
 |
 |
| Фенотип |
Влияние сверхэкспрессии IL-4 |
Значение р |
Влияние сверхэкспрессии IL-4 + соединения 2 |
Значение p |
| BMD |
-17% |
4×10-12 |
+9% |
3×10-6 |
| Длина |
н.о. |
н.д. |
н.о. |
н.д. |
| Общая площадь |
н.о. |
н.д. |
-4% |
0.035 |
| Кортикальная площадь |
-25% |
6×10-12 |
н.о. |
Ns |
| Площадь костного мозга |
+16% |
4×10-7 |
-7% |
7×10-5 |
| Момент инерции |
-17% |
7×10-5 |
н.о. |
н.д. |
| Кортикальная толщина |
-27% |
9×10-10 |
+6% |
0,037 |
 |
 |
 |
 |
 |
| Биомеханические характеристики бедренной кости |
 |
 |
 |
 |
| Фенотип |
Влияние сверхэкспрессии IL-4 |
Значение р |
Влияние сверхэкспрессии IL-4 + соединения 2 |
Значение p |
| Нагрузка, приводящая к перелому |
-45% |
6×10-13 |
+18% |
0,003 |
| Жесткость |
-48% |
3×10-11 |
+11% |
0,09 |
| Прочность |
-34% |
2×10-12 |
+22% |
2×10-4 |
Таблица 3. Влияния сверхэкспрессии IL4 и ингибитора 15-ЛО на параметры всего тела и бедренной кости. Параметры всего тела и бедренной кости измеряли у мышей, несущих трансген Lck-IL4, который вызывает сверхэкспрессию IL4, и сравнивали с мышами линии C57BL/6, используемыми в качестве контролей. Указанные параметры измеряли также у мышей линии Lck-IL4, которым вводили ингибитор 15-ЛО, представляющий собой соединение 2, и сравнивали с параметрами необработанных мышей линии Lck-IL4, используемых в качестве контролей, н.о. обозначает, что не обнаружено различий между группами, н.д. обозначает, что значение p не является достоверным.
Животные
Всех мышей, которых использовали в экспериментах in vivo, выращивали в идентичных условиях в ветеринарном институте Портланда, шт.Вирджиния, из линии, первоначально полученной от Джексоновской лаборатории (Jackson Laboratory) (Бар Харбор, штат Мэн). Из исходной линии, полученной из Джексоновской лаборатории, поддерживали не более трех поколений мышей. После отъема мышей содержали группами (по 9-10 животных на клетку) при световом цикле 12 ч света/темноты (с 6:00 до 18:00 ч) при 21±2°С. Все процедуры были утверждены государственным комитетом по содержанию и использованию животных шт.Вирджиния (VA Institutional Animal Care and Use Committee) и их осуществляли согласно руководствам по содержанию и использованию животных при проведении исследований, утвержденных Национальным институтом здравоохранения.
Денситометрия костной ткани
Измерения минерального содержания костной ткани осуществляли с помощью двойной абсорбциометрии энергии рентгеновских лучей (DEXA). Все исследования проводили с использованием денситометра типа Lunar PIXImus (фирма Lunar Corp., Мэдисон, штат Висконсин). Денситометрические анализы всего тела проводили на анестезированных мышах возрастом 4 месяца, когда заканчивалось накопление массы зрелой кости. Глобальное окно представляло собой изображение всего тела за исключением свода черепа, нижней челюсти и зубов. После умерщвления правую бедренную кость тщательно выделяли и перед осуществлением DEXA-сканирования очищали от присоединенных к ней тканей.
Обработка образцов
Взрослых мышей (возрастом 16 недель) подвергали эвтаназии путем ингаляции СО2 и взвешивали с точностью до 0,1 г. Сразу после умерщвления спускали кровь из сердца и небольшие аликвоты цельной крови сохраняли для определения гематокрита. Сразу выделяли поясничные позвонки и обе бедренные кости, завертывали в стерильную марлю, пропитанную забуференным фосфатом физиологическим раствором, и хранили в замороженном состоянии при температуре не менее примерно -20°С для дальнейших анализов.
Геометрия стержня бедренной кости
Геометрические параметры поперечного сечения средней части диафиза бедренной кости определяли с помощью переносного рентгеновского микротомографа (модель 1074, фирма Skyscan, Антверпен, Бельгия). Сканирование осуществляли с интервалами по 40 мм и на срезах, находящихся в средней части бедренной кости, анализировали общую площадь (FCSA), кортикальную площадь (Ct Ar) и площадь модулярного канала (Ма Ar). Кроме того, на основе количества пикселов, находящихся в кортикальной области цифрового изображения, вычисляли радиус от центроида поперечного сечения до наружного волокнистого слоя в переднезадней плоскости, статический момент инерции площади сечения (Ixx) в плоскости изгиба и среднюю кортикальную толщину (Ct Th).
Исследование биомеханических характеристик
Бедренную кость исследовали в отношении перелома путем изгиба при приложении усилия в трех точках с использованием высокоточного устройства для исследования характеристик материалов (модель Instron 4442, Кантон, шт.Миннесота). Нагрузку, приводящую к перелому, и жесткость определяли с помощью системного программного обеспечения. Затем с использованием данных проведенных ранее измерений площади поперечного сечения рассчитывали прочность на изгиб.
Анализ данных
Все данные анализировали с помощью двунаправленного дисперсионного анализа (ANOVA) с использованием пакета программ JMP (институт SAS).
Пример 6
Способность ингибитора 15-липоксигеназы увеличивать образование костной ткани in vivo
Для определения способности ингибиторов 15-липоксигеназы стимулировать образование костной ткани и накопление костной ткани получали согласно методу, описанному в WO 0196298, изобутиловый эфир [[[5-(5,б-дифтор-1Н-индол-2-ил)-2-метоксифенил]амино]сульфонил]карбаминовой кислоты, т.е. соединение 6, и тестировали согласно стандартному методу анализа остеопении на подвергнутых овариэктомии (Ovx) крысах с дефицитом эстрогена.
Крыс возрастом 3 месяца подвергали овариэктомии (Ovx) и вводили орально с помощью желудочного зонда 1 мг/кг/день соединение 6 или 0,1 мкг/кг/день 1,25-дигидроксивитамин D3 (положительный контроль, сокращенное обозначение в таблице вит.D) один раз в день, начиная со второй недели после овариэктомии, и продолжали в течение 7 недель. Дозу увеличивали до 2 мг/кг/день и продолжали до окончания 11-недельного периода. Крысам в контрольных группах, как в группах животных-имитаторов (крыс, которых не подвергали овариэктомии), так и в Ovx-группе, вводили только носитель. Минеральную плотность костной ткани позвоночника и правого бедра оценивали с использованием пакета программ High Resolution с помощью денситометра костной ткани типа QDR-4500 (фирма Hologic, Валтан, шт.Миннесота). Животных подвергали сканированию, помещая их в положение лежа на спине, таким образом, чтобы правое бедро было перпендикулярно корпусу тела и большеберцовая кость была перпендикулярна бедру. Минеральная плотность костной ткани (г минералов/см2) в большеберцовой кости и позвоночнике при использовании соединений представлена в таблице 4. У животных, обработанных ингибитором 15-ЛО, выявлено увеличение МПК в позвоночнике в период времени >3 недель и в проксимальной части бедренной кости в период времени >7 недель. Результаты приведены в таблице 4.
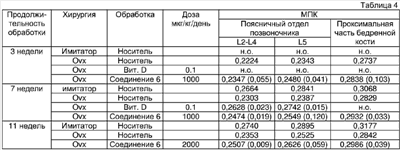
Величины в скобках представляют собой значения p по отношению к OVX-контролю в тот же момент времени, н.о.=данные отсутствуют.
Пример 7
Генная манипуляция с целью уменьшения экспрессии гена 15-липоксигеназы у лабораторных мышей приводит к увеличению массы и прочности костной ткани.
Для изучения связи между экспрессией 15-липоксигеназы и образованием костной ткани создавали генетически гетерогенную популяцию F2 из двух штаммов-предшественников (линий), B6.129S2-Alox15tm1Fun (с дефицитом Alox15 или 15LOKO) и DBA/2 (D2), которые получали от Джексоновской лаборатории (Бар Харбор, шт.Мэн). Мыши линии B6.129S2-Alox15tm1Fun (15LOKO) были гомозиготными по целевой мутации в гена Alox15 и поэтому у них не могла происходить экспрессия арахидоната под воздействием 15-липоксигеназы. В отличие от этого у мышей линии D2 обнаружены высокие уровни Alox15. Мышей поколения F1 линии 15LOKO-D2 разводили в лаборатории, где проводили опыты, из родительских линий, полученных от Джексоновской лаборатории, и подвергали интеркроссу, получая в общей сложности 292 особи поколения F2 мышей линии 15LOKO-D2. После отъема мышей содержали группами (по 2-5 животных на клетку) при световом цикле 12 ч света/темноты (с 6:00 до 18:00 ч) при 21±2°С, при этом животные имели свободный доступ к воде и корму для лабораторных грызунов (диета 5001: 23% протеина, 10% жира, 0,95% кальция и 0,67% фосфора; фирма PMI Feeds, Inc., Сент-Луис, шт.Миссури).
Все мыши, на которых проводили опыты, имели возраст 4 месяца, когда заканчивается накопление массы костной ткани (28). Измерения минеральной плотности костной ткани производили с использованием денситометра с узким лучом типа Hologic QDR 1500 (фирма Hologic, Валтам, шт.Миннесота), который ежедневно калибровали с использованием гидроксиапатитного фантома поясничного отдела позвоночника человека. Анализ осуществляли с использованием программного обеспечения для анализа всего тела мыши (версия 3.2), любезно предоставленного производителем (фирма Hologic, Валтам, шт.Миннесота). Денситометрический анализ осуществляли на анестезированных мышах. Кормление прекращали в ночь перед проведением исследования (для того, чтобы исключить влияние непереваренного корма для грызунов на оценку минеральной плотности костной ткани, которое может исказить результаты), при этом мышей анестезировали путем ингаляции изофураном. Животных взвешивали с точностью до 0,1 г и затем подвергали сканированию для определения плотности костной ткани. Мышей подвергали эвтаназии путем ингаляции СО2 и в асептических условиях выделяли селезенки и бедренные кости и затем сразу замораживали для дальнейшего анализа. Все процедуры были утверждены государственным комитетом по содержанию и использованию животных шт.Вирджиния (VA Institutional Animal Care and Use Committee) и их осуществляли согласно руководствам по содержанию и использованию животных при проведении исследований, утвержденных Национальным институтом здравоохранения.
Структуру бедренной кости (площадь средней части кортикальной области кости и кортикальную толщину) измеряли с помощью настольного микротомографического рентгеновского сканера (модель Sky Scan 1074, Аартзелаар, Бельгия). Левую бедренную кость исследовали в отношении перелома путем изгиба при приложении усилия в трех точках с использованием высокоточного устройства для исследования характеристик материалов (модель Instron 4442, Кантон, шт.Миннесота). Присоединяли экстензометр (модель 2630-113, фирма Instron Corp.) и использовали системное программное обеспечение (серии IX для Windows 95, фирма Instron Corp.) для перемещения силового привода со скоростью деформации 0,5%/с до тех пор, пока не происходил перелом. Регистрировали данные о нагрузке и перемещении (измеряемые с помощью экстензометра) и с помощью системного программного обеспечения рассчитывали нагрузку, приводящую к перелому (F), и прочность (k, определяемую на основе зависимости линейной составляющей нагрузки от перемещения).
Геномную ДНК выделяли из селезенок индивидуальных мышей согласно методу высаливания. Мышей генотипировали согласно протоколу полимеразной цепной реакции (ПЦР), разработанному Джексоновской лабораторией (http://aretha.jax.org/pub-cgi/protocols/protocols.sh?objtype=protocol&protocol_id=304), разработанному для создания имеющих различные размеры продуктов гена ALox15 дикого типа (266 пар оснований) и мутантного гена (172 пары оснований). Амплификацию проводили в термоячейке типа Perkin-Elmer 9700 (Бранчбург, шт.Нью-Джерси). ПЦР-продукты разделяли на 4%-ных агарозных гелях и осуществляли визуализацию путем окрашивания бромидом этидия.
Популяция поколения F2 15LOKO-D2 состояла из примерно равного количества самцов (n=141) и самок (n=151) и, как проиллюстрировано в таблице 5, частота встречаемости генотипа ALox15 согласуется с критерием ожидания Харди-Вайнберга у 70 (24%) гомозиготных мышей «с дефицитом» (отсутствием аллеля 15-ЛО), у 153 (52%) гетерозиготных мышей (один аллель 1 5-ЛО из линии D2) и у 69 (24%) гомозиготных мышей линии D2 мышей (оба аллеля 15-ЛО из линии D2). Хотя не было обнаружено разницы в весе тела, у мышей поколения F2, гомозиготных по дефициту ALox15, была выявлена большая величина МПК всего тела по сравнению с гомозиготными мышами линии D2 или гетерозиготными мышами (р=0,006 по результатам дисперсионного анализа (ANOVA)). Кроме того, у мышей линии F2, гомозиготных по дефициту ALox15, выявлены повышенные количества кортикальной костной ткани стержня бедра (кортикальной площади и кортикальной толщины) и существенно более высокие структурные характеристики, о чем свидетельствуют полученные путем измерений более высокая величина нагрузки, приводящей к перелому, и прочность (таблица 6).
| Таблица 5 |
| Корреляция 15LO-генотипа с МПК в популяции мышей поколения F2 линии 15LOKO-D2 |
 |
Количество аллелей 15LO D2 |
ANOVA значение p |
 |
0 |
1 |
2 |
| Количество мышей |
69 |
127 |
70 |
 |
| Вес тела, г |
28,2±0,61 |
27,5±0,43 |
29,2±0,64 |
н.д. |
| МПК, г/см2 |
66,1±0,33 |
64,9±0,25 |
65,0±0,31 |
р=0,006 |
| Таблица 6 |
| Корреляция 5LO-генотипа с массой и прочностью бедренной кости в популяции мышей поколения F2 линии 15LOKO-D2 |
| Количество аллелей 15LO D2 |
 |
0 |
1 |
2 |
значение p |
| Количество мышей |
15 |
15 |
15 |
 |
| Вес тела, г |
23,3±0,54 |
23,9±0,45 |
23,7±0,40 |
Alox15 |
| МПК, г/см2 |
65,6±0,46 |
64,8±0,95 |
63,4±0,65 |
р=0,005 |
| Площадь Ct, мм |
0,76±0,03 |
0,78±0,03 |
0,70±0,02 |
р=0,046 |
| Толщина Ct, мм |
0,193±0,005 |
0,200±0,006 |
0,176±0,004 |
р=0,006 |
| Нагрузка, |
20,5±0,8 |
20,3±0,8 |
18,0±0,6 |
р=0,013 |
| приводящая к перелому, Н |
 |
 |
 |
 |
| жесткость, Н/мм |
126,5±4,6 |
108,7±5,1 |
110,3±3,3 |
р=0,004 |
(МПК=МПК всего тела; площадь Ct=кортикальная площадь стержня бедренной кости; толщина Ct=кортикальная толщина стержня бедренной кости).
Таким образом, в описании представлены новые способы лечения или предупреждения потери костной ткани, увеличения минеральной плотности костной ткани и увеличения образования и отложения костной ткани. Хотя в заявке подробно описаны предпочтительные варианты осуществления изобретения, следует понимать, что могут быть сделаны очевидные вариации без отклонения от сущности и объема изобретения, которые определяются прилагаемой формулой изобретения.
Формула изобретения
1. Способ идентификации соединений, которые обладают способностью увеличивать минеральную плотность костной ткани, заключающийся в том, что соединение приводят в контакт с 15-липоксигеназой и определяют, обладает ли соединение активностью в отношении ингибирования 15-липоксигеназы.
2. Способ по п.1, отличающийся тем, что соединение тестируют с помощью функционального анализа, который позволяет определять эффективность соединения в отношении формирования костной ткани.
3. Способ по п.2, в котором функциональный анализ заключается в том, что соединение приводят в контакт с человеческими мезенхимальными стволовыми клетками и определяют дифференцировку клеток в костеобразующие клетки.
4. Способ по п.2, в котором функциональный анализ заключается в том, что соединение вводят животному, кроме человека, и измеряют индекс костеобразования.
5. Способ по п.4, в котором измеряемый индекс представляет собой минеральную плотность костной ткани.
6. Способ по п.4, в котором индекс представляет собой биомеханический параметр кости.
7. Способ по п.3, в котором для определения дифференцировки клеток проводят анализ щелочной фосфатазы, анализ содержания кальция, анализ общей ДНК препарата или их комбинацию.
|