
СПИСОК ПАТЕНТОВ С УПОМИНАНИЕМ ГИАЛУРОНОВОЙ КИСЛОТЫ
-
- 2017751 Способ получения гиалурона
- 2192150 БАД для профилактики йодной недостаточности
- 2112542 Препарат для лечения патологий соединительных тканей
- 2225206 Препарат для лечения рака молочной железы
- 2299733 Лечение опорно-двигательного аппарата
- 2299732 Способ лечения глаукомы
- 2299726 Противоинфекционная губная помада
- 2299725 Косметическое средство для ухода за кожей
- 2198878 Ароматическое соединение
- 2198702 Способ подготовки трофических язв к аутодермапластике
- 2198653 Вагинальные суппозитории
- 2197946 Композиция для ухода за волосами
- 2197923 Фармацевтическая композиция для лечения отеков роговицы
- 2298410 Биотрансплантант и способ лечения ревматических и аутоиммунных заболеваний
- 2197501 Фотоотверженный гель на основе сшитой гиалуроновой кислоты
- 2197228 Твердые лекарственные формы
- 2197222 Водная компазиция для ухода за волосами, лица и тела
- 2297425 Полипептиды
- 2297240 Композиция с гиалуроновой кислотой
- 2297230 Фармацевтическая компазиция с ксантоновой смолой
- 2196588 Глазные капли
- 2195955 Применение биологически активных веществ
- 2195926 Дерматологические композиции
- 2295954 Микрочастицы для доставки нуклеиновых кислот
- 2295951 Косметика для ухода за кожей лица и век
- 2195262 Фармакологическое средство на основе гиалуроновой кислоты
- 2194512 Способ профилактики и коррекции процесса старения кожи
- 2194478 Лечение экземы
- 2294716 Расширяемый стент
- 2194055 Сшитые сополимеры
- 2099350 Ассоциаты депротонированной гиалуроновой кислоты
- 2293557 Средство для лечения кожи и слизистых
- 2292878 Приготовление микроцастиц, содержащих метопропол
- 2292746 БАД
- 2192256 Защита кишечника
- 2191782 Получение модифицированной гиалуроновой кислоты
- 2292219 Паратиреоидный гормон человека
- 2291686 Микроцастицы
- 2191000 Косметическая маска
- 2290921 Фармацевтические и косметические средства против старения кожи
- 2290900 Модифицированный биоматериал для использования в офтальмологии
- 2290899 Получение биоматерьяла
- 2290397 Новые инданилиденовые соединения
- 2290186 Лечение сирингомиелии
- 2288702 Иррингационный раствор для офтальмологии
- 2288699 Гель для лечения стоматологических заболеваний
- 2188011 Активирующая остеогенез фармацевтическая композиция
- 2187327 Средство с антисептиком
- 2187325 Средство с радиопротекторным действием
- 2287330 Композиции миноксидила
- 2186786 Способ получения гиалуроновой кислоты
- 2186593 Лечение раненого процесса кожи
- 2286801 Очищение воды
- 2286781 Лечение ожогов пищевода у детей
- 2286764 Средство лечения воспалений полости рта
- 2185840 Лечение инфекционных заболеваний
- 2286151 Альфа-2-Дельта-Лиганда
- 2185149 Ранозаживляющий гель
- 2285527 Лечение ИЛ-6 заболеваний
- 2184448 Раствор хранения роговицы, включающий гиалуроновую кислоту
- 2090179 Крем для кожи
- 2183961 Способ лечения кожи
- 2284331 Соли алифотических аминов
- 2284187 Производные амида
- 2089191 Снизить внутрение давление
- 2283320 Получение гликозаминогликанов
- 2283129 Лечение опухолей
- 2283098 Косметические средства с Q
- 2182574 Ароматические соединения
- 2088257 Средство с гипохолестеролемическим действием
- 2088218 Состав для гигиенических салфеток
- 2088206 Способ получения препарата, создающего исскуственный загар
- 2282462 Противомикробные средства
- 2182008 Интровагинальная компазиция
- 2181999 Препарат с отсроченным высвобождением
- 2181998 Новые композиции липидов
- 2181995 Лечение болевого синдрома
- 2181295 Вирионная вакцина
- 2087144 Витамин Е
- 2379336 Способ стирки
- 2379052 Вакцинация
- 2180855Композиция в виде ионного комплекса
- 2379025 Противоинфекционный гель
- 2180825 Лечение травм роговицы
- 2281082 Способ коррекции эстетических и возрастных проблем кожи
- 2180576 Биоактивная добавка для косметических средств
- 2280459 Средство для изменения скорости роста или репродукции клеток
- 2179981 Соли переходного металла
- 2378010 Жидкие вакцины
- 2378008 Комбинированные вакцины
- 2378007 Анаболическое средство
- 2377973 Растительные экстракты
- 2280041 Способ получения водорастворимых комплексов гиалурил
- 2280038 Биополимеры
- 2323733 Йодный обмен
- 2377260 Гель
- 2178693 Противовирусное средство на основе гиалуроновой кислоты
- 2178692 Облегчающие зуд косметическое средство
- 2377022 Гемостатические спреи
- 2376982 Увлажняющая сыворотка для лица
- 2376974 Трансдермальный гель для лица
- 2362784 Гипо-и гиперацетилированные менингокковые капсульные сахариды
- 2177789 Устройство для доставки лекарства к шейке матки
- 2277954 Крем для лица омолаживающий
- 2376378 Способ получения метионина
- 2177332 Биоматериал для предотвращения послеоперационных спаек, с производной гиалуроновой кислотой
- 2177310 Способ получения таблеток
- 2376011 Средство для позвоночника
- 2277410 Косметическое средство
- 2323748 Медицинская повязка
- 2276998 Гидрогелевые композиции
- 2082416 Способ получения препарата с коллагенном из животного сырья
- 2375081 Адсорбирующее изделие
- 2375049 Охлаждающий пластырь
- 2346049 Способ получения гиалурона
- 2275913 Фармацевтические средства
- 2174985 Полисахарид с антиоксидантом
- 2373957 Носитель для лекарственных средств и биологически активных веществ
- 2373941 Способ коррекции возрастных и патологических изменений кожных покров
- 2174845 Композиции и способы доставки генетического материала
- 2174830 Средство для укрепления волос
- 2373769 Синбиотическая композиция
- 2274472 Лечение апорно-двигательного аппарата и болевых синдромов
- 2372929 Профилактическая композиция на основе веществ фенольной природы в липосомной форме
- 2173563 Способ нанесения на поверхность предметов покрытия на основе гиалуроновой кислоты, её производных и полусинтетических полимеров
- 2079304 фармацевтическая композиция, обладающая иммуносупрессорной и антимикробной активностью
- 2273645 Полипептид ожирения
- 2173154 Фракция кератансульфатолигосахаридов и содержащий ее фармацевтический препарат
- 2173136 Грязная мазь
- 2173128 Способ хирургического лечения центральных разрывов сечатки
- 2078561 Косметическое средство предотвращающее старение кожи
- 2172490 Способ прогнозирования воспалительных заболеваний молочной железы при эндопластике
- 2272645 Способ лечения ЦМВ-Инфекции у детей раннего возроста
- 2272636 Фармацевтическая композиция для местного лечения воспаления
- 2272635 Фармацевтически активная субстанция для офтальмологии
- 2272599 Биоматерьял для стабилизации прогрессирующей миопии "Коллаплант"
- 2172168 Средство для заживления ран на основе гиалуроновой кислоты
- 2371172 Фармацевтическая композиция для лечения нервной системы на основе стефаглабрина
- 2171470 Способ прогнозирования послеоперационной трансформации доброкачественных опухолей нервной системы
- 2077317 Состав для ванн
- 2271213 Комбинированные композиции, содержащие экстракты из растений и морских животных
- 2076872 Способ получения окрашенной гиалуроновой кислоты
- 2076671 Раствор для защиты роговицы
- 2370281 Конъюгаты гидроксиалкилкрахмал
- 2370275 Способ лечения (коррекции) косметических и возрастных дефектов кожи
- 2370258 Фармацевтическая композиция для парентальной доставки в форме лиофилизата
- 2270023 Способ экстракции и очистки протеогликана хрящего типа (варианты)
- 2369408 Гемостатическая композиция, включающая гиалуроновую кислоту
- 2369387 Фармацевтическая композиция для лечения нервной системы
- 2369379 Нетаблитированные жевательные формы для индивидуального введения
- 2169136 Производное коричной кислоты
- 70792 Медицинский аппликатор
- 20741717 Способ стабилизации аскорбиновой кислоты
- 2074712 Способ получения препарата, препятствующего преждевременной эякуляции
- 2367954 Способ прогнозирования развития кожной патологии у женщин с синдромом склерополикистозных яичников (СПКЯ)
- 2268075 Устройство для электрокинетической доставки
- 2268052 Средство для лечения воспалительных и дегенеративных заболеваний суставов
- 2167649 Способ получения твердой дисперсии умеренного водорастворимого лекарственного вещества
- 2167647 Гель для бритья
- 2073520 Лечение урологических инфекций
- 2367476 Биопластический материал
- 2367475 Мембрана для использования при направленной регенерации тканей
- 2367469 Фармацевтическая композиция на основе лизоамидазы
- 2367456 Фармацевтическая композиция обладающая антибактериальным и некролитическим действием
- 2367455 Фармацевтическая композиция обладающая некролитическим и антибактериальным действием
- 2267324 Применение антиадгезивных углеводов, препарат для уменьшения и /или блокирования адгезии патогенных веществ
- 2166934 Композиции включающие биологический агент
- 2166510 Псевдодипептиды
- 2366460 Композиции, имеющие высокую противовирусную и антибактериальную активность
- 2360901 Производные феноксиуксусной кислоты
- 2165749 Способ восстановления эндотелия роговицы
- 2265441 Способ укрепления склеры
- 2365382 Композиции и способы для регуляции развития сосудов
- 2070879 Соли гликозаминогликанов
- 2164914 Циклические и гетероциклические N - замещенные - иминогидроксамовые карбоновые кислоты
- 2264627 Хламидийный конъюктивит
- 2364399 Фармацевтический препарат на основе стефаглабрина
- 2264230 Препарат с замедленным высвобождением активного вещества
- 2363497 Фармацевтические композиции
- 2363496 Способ увеличения объема мягких тканей
- 2363473 Способ антифлогистической активации в эксперементе
- 2363461 Фармацевтический препарат на основе сигетина
- 2363459 Средства для введения в роговицу глаз для предотвращения офтальмологических нарушений
- 2363448 Фармацевтические композиции
- 2163123 Глазные капли
- 2162687 Усовершенствованнная лекарственная форма индуктора интерферана
- 2162343 Биосовместимый полимерный материал и способ его получения
- 2162327 Лечение рака
- 2067841 Способ получения ароматизатора
- 2161478 Способ консервированого лечения гонартроза
- 2361617 Вольфрамовые частицы в качестве рентгеноконтрастных веществ
- 2361552 Способы и устройства для дренирования жидкостей и понижения внутриглазного давления
- 2066996 Способ изготовления пленочного материала для офтальмохирургии
- 2361417 Корм с глюкозамином и экстрактом ивы для профилактики артроза у животных
- 2161002 Пищевой общеукрепляющий лечебно-профилактический продукт из хрящевой ткани акул
- 2360928 Комплексная матрица для медико-биологического применения
- 2160574 Способ лечения глаукомы
- 2360688 Способ лечения повреждений переферических нервов
- 2360670 Фармацевтическая композиция при климактерических расстройствах
- 2360646 Эндолюминальный протез
- 2260445 Способ усовершенствования транспортировки через легко прспосабливаемый полупроницаемый барьер
- 2260007 Производные амида
- 2359975 Способ получения модифицированных арабиногалактанов
- 2359974 Антигенные Пептиды
- 2159775 Псевдопептидный продукт
- 2259833 Фармацевтическая композиция для лечения роговицы глаза
- 2259816 Ранозаживляющее средство
- 2259815 Способ коррекции возрастных изменений, связанных с процессами старения кожи
- 2359706 Способ сохранения офтальмологических растворов
- 2359704 Антисептическое средство
- 2359662 Микрокапсулы
- 2159253 Катионные полимеры
- 2159111 Средство для ухода за кожей лица
- 2159105 Композиция для защиты кожи от опасных химических веществ Получение
- 2158593 Биосовместимый водный раствор
- 2358728 Способ лечения и предупреждения потери костной ткани
- 2258517 Способ хирургического лечения травмотических повреждений селезенки пленкой на основе гиалуроновой кислоты
- 2357968 Кристалические формы производной имидазола
- 2357957 Ингибиторы P38 и их применение
- 2157647 Пищевая добавка и ее получение
- 2357758 Препараты для чрескожной и чересслизистой добавки
- 2063244 Способ стабилизации растворов
- 2063140 Способ получения препарата для консервирования мяса
- 2157381 Способ получения гиалуроновой кислоты
- 2257198 Композиции микроцастиц
- 2356909 Белковый комплекс
- 2356570 Косметическая композиция
- 2256434 Способ закрытия перфорации барабанной перепонки
- 2356520 Способ лечения постконтузионного повреждения сечатки глаза
- 2156133 Гель
- 2255945 Полимерная композиция
- 2355761 Средства повторной дифференцировки
- 2061043 Способ повышения устойчивости урокиназы к нагреванию
- 2061005 Способ получения красителей для гистологических исследований
- 2355420 Зубная паста
- 2355385 Композиции пролонгированного действия с контролируемым высвобождением
- 2355240 Способ получения пищевого препарата хондропротекторного действия
- 2155057 Пихтово репейный бальзам
- 2354409 Способ производства высвобождающих лекарственные средчтва медицинских устройств
- 2254145 Раневое покрытие на основе коллаген-хитозанового комплекса
- 2254133 Лечение и профилактика ВИЧ-инфекции у человека
- 2253439 Фармацевтическая композиция для защиты и улучшения оптических свойств роговици при проведении эндовитреальных вмешательств
- 2253437 Способ омоложения кожи
- 2153352 Фармацевтическая композиция обладающая ранозаживляющим и противовоспалительным действием
- 2353354 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2252787 Способ получения искусственной матрицы кожи
- 2252767 Способ нормализации иммунобиохимического гомеостаза коров в предродовом и послеродовом периодах
- 2352583 Фармацевтическая композиция содержащая Fc-область иммуноглобулина в качестве носителя
- 2152403 Модифицированные полисахариды
- 2352356 Иммуногенная композиция
- 2352342 Исскусственный физиологический солевый раствор Способ его получения
- 2352330 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2352323 Фармацевтический препарат с модифицированным высвобождением
- 2152027 Способ подготовки ткани мозга для определения гликозаминогликанов
- 2251842 Интектицидный состав для борьбы с личинками оводов
- 2151580 Способ активации пролиферации эндотелия роговицы
- 2351648 Дифференцировка стромальных клеток, полученных из жировой ткани, в эндокринные клетки поджелудочной железы и их использование
- 2351595 N - гидроксиформамидные соединения в качестве ингибиторов металлопротеина
- 2251411 Косметическое средство в лиофилизированной фармацевтической форме
- 2251405 Косметика...ее композиции для косметических препаратов
- 2251367 Средство со сшитой гиалуроновой кислотой для наращивания тканей
- 2351359 Косметика для профилактики и лечения избыточной массы тела
- 2351322 Препарат на основе низкомолекулярного индуктора интерферона
- 2351153 Диета при остеортрите собак
- 2350958 Способ определения групповой принадлежности синовальной жидкости
- 2350625 Производные гиалуроновой кислоты с пониженной биодеградируемостью
- 2150266 Крем после бритья
- 2350354 Фармацевтическое средство содержащие антагонист и фактор некроза
- 2350340 Способ коррекции процессов регенерации
- 2350309 Способ лечения избыточной массы тела с помощью рефлексотерапии
- 2250047 Профилактический продукт из хрящевой ткани гидробионтов
- 2249467 Медицинский матерьял и изделия на его основе
- 2055079 Способ получения препарата гиалуроновой кислоты
- 2349599 Биоадгезив мидии
- 2054903 Способ лечения коллагеноза у бычков на откорме
- 2249210 Способ прогнозирования предрасположенности к развитию и тяжести течения деформирующего остеоартроза коленного сустава у взрослых
- 2349339 Средство для соединительной ткани
- 2148988 Человеческий интерферона
- 2148399 Лечение атеросклероза
- 2148396 Способ определения активного вещества в дифильных мазевых основах
- 2148375 Способ диагностики близорукости
- 2348415 Способ противоспаечной терапии после хирургического вмешательства
- 2348400 Препарат на основе низкомолекулярного индуктора интерферона
- 2348386 Способ непроникающего хирургического лечения первичной открытоугольной глаукомы
- 2248213 Лечение Галактозидальной А недостаточности
- 2347586 Микрофлюидизированные эмульсии типа "масло в воде" и вакцинные средства
- 2147243 Контрастное средство
- 2146526 Лечебный препарат дисбактериоза и урогенитальных инфекций
- 2146148 Терапевтическое применение фактора роста кератиноцитов (ФРК)
- 2146139 Способ повышения активности макрофагов и комбинации для его осуществления
- 2346277 Способ диагностики специфического синовита
- 2345793 Ультразвуковые контрастные вещества и их получение
- 2345782 Терапевтические комбинации на основе PORIFERA для лечения и предотвращения кожных заболеваний
- 2245131 Способ коррекции косметических недостатков кожи
- 2245130 Способ активации восстановительных процессов в коже
- 2144833 Хондроитиназа
- 2344809 Получение твердых дозированных форм с использованием сшитого нетермопластичного носителя
- 2244540 Косметический гель для ухода за кожей лица
- 2244536 Способ лечения дегенеративно-дистрофических заболеваний тазобедренного сустава
- 2344167 Хмелевый экстракт
- 2143884 Агент регулирования дифференциации клеток кожи, культурная среда для клеток или тканей и способ регулирования дифференциации клеток кожи
- 2343932 Способ получения обладающих пониженной растворимостью в воде пленночных материалов
- 2343903 Устройство доставки лекарств для контролируемого введения препаратов
- 2048817 Способ получения материала для лечения ожогов и гнойно - некронических ран
- 2048803 Гидратантный крем
- 2242974 Средства и способы лечения воспалительных заболнваний
- 2142816 Способ получения антигерпетической вакцины
- 2342923 Средство для обработки рук с увлажняющим эффектом
- 2142781 Косметика для макияжа ресниц и бровей и агент ингирирующий рост микроорганизмов в косметических средствах
- 2242251 Трансплантируемые стенты с биоактивными покрытиями
- 2142257 Способ обработки глазных имплантантов и контакных линз
- 2342389 Мононатриевая соль
- 2342107 Способ устранения западения верхнего века при анофтальме
- 2141828 Средство, пролонгирующее эффективность чесночного порошка
- 2241489 Косметическое средство матриксных протеинов для залечивания ран
- 2241443 Средство для лечения герпеса
- 2241414 Способ получения протезов кровеносных сосудов
- 2341539 Гидрогель
- 2141324 Регулятор скорости воздействия препарата для инъекций
- 2141312 Косметическое средство для ухода за кожей лица
- 2341296 Средства и способы покрытия медицинских имплантантов
- 2341272 Средство для неспецифической иммунотерапии
- 2341266 Стенты с нанесенным покрытием содержащим N - (5-(4-(4-
- 2341257 Иммуномодулирующее средство
- 2341255 Средство для лечения климактерических расстройств
- 2240821 Способ лечения урологических инфекций
- 2140786 Способ лечения лишая
- 2140243 Способ хирургического лечения диабетической ретинопатии и отслоек сечатной оболочки
- 2240140 Медицинская многослойная повязка и изделия на ее основе
- 2240135 Культура клеток, содержащая клетки - предшественники остеонегеза, имплантант на ее основе и его использование для восстановления целостности кости
- 2240123 Экзогенные биологически активные коньюгирующие вещества
- 2139886 Фотоотвержаемое производное гликозаминогликата, сшитое производное гликозаминогликата и способы их получения, способ предотвращения клеточной и тканевой адгезии
- 2139729 Вакцина. Способ стимулирования иммунной системы
- 2339386 Средство обладающее радио - и химиозащитным действием
- 2339369 Лечение офтальмологических нарушений с использованием мочевины и ее производных
- 2139041 Гидратантный регенерирующий крем и способ его получения
- 2139039 Косметический суперкрем для ухода за кожей
- 2139017 Способ получения боисовместимого материала
- 2138503 Производные камптотецина, способы их получения, уникальное средство
- 2338556 Средство содержащие антагонист Р2Х - рецептора и нестероидное противоспалительное лекарственное средство
- 2338514 Косметическое средство для профилактики старения кожи
- 2138297 Медицинские устройства, подверженные вызываемому разложению
- 2138295 Покрытие для ран
- 2337906 Ингибиторы цитозольной фосфолипазы А2 Применение физиологически допустимого корпускулярного ферримагнитного или ферромагнитного материала. Способ формирования магнитометрического изображения
- 2137501 Устройство формирования изображения
- 2137477 Способ лечения заболеваний характеризующихся аутоиммунной агрессией
- 2137467 Крем для кожи лица и тела
- 2137449 Способ коррекции дефектов преломления в глазу млекопитающего
- 2137402 Пищевая Добавка БАД
- 2336899 Способ стимуляции миелопоэза
- 2336862 Способ получения раствора для лечения роговицы
- 2336830 Способ восстановления костных структур челюсти
- 2136696 Новый полипептид и средство против ВИЧ - Инфекции
- 2336092 Биоадгезивное средство, по существу свободное от воды
- 2336089 Средство и способ лечения заболеваний периодонтальных и пульпы
- 2336074 Средства и способы лечения заднего сегмента глаза
- 2235548 Ранозаживляющее средство
- 2135186 Способ лечения рефлекторных синдромов при остеохондрозе
- 2234945 Стабилизатор водного раствора и водосодержащего сырья
- 2334762 Растворимая ассоциативная карбоксиметилцеллюлоза
- 2234514 Макропористые хитозановые гранулы и способ их получения. Способ культивирования клеток
- 2133615 Средство для лечения неврологических заболеваний
- 2233164 Способ профилактики развития послеоперационных спаек брюшной полости
- 2133127 Неткатный материал, способ его получения и способ лечения
- 2333223 Альдегидные производные сиаловой кислоты и средства на их основе
- 2333007 Полипептидные вакцины для широкой защиты против рядов поколений менингококов с повышенной вирулентностью
- 2332985 Дозированные формы анестезирующих средств с длительным высвобождением для обезболивания
- 2132677 Косметическая маска
- 38603 Пленочный аппликатор
- 2232594 Средство содержащие ингибирующие остеокластогенез фактор и полисахарид
- 2332238 Средство для прокладок, раневых повязок и других изделий, контактирующих с кожей
- 2331668 Стромальные клетки, получение из жировой ткани, для заживления дефектов роговицы и внутриглазных дефектов и их использование
- 2331438 Альфа - 2 - Дельта Лигант для лечения симптомов нижних мочевыводящих путей
- 2331411Электропряденые аморфные фармоцевтические средства
- 2331367 Способ профилактики образования спаек и их рецидива
- 2130767 Масло в воде для получения косметических и дерматологических средств, способ косметической обработки
- 2230752 Поперечносшитые гиалуроновые кислоты и их применение в медицине
- 2230558 Способ восстановления и сохранения здоровья скмьи
- 2230550 Средства длительного высвобождения, способ их получения и применения
- 2230458 Поддержания здоровья суставов
- 2330290 Способ определения состояния метаболических процессов в ткани суставного хряща
- 2230073 Способ поперечного сшивания карбоксилированных полисахаридов
- 2329059 Способ лечения полипозного риносинусита
- 2329037 Комбинированная терапия для лечения иммуновоспалительных заболеваний
- 2128666 Гиалуроновая кислота и ее соли, способ очистки гиалуроновой кислоты, способ получения гиалуроновой кислоты. Фармацевтический препарат с гиалуроновой кислотой и средства с гиалуроновой кислотой используемые в офтальмологии
- 2328740 Способ экспресс - оценки действия зубных паст
- 2128502 Косметический гель
- 2328272 Суппозитории индуктора интерферона
- 2328268 Косметика содержащая амфолитный сополимер
- 2128057 Композиционная мембрана, способ ее получения и способ направленной регенерации тканей с ее применением
- 2128055 Средство замедленного освобождения и способ его получения
- 2128049 Свечи
- 2227743 Полипептидные варианты с повышенной гепаринсвязывающей способностью
- 2326893 Ковалентное и нековалентное сшивание гидрофильных полимеров
- 2326697 Новый перевязочный материал для быстрого заживления раневой поверхности кожи
- 2126264 Фармацевтическое средство с гиалуроновой кислотой
- 2326137 Способ получения содержащих альгинат пористых формованных изделий
- 2325902 Способ выделения гликозаминогликанов из минерализованной соединительной ткани
- 2225195 Репелленты против насекомых
- 2325193 Сосудистый стент
- 2325184 Улучшенные везикулы наружной мембраны бактерий
- 2325153 Многокомпонентная фармацевтическая дозированная форма
- 2325152 Удерживаемая в желудке система регулируемой доставки лекарственного средства
- 2029955 Способ предоперационного определения помутнения задней капсулы хрусталика при экстракции катаракты
- 2324688 Производные бисбензизоселеназолонила с противоопухолевым, противовоспалительным и антитромбоническим действием
- 2323017 Устройство и способ контролируемый доставки активных веществ в кожу
- 2323011 Содержащий Коллаген I и Коллаген II способный к рассасыванию внеклеточный матрикс, предназначенный для реконструирования хряща
- 2322955 Способ изготовления имплантанта для пластики дефектов хрящевой ткани
- 2322454 Антитело против CCR5
- 2322263 Система продолжительного высвобождения растворимого лекарственного средства
- 2221561 Витамин Е и его сложные эфиры
- 2321634 Гены участвующие в метаболизме углерода и продуцировании энергии
- 2321597 Биоматерьял, способ его приготовления и его применение, медицинское средство, имплантант и вкладыш
- 2121340 Средство для похудения
- 2220737 Средство для улучшения состояния опорно-двигательного аппарата
- 2220729 Гель используемый в стоматологии
- 2320720 Способ культивирования фибропластов для заместительной терапии
- 2320378 Накожный аппликатор
- 2320369 Средства, содержащие Альфа - 2 - Дельта Лиганды и ингибиторы обратного захвата серотонина/норадреналина
- 2320362 Местные фармацевтические средства, содержащие проантоцианидины, для лечения дерматитов
- 2320322 Биоадгезивная доставка лекарств
- 2320318 Чувствительное к температуре изменяющие состояние средство гидрогеля
- 2025120 Способ получения препарата, содержащего Фактор /G-CSF/, стимулирующий рост колоний гранулоцитов
- 2319490 Средство для введения железа при лечении синдрома беспокойных ног
- 25995 Содержащее адгезив приспособление для фиксации зубных протезов в полости рта
- 2218907 Средство для ухода за кожей лица и веками
- 2318830 Способ получения модифицированного дерматансульфата
- 2118153 Косметика - туш для ресниц
- 2217441 Способ получения полимера
- 2317296 Изетионатная соль селективного ингибитора CDK4
- 2217171 Мембрана для использования при направленной регенерации тканей
- 2317095 Экстракты ECHINACEA ANGUSTIFOLIA
- 2216332 Препарат для лечения астроза
- 2216314 Крем - маска для обезвоженной кожи
- 2316333 Средство оздоровительно-восстановительных косметических панто-магниевых ванн
- 2021304 Способ получения биологически активного средства
- 2115662 Способ получения гиалуроновой кислоты
- 2315627 Впрыскиваемые имплантанты на керамической основе для заполнения морщин, кожных впадин, шрамов
- 2315623 Средство получаемое путем лиофилизации препарата
- 2114862 Способ получения гиалуроновой кислоты
- 2314791 Лечебно-Косметическое средство
- 2314791 Косметический крем-бальзам для ухода за кожей лица и шеи
- 2214600 Способ оценки эффективности лечения неврологических проявлений
- 2114602 Способ косметической обработки
- 2114587 Раствор для защиты роговицы
- 2214283 Имплантант для подкожного или внутрикожного введения
- 2313370 Медицинские протезы, имеющие улучшенную биологическую совместимость
- 2313356 Препарат для лечения демодекоза
- 2313338 Средство на основе этиллинолеата и триэтилцитрата для лечения себореи и угрей
- 2313328 Косметика содержащая тонкодисперный и пористый порошок
- 2212880 Способ получения препарата содержащего антибиотик, с замедленным высвобождением активного вещества
- 2312640 Способ лечения Блефароконьюнктивальной формы синдрома сухого глаза
- 2017751 Способ получения гиалуроновой кислоты
- 2312145 Гены CORYNEBACTERIUM GLUTAMICUM, кодирующие белки, участвующие в синтезе мембран и мембранном транспорте
- 2311458 Белки вызывающие измененную иммуногенную реакцию. Способ их получения и использования
- 2311183 Улучшенное разделение с использованием гталуроновой кислоты
- 2311177 Ингибиторы интегрина для лечения заболевания глаз
- 2300069 Косметическая маска
- 2211024 Уход за сухой кожей
- 2310440 Раствор для защиты роговицы от повреждений
- 2309684 Лечение межфалангового остеоатроза узелковой формы
- 2309406 Способ мониторинга фиброза печени у больных хроническим гепатитом с (ХГС)
- 2209088 Опосредованная рецепторами доставка генов с использованием векторов на основе бактериофагов
- 2308967 Уменьшение объема ткани
- 2308962 Средство для опорно-дигательного аппарата
- 2308957 Способ получения препарата для мезотерапии
- 2308954 Средство для лечения ран, содержащее плазму или сыворотку крови
- 2308951 Комплексный способ профилактики вагинальных дисбактериозов
- 2308937 Косметическая биологически активная добавка и косметический литофитокомплекс на ее основе
- 2208638 ДНК (варианты), способ получения белка
- 2207885 Способ подачи небольшого объема лечебного раствора к целевому месту
- 2207858 Лишенные побочных эффектов производные простагландинов для лечения глаукомы
- 2207845 Твердая лекарственная форма пролонгированного действия
- 2207844 Препарат для местного неинвазивного применения
- 2207841 Средства с антиферментативным действием
- 2306335 Стволовые клетки и решетки полученные из жировой ткани
- 2306140 Новые рецепторы для Helicobacter pylori и их применение
- 2205612 Способ эндотелизации IN VITRO протезов кровеносных сосудов
- 2105540 Депигментирующее средство
- 2304960 Косметическое средство для кожи
- 2304616 Гены участвующие в гомеостазе и адаптации
- 2204550Способ получения длинноцепочечной N-Ацилированной кислотой Аминокислот
- 2204415 Способ получения изображения
- 2204394 Средство для лечения грибковых инфекций, желудочных язв
- 2204366 Способ хирургического лечения глаукомы
- 2104034 Вагинальное увлажняющие средство, способ его получения
- 2303991 Биологически активная добавка
- 2303990 БАД
- 2303973 Адсорбирующее изделие
- 2203676 Средство обладающее иммунокорригирующим действием
- 2203672 Способ предупреждения беременности
- 2303635 Гены кодирующие белки резистентности и толерантности к стрессам
- 2303529 Способ фиксации альгинатного геля на твердой фазе, способ получения клеточного чипа на его основе
- 2203078 Способ лечения гнойных ран
- 2302412 Гидразоно-малонитрилы
- 2102400 Способ получения гиалуроновой кислоты
- 2202356 Способ стимуляции репаративных процессов длительно незаживающих ран и трофических язв
- 2202336 Средство для ухода за кожей
- 2302231 Глазные капли
- 2102082 Способ магнитометрического исследования тела человека или животного
- 2301814 Полиакриламидный гидрогель
- 2201765 Гибридные матричные имплантанты и эксплантанты
- 2301677 Биотрансплантант для лечения дегенеративных и трвматических заболеваний хрящевой ткани и способ его получения
- 2301676 Способ лечения ревматизма
- 2301674 Способ лечения больных с переломами нижней челюсти
- 2301661 Средство с регулируемым освобождением и способ его получения
- 2005488 Средство для лечения болезней соединительной ткани
- 2200001 Крем для кожи
|
РОССИЙСКАЯ ФЕДЕРАЦИЯ

ФЕДЕРАЛЬНАЯ СЛУЖБА
ПО ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ
ПАТЕНТАМ И ТОВАРНЫМ ЗНАКАМ
|
Патент №2301814 |
(54) ПОЛИАКРИЛАМИДНЫЙ ГИДРОГЕЛЬ И ЕГО ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ ЭНДОПРОТЕЗА
(57) Реферат:
Изобретение относится к биологически устойчивым гидрогелям для использования в качестве эндопротеза, состоящего по существу из следующих компонентов: полиакриламида, который включает полимер акриламида, сшитый метилен-бис-акриламидом, в котором акриламид и метилен-бис-акриламид соединены в молярном отношении от 150:1 до 1000:1, где гидрогель промыт водой или физиологическим раствором, так чтобы в результате содержать около 0,5-3,5 мас.% полиакриламида, при этом гидрогель содержит менее 50 ч./млн мономеров акриламида и метилен-бис-акриламида, и где модуль упругости гидрогеля составляет примерно от 10 до 700 Па, а его комплексная вязкость составляет примерно от 2 до 90 Па·с. Наличие стадии промывания позволяет удалить почти все (даже следовые) количества мономеров акриламида и N,N'-метилен-бис-акриламида, что снижает токсичность и увеличивает стабильность гидрогеля. Биологически стабильный гидрогель применяется в качестве инъецируемого протеза для наполнения мягких тканей, а также для лечения недержания мочи или анального недержания или для получения протеза для лечения или профилактики недержания мочи или анального недержания. Гидрогель, полученный в несколько стадий, включающих объединение акриламида и метилен-бис-акриламида, инициирование радикальной полимеризации и промывание апирогенной водой или физиологическим раствором применяется также для лечения или профилактики пузырно-мочеточникового рефлюкса у млекопитающих. Биологически устойчивые гидрогели, используемые для лечения и профилактики недержания мочи или анального недержания, а также для лечения пузырно-мочеточникового рефлюкса содержат от 0,5 до 25 мас.% полиакриламида. 10 н. и 67 з.п. ф-лы, 3 ил., 7 табл.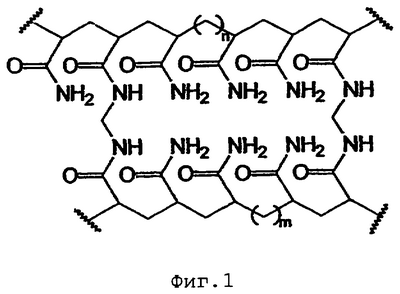
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к новому полиакриламидному гидрогелю из сшитого полиакриламида. Гидрогель можно получить смешиванием акриламида и метилен-бис-акриламида в определенном соотношении таким образом, чтобы придать гидрогелю некоторые физические свойства. Кроме того, данное изобретение относится к применению гидрогеля для получения эндопротеза для косметической хирургии и реконструктивной хирургии, применения в качестве эндопротеза (наполнителя) мягких тканей, эндопротеза для лечения недержания, эндопротеза для лечения артрита, для пластики молочной железы и для лечения рефлюкс-эзофагита.
ПРЕДПОСЫЛКИ ДЛЯ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
В качестве эндопротезов используют натуральные и синтетические полимеры, например, коллаген, сою, глицерин, силикон, поливинилпирролидон и гиалуроновую кислоту. С помощью веществ, используемых в качестве эндопротезов, обычно пытаются имитировать мягкие ткани природного происхождения, и подразумевается, что эти вещества не представляют опасности для здоровья пациента.
Полиакриламидные гели также были описаны. Патент США №5798096 относится к биосовместимому гидрогелю, содержащему от 3,5 до 6,0% сшитого полиакриламида. Однако, в патенте США №5798096 сообщают, что гидрогель неустойчив при концентрациях сшитого полиакриламида ниже 3,5%.
Патент Великобритании №2114578 относится к полиакриламидному гелю медицинского и биологического назначения, содержащему от 3 до 28% полиакриламида, а остальную часть гидрогеля составляет физиологический раствор.
Патент США №5658329 относится к имплантируемому эндопротезу, включающему оболочку, заполненную полиакриламидным гелем, который содержит от 2 до 20 мас.% полиакриламида, причем вязкость этого геля составляет от 15 до 75 Па·с.
Полиакриламидный продукт "Formacryl®" представляет собой эндопротез мягкой ткани, состоящий из 5% сетчатого полиакриламидного полимера и 95% апирогенной воды. "Formacryl®" выпускается в виде средства для инъекций медицинского или дентального назначения для коррекции врожденных или приобретенных дефектов, например, морщин, складок и шрамов. Этот эндопротез имплантируют в гиподерму с помощью шприца.
Патент США №5306404 относится к способу получения пластин полиакриламидного геля для электрофореза.
Публикация международной заявки WO 99/10021 относится к биосовместимому гидрогелю для инъекций, содержащему 0,5-10% полиакриламида и антибиотик или антисептик.
Международная заявка WO 99/10021 нацелена на решение проблемы нагноения и отторжения геля при его использовании в качестве эндопротеза.
КРАТКОЕ СОДЕРЖАНИЕ ИЗОБРЕТЕНИЯ
В целом изобретение относится к биостабильному гидрогелю, который можно получить путем объединения акриламида и метилен-бис-акриламида в таких количествах, чтобы содержание полиакриламида составляло около 0,5-25 мас.% (считая на общую массу гидрогеля); инициированием радикальной полимеризации и промыванием апирогенной водой или физиологическим раствором. Биостабильный гидрогель обычно имеет молекулярную массу от 0,01×106 до 20×106. Полимер обладает устойчивостью к биологическому расщеплению и не проникает через биологические мембраны. Полиакриламидный гидрогель по данному изобретению является полностью биосовместимым (согласно стандартному тесту ISO: - ISO-10993). Полиакриламидный гидрогель не обладает цитотоксическим действием на фибробласты человека, он нетоксичен, не является канцерогеном, аллергеном и мутагеном; устойчив к ферментативному и микробиологическому расщеплению. Кроме того, полимер не растворяется в воде. Этот гидрогель полезен в качестве материала для эндопротезов, и указанный гель изготавливают специально для исправления конкретного дефекта, требующего коррекции.
Один из аспектов данного изобретения относится к биосовместимому гидрогелю, состоящему из (i) менее чем 3,5 мас.% полиакриламида, сшитого метилен-бис-акриламидом, и (ii) апирогенной воды. Конкретно изобретение относится к гидрогелю, содержащему (i) менее чем 3,5% (мас./мас.) полиакриламида, который можно получить смешиванием акриламида и метилен-бис-акриламида, инициированием радикальной полимеризации; и промыванием апирогенной водой, причем указанное объединение акриламида и метилен-бис-акриламида проводят при мольном соотношении от 150:1 до 1000:1.
Цель данного изобретения состоит в том, чтобы предоставить гидрогель для применения в качестве эндопротеза для инъекции или имплантации, состоящий из (i) менее 3,5% (мас./мас.) полиакриламида, сшитого метилен-бис-акриламидом, и (ii) апирогенной воды или физиологического раствора. Данное изобретение относится, кроме того, к способу получения гидрогеля, включающему стадии объединения акриламида и метилен-бис-акриламида, инициирования радикальной полимеризации и промывания апирогенной водой, таким образом, чтобы содержание полиакриламида составляло около менее 3,5 мас.%.
Еще одной целью изобретения является инъецируемый или имплантируемый эндопротез, состоящий из (i) менее 3,5 мас.% полиакриламида, сшитого метилен-бис-акриламидом, и (ii) апирогенной воды или физиологического раствора. Кроме того, изобретение относится к применению гидрогеля, состоящего из (i) менее 3,5 мас.% полиакриламида, сшитого метилен-бис-акриламидом, и (ii) апирогенной воды или физиологического раствора, для получения эндопротеза для косметической хирургии, реконструктивной хирургии и терапии. Здесь также излагается способ получения инъецируемого или имплантируемого эндопротеза, состоящий из стадий объединения акриламида и метилен-бис-акриламида (в таком соотношении, чтобы содержание полиакриламида составляло менее 3,5 мас.%), инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором.
Кроме того, изобретение относится к способу лечения косметического или функционального дефекта с помощью инъецируемого или имплантируемого биосовместимого эндопротеза, состоящему из
(а) получения полиакриламидного гидрогеля, причем вышеуказанный гидрогель содержит менее 3,5 мас.% указанного полиакриламида, сшитого с помощью метилен-бис-акриламида,
(b) инъекции или имплантации достаточного количества указанного гидрогеля в область тела, пораженную косметическим или функциональным дефектом.
Гидрогели с более высоким содержанием полиакриламида также включены в данное изобретение особенно относительно некоторых медицинских показаний. Еще одна цель данного изобретения относится к применению гидрогеля, состоящего из (i) более 9,5 мас.% полиакриламида (считая на общую массу гидрогеля) и (ii) апирогенной воды или физиологического раствора, для получения имплантируемого эндопротеза для пластики молочной железы.
Еще одна цель данного изобретения относится к применению гидрогеля, содержащего 9,5 мас.% полиакриламида (считая на общую массу гидрогеля) для получения имплантируемого эндопротеза для контурной пластики.
В данном изобретении обращаются к лечению рефлюкс-эзофагита. Применение гидрогеля, содержащего более 6,0 мас.% полиакриламида (считая на общую массу гидрогеля), для получения имплантируемого эндопротеза для лечения (рефлюкс) эзофагита является еще одной целью изобретения, как и способ лечения рефлюкс-эзофагита, состоящий в имплантации или инъекции эндопротеза из полиакриламидного гидрогеля, в котором гидрогель содержит более 6,0 мас.% полиакриламида (считая на общую массу гидрогеля).
К пластике молочной железы также обращаются в данном изобретении. Кроме того, данное изобретение относится к способу косметического изменения молочной железы или осуществления частичной или полной пластики молочной железы у женщин, состоящему в имплантации полиакриламидного гидрогеля; причем (i) вышеуказанный гидрогель содержит более 9,5 мас.% полиакриламида (считая на общую массу гидрогеля) и (ii) апирогенную воду или физиологический раствор.
Косметическая хирургия тела (исключая лицо) упоминается в данной заявке как контурная пластика и также рассматривается здесь. Кроме этого, данное изобретение нацелено на способ косметического изменения формы тела млекопитающего (контурная пластика), состоящий в имплантации протеза из полиакриламидного гидрогеля; причем (i) вышеуказанный гидрогель содержит более 9,5 мас.% полиакриламида (считая на общую массу гидрогеля) и (ii) апирогенную воду или физиологический раствор.
Другой аспект данного изобретения относится к гидрогелю для применения в качестве эндопротеза-наполнителя мягких тканей из вышеуказанного гидрогеля, получаемого путем объединения акриламида и метилен-бис-акриламида, инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором таким образом, чтобы получить гидрогель, содержащий менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля.
Еще один аспект данного изобретения относится к применению гидрогеля, содержащего менее 3,5 мас.% полиакриламида (считая на общую массу гидрогеля) для получения эндопротеза для наполнения мягких тканей. Аналогично, изобретение относится к способу наполнения мягких тканей млекопитающих, состоящему во введении эндопротеза, где эндопротез состоит из гидрогеля, содержащего менее 3,5 мас.% полиакриламида (считая на общую массу гидрогеля).
Еще одна цель данного изобретения состоит в предоставлении протеза для увеличения объема мягких тканей, причем вышеуказанный протез является инъецируемым и состоит из вышеуказанного гидрогеля, получаемого путем объединения акриламида и метилен-бис-акриламида, инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором таким образом, чтобы получить гидрогель, содержащий менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля.
Важный аспект данного изобретения относится к биостабильному гидрогелю для применения в лечении и профилактике недержания и пузырно-мочеточникового рефлюкса, причем вышеуказанный гидрогель получают путем объединения акриламида и метилен-бис-акриламида (в таких количествах, чтобы содержание полиакриламида составляло от 0,5 до 25 мас.%, считая на общую массу гидрогеля); инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором.
Еще один аспект данного изобретения относится к применению биостабильного гидрогеля, содержащего от 0,5 до 25 мас.% полиакриламида (считая на общую массу гидрогеля), для получения эндопротеза для лечения и профилактики недержания и пузырно-мочеточникового рефлюкса и к способу лечения или профилактики недержания и пузырно-мочеточникового рефлюкса, состоящего во введении гидрогеля млекопитающему, причем вышеуказанный гидрогель содержит от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля.
Важная цель данного изобретения состоит в предоставлении протеза для увеличения резистентности каналов, выбранных из группы, состоящей из мочеиспускательного канала, прямой кишки или ободочной кишки и мочеточника, для лечения недержания мочи, недержания кала и пузырно-мочеточникового рефлюкса, соответственно, причем вышеуказанный протез является инъецируемым и состоит из биостабильного гидрогеля по данному изобретению.
Одна из целей данного изобретения состоит в том, чтобы предложить полиакриламидный гидрогель для применения в качестве протеза для прибавления, увеличения или замены хряща в интраартикулярной полости сустава. Мягкий материал обладает по меньшей мере двумя полезными свойствами, которые состоят в том, что, во-первых, материал является как биосовместимым, так и биоустойчивым; и, во-вторых, материал обладает механической упругостью, не образует гранулы, не рвется и не рассыпается или не разрушается легко при механической нагрузке. Материал может быть инъецирован или имплантирован, и его можно обрабатывать таким образом, чтобы распределить опору, обеспечиваемую материалом, равномерно или в соответствии с нуждами пациента. Гидрогель также служит смазкой для сустава и ранее существовавшего хряща.
Основная цель данного изобретения состоит в том, чтобы предложить гидрогель для применения в лечении или профилактике артрита, причем вышеуказанный гидрогель можно получать путем объединения акриламида и метилен-бис-акриламида в таких количествах, чтобы содержание полиакриламида составляло около 0,5-25 мас.%, считая на общую массу полученного гидрогеля, инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором.
Еще один аспект изобретения относится к применению гидрогеля, содержащего около 0,5-25 мас.% полиакриламида, считая на общую массу гидрогеля, для изготовления эндопротеза для частичного снятия или профилактики симптомов, связанных с артритом.
Кроме того, предложение способа лечения или профилактики артрита, включающий введение гидрогеля млекопитающему, причем вышеуказанный гидрогель, содержит от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля, является дополнительной целью данного изобретения.
Еще один аспект данного изобретения относится к протезу для лечения артрита, где протез состоит из полиакриламидного гидрогеля, содержащего от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля, причем вышеуказанный протез вводят в интраартикулярную полость сустава. Другими словами, протез по данному изобретению предназначен для наращивания или замены хряща в интраартикулярной полости сустава; причем вышеуказанный протез состоит из полиакриламидного гидрогеля, содержащего от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Гидрогели и их получение
Успех пластической или реконструктивной хирургии в большой степени зависит от физических свойств используемых материалов. Эти материалы должны безусловно быть биосовместимыми, стабильными и нетоксичными, но они также должны обладать физическими характеристиками, которые позволяют имитировать ткани организма, заменяемые ими, как в случае реконструктивной хирургии, или имитировать ткани вблизи эндопротеза, как в косметической хирургии.
Вещества, такие как коллаген, рассасываются в организме за короткое время. В случае таких материалов, как силикон и соя, сталкиваются с серьезными проблемами, связанными с безопасностью пациентов. В настоящее время существует потребность в безвредном, биосовместимом материале, который обладает физическими характеристиками, позволяющими имитировать мягкие ткани.
Авторы данного изобретения неожиданно обнаружили, что полиакриламидный гидрогель, содержащий менее 3,5 мас.% полиакриламида (считая на общую массу гидрогеля), является эффективным эндопротезом с полезными физическими характеристиками, причем этот полиакриламидный гель стабилен, в отличие от геля, описанного в патенте США №5798096. Гидрогель, полученный способом по данному изобретению, подвергают поперечному сшиванию с метилен-бис-акриламидом, причем степень сшивания такова, что эндопротез, изготовленный из этого гидрогеля, обладает полезными физическими характеристиками. Гидрогель по данному изобретению представляет собой новый химический объект, на что указывают его новые и полезные физические характеристики. Эти вторичные характеристики показывают, что степень сшивания в гидрогеле по данному изобретению сильно отличается от степени сшивания в полиакриламидных гидрогелях, полученных ранее описанными способами. Степень сшивания является фактором, определяющим физические свойства гидрогеля.
Авторы данного изобретения предложили биостабильный гидрогель, получаемый путем объединения акриламида и метилен-бис-акриламида (в количествах, необходимых для того, чтобы содержание полиакриламида составляло от 0,5 до 25 мас.%, считая на общую массу гидрогеля); инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором. Молекулярная масса биостабильного гидрогеля обычно составляет от 0,01×106 до 20×106. Полимер устойчив, не подвергается биологическому расщеплению и не проникает через биологические мембраны. Полиакриламидный гидрогель по данному изобретению полностью биосовместим (согласно стандартному тесту ISO - ISO-10993). Полиакриламидный гидрогель не обладает цитотоксическим действием на фибробласты человека, он нетоксичен, не является канцерогеном, аллергеном или мутагеном; устойчив к ферментативному и микробиологическому расщеплению. Кроме того, полимер не растворяется в воде. Главная цель данного изобретения состоит в предложении гидрогеля, содержащего менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля, где вышеуказанный гидрогель можно получить путем объединения акриламида и метилен-бис-акриламида, инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором; причем указанный гидрогель является биосовместимым, а указанное смешивание проводят при молярном соотношении реагентов от 150:1 до 1000:1.
Другими словами, один из аспектов изобретения относится к гидрогелю, содержащему (i) менее 3,5 мас.% полиакриламида (сшитого метилен-бис-акриламидом), считая на общую массу гидрогеля, и (ii) не менее 95% апирогенной воды или физиологического раствора.
Еще один аспект изобретения относится к гидрогелю для использования в качестве инъецируемого или имплантируемого эндопротеза, причем вышеуказанный гидрогель содержит (i) менее 3,5 мас.% полиакриламида (сшитого метилен-бис-акриламидом), считая на общую массу гидрогеля, и (ii) не менее 95% апирогенной воды или физиологического раствора.
Во всех вариантах осуществления данного изобретения, в которых гидрогель содержит менее 3,5 мас.% полиакриламида (считая на общую массу гидрогеля), гидрогель обычно содержит, кроме того, не менее 95% апирогенной воды или физиологического раствора.
Гидрогель содержит менее 3,5 мас.% полиакриламида, причем предпочтительно не менее 0,5%, например, не менее 1%, предпочтительно не менее 1,5% полиакриламида, например, не менее 1,6 мас.% полиакриламида, считая на общую массу гидрогеля.
Гидрогели, содержащие менее 3,5% полиакриламида, химически и биологически стабильны, но могут быть очень (жидко) текучими, так что их можно характеризовать как вещества, обладающие комплексной вязкостью не менее 2 Па·с, например, не менее 3, 4 или 5 Па·с. В приемлемом варианте осуществления данного изобретения гидрогель, содержащий менее 3,5% полиакриламида, характеризуется комплексной вязкостью приблизительно от 2 до 90 Па·с, например, 5-80 Па·с, предпочтительно от около 6 до 76 Па·с, например, от около 6 до 60, от 6 до 40, от 6 до 20, например, от 6 до 15 Па·с.
Гидрогель, содержащий менее 3,5% полиакриламида, обладает упругими свойствами, по которым гидрогель можно характеризовать, как вещество с модулем упругости не менее 10 Па, например, не менее 20, 25, 30, 31, 32, 33, 34 или 35 Па, таким как, например, не менее 38 Па. Обычно гидрогель имеет модуль эластичности от около 10 до 700 Па, например, от около 35 до 480 Па.
Эти реологические характеристики частично определяются степенью сшивания и степенью набухания гидрогеля. Гидрогель, содержащий менее 3,5% полиакриламида, можно характеризовать такой степенью сшивания полиакриламида, которая обеспечивает эффективную концентрацию поперечных связей от около 0,2 до 0,5%, предпочтительно от около 0,25 до 0,4%.
Концентрация поперечных связей в свою очередь частично определяется молярным соотношением между акриламидом и метилен-бис-акриламидом. Обычно указанное соотношение составляет от 175:1 до 800:1, например, от 225:1 до 600:1, предпочтительно от 250:1 до 550:1, наиболее предпочтительно от 250:1 до 500:1. Абсолютное и относительное количество окислительно-восстановительного агента (TEMED) и инициатора также влияют на степень сшивания. Как можно видеть в таблицах 1-4, авторы данного изобретения регулируют эти параметры, чтобы воздействовать на реологические свойства гидрогеля.
Биосовместимые гидрогели по данному изобретению, содержащие менее 3,5% полиакриламида, можно в подходящем случае охарактеризовать, по крайней мере частично, одним или несколькими из следующих свойств: (i) концентрацией поперечных связей от 0,2 до 0,5%; (ii) модулем упругости (G') от 10 до 700 Па; (iii) комплексной вязкостью от 2 до 90 Па·с; (iv) содержанием сухого вещества менее 3,5%, например, менее 3,4, например, менее 3,3, например, менее 3,2, например, менее 3,1, например, менее 3,0, например, менее 2,9, например, менее 2,8, например, менее 2,7, например, менее 2,6%; (v) показателем преломления в интервале между 1,33 и 1,34.
Как было указано, во всех аспектах данного изобретения, в которых гидрогель включает менее 3,5 мас.% полиакриламида (считая на общую массу гидрогеля), гидрогель, кроме того, содержит не менее 95% апирогенной воды или физиологического раствора. Во всех вариантах осуществления данного изобретения, в которых гидрогель дополнительно содержит физиологический раствор, гидрогель предпочтительно содержит менее 3 мас.% полиакриламида (считая на общую массу гидрогеля).
Гидрогель по данному изобретению практически не содержит других веществ, которые вносят вклад в содержание твердых веществ, кроме акриламида, метилен-бис-акриламида и остаточных количеств (если они имеются) инициаторов. Гидрогель практически не содержит никаких других полимеров. Гидрогель содержит не менее 75 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды. В приемлемом варианте осуществления данного изобретения гидрогель содержит не менее 80 мас.% апирогенной воды или физиологического раствора, предпочтительно не менее 85 мас.%, более предпочтительно не менее 90 мас.%, еще предпочтительнее не менее 95 мас.% апирогенной воды или физиологического раствора.
Гидрогель содержит апирогенную воду или физиологический раствор. Следовательно, смешивание реагентов и разливка геля могут быть выполнены в апирогенной воде или в физиологическом растворе. Применение физиологического раствора конечно будет увеличивать общую массу твердых веществ в гидрогеле, но не влияет существенным образом на содержание полиакриламида во время реакции полимеризации.
Приемлемый физиологический раствор имеет осмолярность, аналогичную осмолярности тканевой (интерстициальной) жидкости. Приемлемые физиологические растворы включают группу (но не ограничиваются ею), выбранную из 0,25-1% водного раствора хлорида натрия, раствора Рингера-Локка, раствора Эрла, раствора Хэнкса, среды Игла, 0,25-1% раствора глюкозы, раствора хлорида калия и раствора хлорида кальция. В предпочтительном варианте осуществления данного изобретения физиологический раствор представляет собой 0,8-1% водный раствор хлорида натрия, например, 0,8; 0,9 или 1% водный раствор хлорида натрия.
Как было указано, апирогенная вода или физиологический раствор используются для процесса промывания геля. Процесс промывания частично служит для удаления почти всех, даже следовых количеств мономеров акриламида и N,N'-метилен-бис-акриламида. Эти мономеры токсичны для пациента, а также плохо влияют на стабильность гидрогеля. Процесс промывания предпочтительно проводить так, чтобы концентрации мономеров акриламида и N,N'-метилен-бис-акриламида в гидрогеле составляли меньше 50 млн-1, более предпочтительно меньше 40 млн-1, например, меньше 30 млн-1, наиболее предпочтительно меньше 20 млн-1, обычно меньше 10 млн-1, обычно меньше 5 млн-1. В способе по данному изобретению стадия промывания включает набухание продукта в течение 50-250 ч, обычно в течение 70-200 ч.
Неожиданно было обнаружено, что гидрогель, содержащий 3,5% полиакриламида, является стабильным при очень низком содержании твердых веществ, в отличие от информации, раскрытой в патенте США №5798096. Полиакриламидные гидрогели с содержанием твердых веществ 0,5 мас.% получены авторами данного изобретения. Предпочтительные варианты гидрогеля по данному изобретению содержат не меньше 0,5 мас.%, например, не меньше 1 мас.%, предпочтительно не меньше 1,5 мас.% полиакриламида, например, не меньше 1,6 мас.% полиакриламида (считая на общую массу гидрогеля).
Гидрогель является, в подходящем случае, композицией из цепей сшитого полиакриламида и апирогенной воды. Вода, содержащаяся в гидрогеле как часть композиции, слабо (не жестко) связана полимерными цепями. Когда гидрогель находится в организме, некоторые молекулы воды перемещаются в ткань осмосом, что в результате приводит к разглаживанию поверхности кожи под действием геля. В варианте осуществления изобретения, в котором гидрогель содержит физиологический раствор, изоосмолярность физиологического раствора и тканевой (интерстициальной) жидкости сводит к минимуму иммунные реакции.
Как было указано, на физические свойства гидрогеля частично влияет степень сшивания. Степень сшивания можно частично регулировать с помощью молярного соотношения сшивающего агента (метилен-бис-акриламида) и акриламида.
Следовательно, еще одной целью данного изобретения является метод получения гидрогеля, состоящий из стадий объединения акриламида и метилен-бис-акриламида, инициирования радикальной полимеризации и промывания апирогенной водой, таким образом, чтобы содержание полиакриламида составляло менее 3,5 мас.% (считая на общую массу гидрогеля). Способ предпочтительно таков, что дает гидрогель, который содержит не менее 0,5 мас.%, например, не менее 1 мас.%, предпочтительно не менее 1,5 мас.% полиакриламида, например, не менее 1,6 мас.% полиакриламида (считая на общую массу гидрогеля).
В особенно предпочтительном варианте осуществления изобретения гидрогель можно получить путем объединения акриламида и метилен-бис-акриламида в таких количествах, чтобы гель содержал от 1,6 до 3,5 мас.% полиакриламида, и в молярном отношении от 150:1 до 1000:1; инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором.
Объединение акриламида и метилен-бис-акриламида предпочтительно проводят при молярном соотношении акриламида и метилен-бис-акриламида от 175:1 до 800:1, например, от 225:1 до 600:1, предпочтительно от 250:1 до 550:1, наиболее предпочтительно от 250:1 до 500:1.
Получение гидрогеля по данному изобретению наглядно описано в примере 1. Гидрогель, обладающий требуемыми физическими характеристиками, получен путем объединения акриламида и метилен-бис-акриламида в соотношении приблизительно 250:1, например, 252:1, 254:1, 256:1, 258:1, 260:1, а также путем объединения акриламида и метилен-бис-акриламида в соотношении приблизительно 500:1, например, 498:1, 496:1, 494:1, 492:1, 490:1. Гидрогель по данному изобретению предпочтительно имеет комплексную вязкость приблизительно от 2 до 90 Па·с, например, 5-80 Па·с, обычно от около 6 до 76 Па·с, например, от около 6 до 60, от 6 до 40, от 6 до 20, например, такую как 6-15 Па·с. В приемлемом варианте осуществления изобретения стадия промывания включает набухание продукта стадии инициирования радикальной полимеризации до тех пор, пока его комплексная вязкость не составит приблизительно от 6 до 100 Па·с.
В приемлемом варианте осуществления данного изобретения гидрогель имеет такую степень сшивания, что его комплексная вязкость составляет не менее 2 Па·с, например, не менее 3, 4 или 5 Па·с, например, не менее 5,5 Па·с, например, не менее 6 Па·с, предпочтительно не менее 6,2 Па·с.
Модуль упругости является другой характеристикой гидрогеля, указывающей частично на степень сшивания гидрогеля по данному изобретению. Обычно степень сшивания такова, что модуль упругости гидрогеля составляет не менее 10 Па, например, не менее 25, 30, 31, 32, 33, 34 или 35 Па, например, не менее 38 Па. Гель можно характеризовать величиной модуля упругости приблизительно от 10 до 700 Па, например, приблизительно от 35 до 480 Па.
Как было указано, в наиболее предпочтительном варианте осуществления изобретения гидрогель можно получить путем объединения акриламида и метилен-бис-акриламида в таких количествах, чтобы гель содержал от 1,6 до 3,5 мас.% полиакриламида, и при молярном отношении от 150:1 до 1000:1; инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором. Стадия инициирования радикальной полимеризации дает гидрогель, по-прежнему содержащий токсичные реагенты и еще не обладающий полезными физическими характеристиками гидрогеля по данному изобретению. Стадия промывания гидрогеля включает набухание гидрогеля, полученного на стадии радикального иницирования, до тех пор, пока его комплексная вязкость не составит приблизительно от 2 до 90 Па·с.
Или же стадия промывания может включать набухание продукта стадии инициирования радикальной полимеризации до тех пор, пока его модуль упругости не составит приблизительно от 10 до 70 Па, например, приблизительно от 35 до 480 Па.
Естественно, низкая степень сшивания обычно в результате приводит к более высокой скорости набухания, следовательно, к снижению содержания сухого вещества (процентного содержания акриламида), а также уменьшению модуля упругости и вязкости. Таким образом, наряду со степенью сшивания, время, в течение которого гидрогель подвергается промыванию, в существенной степени влияет на физические характеристики геля.
Обычно стадия промывания включает набухание продукта в течение 80-100 ч, например, 90-95 ч. Это обычно приводит к увеличению массы гидрогеля приблизительно на 75-150%, обычно примерно на 100%.
Кроме того, количество инициатора радикальной полимеризации на стадии инициирования и количество соинициатора влияют на длину цепи и, следовательно, на физические характеристики гидрогеля. В типичном примере получения гидрогеля в качестве соинициатора используют N,N,N',N'-тетраметилэтилендиамин (TEMED), а персульфат аммония (APS) используют в качестве инициатора свободно-радикальной полимеризации (окислительно-восстановительная система). Для получения гидрогеля по данному изобретению требуются адекватные количества инициатора и соинициатора. В качестве примера отметим, что недостаточное количество этих реагентов приведет к уменьшению длины цепи и в результате повлияет на степень сшивания и, следовательно, на физические характеристики гидрогеля. Другие условия реакции, например, температура, также оказывают воздействие на длину цепи.
Как было указано, степень сшивания влияет на физические характеристики гидрогеля. Степень сшивания гидрогеля по данному изобретению можно определить косвенным образом, как описано выше, с помощью модуля упругости и/или комплексной вязкости. Другой мерой степени сшивания гидрогеля является эффективная концентрация поперечных связей (плотность полимерной сетки) в нем. Гидрогель по данному изобретению предпочтительно содержит от 1,6 до 3,5% (мас./мас.) полиакриламида, сшитого метилен-бис-акриламидом, и (ii) апирогенную воду или физиологический раствор, предпочтительно, чтобы степень сшивания, определенная с помощью эффективной концентрации поперечных связей в геле, была такой, чтобы эффективная концентрация поперечных связей составляла приблизительно 0,2-0,5%, предпочтительно около 0,25-0,4%.
В приемлемом варианте осуществления данного изобретения гидрогель может содержать от 1,6 до 3,25% (мас./мас.) полиакриламида, например, от 1,8 до 3,1; от 2,0 до 3,0; от 2,0 до 2,9, предпочтительно от 2,0 до 2,8 (мас./мас.) полиакриламида.
Применение полиакриламидных гидрогелей в медицине
Гидрогели по данному изобретению предназначены для применения в качестве эндопротезов. В эндопротезах по данному изобретению и в способах лечения, описанных здесь, гидрогель может использоваться в любых вариантах осуществления данного изобретения, описанных выше.
Эндопротез можно вводить в организм индивида путем инъекции, например, шприцем или катетером, или хирургической имплантацией. В варианте осуществления изобретения, в котором гидрогель предназначен для применения в качестве имплантируемого эндопротеза, гидрогель может необязательно служить веществом-наполнителем для оболочки, которую вместе с наполнителем имплантируют в организм. Таким образом, гидрогель или эндопротез могут включать силиконовую оболочку, в которую помещен гидрогель.
Как было указано, целью данного изобретения является способ лечения косметических или функциональных дефектов с помощью инъецируемого биосовместимого эндопротеза, включающий
(а) получение 1,6-3,5 мас.% полиакриламидного гидрогеля, причем вышеуказанный полиакриламид сшивают метилен-бис-акриламидом,
(b) инъекцию достаточного количества указанного гидрогеля в область тела с косметическим или функциональным дефектом. Гидрогель, инъецируемый в указанную область, можно получить смешиванием акриламида и метилен-бис-акриламида, взятых в таких количествах, чтобы содержание полиакриламида составляло 1,6-3,5 мас.% и при молярном соотношении от 150:1 до 1000:1, инициированием радикальной полимеризации и промыванием апирогенной водой или физиологическим раствором. Соотношение акриламида и метилен-бис-акриламида предпочтительно является таким, чтобы комплексная вязкость составляла приблизительно от 2 до 90 Па·с, например, 5-80 Па·с, предпочтительно от около 6 до 76, или таким, чтобы модуль упругости составлял приблизительно от 10 до 700 Па, например, около 35-480 Па. Стадию промывания можно осуществлять до такой степени, чтобы комплексная вязкость составляла приблизительно от 6 до 80 Па·с, или чтобы модуль упругости составлял от 10 до 700 Па, например, 35-480 Па.
Эндопротез может состоять из любого варианта гидрогеля, из описанных в данной заявке, и может быть предназначен или для инъекций, или для имплантации. Таким образом, важным аспектом данного изобретения является применение гидрогеля, содержащего (i) менее 3,5 мас.% полиакриламида, сшитого метилен-бис-акриламидом, и (ii) не менее 95% апирогенной воды или физиологического раствора, для получения эндопротеза для косметической хирургии, реконструктивной хирургии и терапии. В особенно интересных вариантах осуществления данного изобретения эндопротез является инъецируемым.
Еще одной целью данного изобретения является гидрогель, как описано выше, для применения в получении эндопротеза. Конкретно, цель изобретения состоит в применении геля, содержащего (i) от 1,6 до 3,5 мас.% полиакриламида, сшитого метилен-бис-акриламидом, и (ii) апирогенную воду или физиологический раствор, для получения эндопротеза для косметической хирургии, реконструктивной хирургии и терапии. Эндопротез по данному изобретению может быть инъецируемым или имплантируемым. Косметическая и реконструктивная хирургия позволяет исправлять черты лица, например, изменяя форму или размер губ, устранять морщины и лечить асимметрии лица или изменять форму носа, а также выполнять множество коррекций лица, известных специалисту в данной области. Кроме того, косметическая и реконструктивная хирургия делают возможным коррекцию дефектов, вызванных травмой или связанных с заболеваниями, такими, например, как гемиплегия.
Гидрогель, как описано выше, может быть применен для получения эндопротезов. Таким образом, еще одной целью данного изобретения является инъецируемый эндопротез, содержащий (i) от 1,6 до 3,5 мас.% полиакриламида, сшитого метилен-бис-акриламидом, и (ii) апирогенную воду или физиологический раствор. Инъецируемый эндопротез по данному изобретению предпочтительно имеет комплексную вязкость приблизительно от 2 до 90 Па·с, например, 5-80 Па·с, предпочтительно от около 6 до 76 Па·с, например, от около 6 до 60, от 6 до 40, от 6 до 20, например, от 6 до 15 Па·с. В тех случаях, где эндопротез вводится с помощью инъекции, гидрогель обычно несколько текуч по своей природе.
Многие заболевания имеют отношение к потере эффективной активности ткани на функциональной границе раздела между двумя органами. Например, недержание мочи связано с недостаточной активностью сфинктера между мочевым пузырем и мочеиспускательным каналом. Инъекция или имплантация эндопротеза, изготовленного из гидрогеля по данному изобретению, в проксимальную подслизистую основу мочеиспускательного канала приводит к сужению мочеиспускательного канала, что позволяет в значительной степени контролировать заболевание. Аналогично, рефлюкс-эзофагит связан с недостаточной резистентностью ткани между пищеводом и желудком. Путем инъекции или имплантации эндопротеза, изготовленного из гидрогеля по данному изобретению, вдоль сфинктера между пищеводом и желудком, можно уменьшить контакт между содержимым желудка и пищевода. Таким образом, в приемлемых вариантах осуществления данного изобретения гидрогель используют для получения эндопротеза для лечения недержания мочи и рефлюкс-эзофагита. Эндопротез вообще можно применять для лечения заболеваний, связанных с недостаточной резистентностью на функциональной границе раздела между двумя органами или между частями одного органа.
Содержание твердых веществ от процентного содержания акриламида, как определяют после стадии промывания, а также степень сшивания адаптируют к конкретному применению эндопротеза, получаемого из гидрогеля. В предпочтительных вариантах осуществления данного изобретения протез предпочтительно получают из гидрогеля, содержащего 1,6-3,25% (мас./мас.) полиакриламида, например, 1,8-3,1; 2,0-3,0; 2,0-2,9; предпочтительно 2,0-2,8% (мас./мас.) полиакриламида. Другими словами, предпочтительная степень сшивания гидрогеля, предназначенного для коррекции недостатков лица, может быть такой, чтобы комплексная вязкость гидрогеля составляла приблизительно от 2,0 до 15 Па·с, например, от около 5,5 до 15 Па·с, например, от 6 до 12 Па·с. Альтернативно, предпочтительная степень сшивания гидрогеля, предназначенного для коррекции недостатков лица, может быть такой, чтобы модуль упругости составлял от около 10 до 100 Па, например, от приблизительно 35 до 75, конкретно, от 35 до 60 Па, например, 35-50 Па.
С помощью эндопротезов можно исправлять дефекты, которые являются результатом травм, таких, например, как опухоли или физические ранения, а также врожденные дефекты.
В приемлемом варианте осуществления данного изобретения гидрогель, как описано выше, используется в качестве материала-наполнителя, чтобы наполнить или частично наполнить емкость или оболочку на основе силикона для получения имплантируемого эндопротеза. Таким образом, дополнительной целью данного изобретения является имплантируемый эндопротез, состоящий из (i) гидрогеля, содержащего от 1,6 до 3,5% (мас./мас.) полиакриламида, сшитого метилен-бис-акриламидом, и апирогенную воду или физиологический раствор; (ii) силиконовой оболочки, приспособленной для размещения вышеуказанного гидрогеля. Гидрогель, используемый для заполнения или частичного заполнения силиконовой оболочки, может быть гидрогелем, получаемым объединением акриламида и метилен-бис-акриламида в таких количествах, чтобы получить гидрогель с содержанием полиакриламида от 1,6-3,5 мас.%, и в молярном соотношении от 150:1 до 1000:1; инициированием радикальной полимеризации и промыванием апирогенной водой или физиологическим раствором. В вариантах осуществления данного изобретения, в которых эндопротез является имплантируемым, изготовление указанного эндопротеза из гидрогеля необязательно дополнительно включает стадию введения указанного гидрогеля в силиконовую оболочку.
После того, как гидрогель помещают в силиконовую оболочку, она предпочтительно может быть герметизирована химическим, механическим или термическим способом или с помощью лазера или света. Обычно внешняя поверхность оболочки модифицирована химически или физически так, что она является биосовместимой и имеет коэффициент трения, позволяющий свести к минимуму ее перемещение или выскальзывание из положения, в которое она была помещена.
В другом варианте осуществления данного изобретения эндопротез может содержать лекарственное средство для терапевтического применения.
Полиакриламидный гидрогель в качестве эндопротеза (наполнителя) мягких тканей
В данном аспекте изобретения эндопротез предназначен для коррекций лица, увеличения объема губ и контурной пластики тела.
Предполагалось, что термин "лицевой (лицо)" в этом аспекте изобретения означает все то, что имеет отношение ко всем областям лица, например, но не исключительно, щеки, челюсть (подбородок), шея, лоб, область под глазами, область головы и нос.
Предполагалось, что термин "контурная пластика тела" означает косметическую или реконструктивную хирургию, которая осуществляет наращивание объема мягких тканей с целью исправления косметических и некосметических дефектов мягких тканей организма, за исключением мягких тканей лица, губ, молочных желез и полового члена.
В данном аспекте изобретения термин "гидрогель" относится к полиакриламидному полимеру по данному изобретению, содержащему менее 3,5% полиакриламида и не менее 95% апирогенной воды или физиологического раствора, тогда как термин "эндопротез" относится к гидрогелю, который находится в организме.
Полиакриламидный гидрогель можно получить полимеризацией мономеров - акриламида и N,N-метилен-бис-акриламида - при радикальном инициировании, с последующим промыванием полимера апирогенной водой или физиологическим раствором. Промывание полимера приводит в результате к набуханию геля, которое объясняется абсорбцией апирогенной воды или физиологического раствора полимером. Набухание гидрогеля влияет на содержание твердого вещества в геле, т.е. на количество полимерного вещества - полиакриламида. Содержание твердого вещества в гидрогеле влияет, по крайней мере частично, на физические (реологические) характеристики гидрогеля и, следовательно, на его способность имитировать ткани человека, когда его используют в качестве эндопротеза.
Авторы данного изобретения получили гидрогель, обладающий нужными реологическими характеристиками, для того, чтобы он мог функционировать в качестве эндопротеза наполнителя мягких тканей, который является совершенно нетоксичным, стабильным и нерассасываемым. Авторы данного изобретения разработали гидрогель, который особенно подходит для применения в качестве эндопротеза для косметической и реконструктивной хирургии лица, для контурной пластики и для увеличения объема губ или их изменения. В этом аспекте данного изобретения гидрогель не предназначен для применения в качестве эндопротеза для увеличения груди или полового члена.
Первая сторона этого аспекта данного изобретения относится к гидрогелю для применения в качестве эндопротеза наполнителя мягких тканей; указанный гидрогель можно получить путем объединения акриламида и метилен-бис-акриламида в таких количествах, чтобы получить гидрогель с содержанием полиакриламида от 1,6-3,5% (мас.), считая на общую массу гидрогеля; инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором. Обычно гидрогель получают указанным смешиванием акриламида и метилен-бис-акриламида при их молярном соотношении от 150:1 до 1000:1. Гидрогель, полученный таким образом, имеет структурную формулу, представленную на фиг.1, он является стерильным, прозрачным или бесцветным и его pH составляет от 6,5 до 9,0, обычно от 7,0 до 9,0.
Кроме того, гидрогель по данному изобретению устойчив при воздействии кислорода, высокого давления, высоких и низких температур, ферментов и бактерий.
Этот аспект изобретения относится к применению гидрогеля, содержащего менее 3,5 мас.% полиакриламида (считая на общую массу гидрогеля), для изготовления эндопротеза для наполнения мягких тканей. Если учитывать, что гидрогель в этом аспекте изобретения предназначен для использования в качестве эндопротеза, он должен быть стабилен. Кроме того, если гидрогель в этом аспекте изобретения предназначен для применения в качестве эндопротеза для выбранных частей человеческого тела, то гидрогель обычно содержит не менее 0,5 мас.% полиакриламида (считая на общую массу гидрогеля), предпочтительно, не менее 1,0 мас.% полиакриламида, например, не менее 1,6 мас.% полиакриламида (считая на общую массу гидрогеля). Обычно в гидрогеле по данному изобретению содержание твердых веществ может составлять 5; 1,6; 1,7; 1,8; 1,9; 2,0; 2,1; 2,2; 2,3; 2,4; 2,5; 2,6; 2,7; 2,8; 2,9; 3,0; 3,1; 3,2; 3,3; 3,4 или 3,5 мас.% полиакриламида (считая на общую массу гидрогеля).
В предпочтительном варианте осуществления этого аспекта данного изобретения гидрогель содержит около 1,9-2,9 мас.% полиакриламида (считая на общую массу гидрогеля). Кроме того, гидрогель обычно содержит не менее 95 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды. В предпочтительном варианте гидрогель содержит не менее 96 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды, более предпочтительно не менее 97 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды, например, 95%; 95,5%; 96%; 96,5%; 97% или 97,5% (мас.) апирогенной воды или физиологического раствора, предпочтительно апирогенной воды.
Приемлемый физиологический раствор имеет осмолярность, аналогичную осмолярности тканевой (интерстициальной) жидкости. Приемлемые физиологические растворы включают группу (но не ограничиваются ею), выбранную из 0,25-1% водного раствора хлорида натрия, раствора Рингера-Локка, раствора Эрла, раствора Хэнкса, среды Игла, 0,25-1% раствора глюкозы, раствора хлорида калия и раствора хлорида кальция. В предпочтительном варианте осуществления данного изобретения физиологический раствор представляет собой приблизительно 0,8-1,0% водный раствор хлорида натрия, например, 0,8; 0,9 или 1% водный раствор хлорида натрия.
Для процесса промывания геля применяют апирогенную воду или физиологический раствор. Процесс промывания частично служит для удаления почти всех, даже следовых количеств мономеров акриламида и N,N'-метилен-бис-акриламида. Эти мономеры токсичны для пациента, а также плохо влияют на стабильность гидрогеля. Процесс промывания предпочтительно проводить так, чтобы концентрации мономеров акриламида и N,N'-метилен-бис-акриламида в гидрогеле составляли меньше 50 млн-1, более предпочтительно меньше 40 млн-1, например, меньше 30 млн-1, наиболее предпочтительно меньше 20 млн-1, обычно меньше 10 млн-1, наиболее предпочтительно меньше 5 млн-1.
Содержание твердых веществ в гидрогеле по данному изобретению по существу полностью определяется вкладом полиакриламида и N,N'-метилен-бис-акриламида и остаточных количеств инициатора. Гидрогель практически не содержит никаких других полимеров.
Как было указано, гидрогель по данному изобретению биосовместим, нетоксичен, не является аллергеном, не способен рассасываться, химически инертен и устойчив к действию кислорода, высокого давления, высоких и низких температур, ферментов и бактерий. Если гидрогель подвергается избыточному воздействию УФ-облучения, его физические характеристики изменяются, и он превращается в вещество, похожее на клей. Преимуществом является то, что это вещество также нетоксично.
При введении гидрогеля эндопротез окружается тонким слоем соединительной ткани, что позволяет эндопротезу стать стабильной частью соединительной ткани. Благодаря биостабильности гидрогеля и тонкому слою соединительной ткани, эндопротез может быть легко удален из организма пациента, когда он находится в подкожной области. Это преимущество, по крайней мере частично, объясняется стабильностью гидрогеля, которая, в свою очередь, по крайней мере частично, обусловлена процессом промывания.
Несколько факторов влияют на реологические характеристики гидрогеля, например, относительное количество используемого мономера, относительное количество инициатора, температура, время полимеризации и другие параметры процесса полимеризации, а также процесс промывания. Таким образом, процесс полимеризации может давать гидрогели, с множеством значений вязкости и содержанием твердых веществ менее 3,5 мас.%. Данное изобретение направлено на гидрогель в качестве эндопротеза наполнителя мягких тканей и, следовательно, предпочтительно, если гидрогель имеет вязкость, соответствующую вязкости мягких тканей, которые он предназначен имитировать. Гидрогель по данному изобретению обычно предназначен для применения в качестве инъецируемого эндопротеза для косметической или реконструктивной хирургии лица, косметической или реконструктивной хирургии тела (контурная пластика) и для увеличения объема губ или реконструктивной пластики губ.
Гидрогель по этому аспекту данного изобретения может быть предназначен для инъекций или имплантации в подкожный слой эпидермы, предпочтителен инъецируемый гидрогель.
В еще одном варианте осуществления данного изобретения эндопротез предназначен для применения в косметической или реконструктивной хирургии лица, и вязкость гидрогеля составляет приблизительно от 2 до 100 Па·с, предпочтительно около 5-90 Па·с, например, приблизительно от 10 до 60 Па·с. Наиболее предпочтительно, когда эндопротез, предназначенный для применения в косметической или реконструктивной хирургии лица, вводят путем инъекции гидрогеля.
Вязкость гидрогеля может варьироваться в зависимости от условий и той области эпидермы лица, куда требуется ввести наполнитель мягких тканей (например, подбородок, в отличие от щеки). Соответственно, гидрогель может быть предназначен для применения в косметической или реконструктивной хирургии лица и иметь комплексную вязкость приблизительно от 2 до 20 Па·с, предпочтительно около 2-18 Па·с, например, приблизительно от 2 до 15, более предпочтительно от 2 до 7 Па·с, наиболее предпочтительно от 3 до 5 Па·с.
В типичных вариантах осуществления данного изобретения эндопротез может предназначаться для коррекции недостатков контура лица, вызванных старением, угреватостью, травмой, хирургической операцией, инфекцией или врожденными пороками. Обычно в коррекции нуждаются такие черты лица, как, например, скуловые кости, носогубные складки, брови сдвинутые (сросшиеся) в области надпереносья, вогнутые очертания рта, подбородок, размер или форма губ, а также другие недостатки мягких тканей лица. Гидрогель восстанавливает контуры кожи, исправляя недостатки контуров мягких тканей лица, например, морщины и складки. Гидрогель можно использовать для получения инъецируемого гидрогеля для увеличения губ или исправления множества эстетических недостатков, вызванных врожденными дефектами, травматическими или возрастными изменениями.
Как было указано, этот аспект изобретения относится к использованию гидрогеля для получения эндопротеза для наполнения мягких тканей, выбранных из мягких тканей лица и губ и мягких тканей тела. Гидрогель по данному изобретению, предназначенный для применения в косметической и реконструктивной хирургии тела (контурная пластика), предпочтительно имеет комплексную вязкость приблизительно 5-50 Па·с, предпочтительно около 7-40 Па·с, наиболее предпочтительно около 7-30 Па·с.
В варианте осуществления данного изобретения, в котором гидрогель применяют для получения эндопротеза для увеличения объема губ или реконструкции губ, комплексная вязкость гидрогеля составляет предпочтительно около 2-10 Па·с, более предпочтительно 2-7 Па·с, наиболее предпочтительно около 3-5 Па·с.
Еще одна цель данного аспекта изобретения состоит в том, чтобы предложить протез для наращивания мягкой ткани, причем указанный протез является инъецируемым и содержит полиакриламидный гидрогель; причем вышеуказанный гидрогель можно получить путем объединения акриламида и метилен-бис-акриламида в таких количествах, чтобы содержание полиакриламида в гидрогеле составляло менее 3,5 мас.%, считая на общую массу гидрогеля; инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором.
Протез по данному аспекту изобретения предпочтительно включает гидрогель, содержащий не менее 0,5 мас.% полиакриламида (считая на общую массу гидрогеля), предпочтительно не менее 1 мас.% полиакриламида, более предпочтительно не менее 1,5 мас.% полиакриламида, например, не менее 1,6 мас.% полиакриламида (считая на общую массу гидрогеля). Обычно гидрогель содержит около 1,9-2,9 мас.% полиакриламида (считая на общую массу гидрогеля). Протез состоит из гидрогеля, который обычно содержит не менее 95 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды.
Еще один аспект данного изобретения относится к способу наполнения мягких тканей, состоящему во введении эндопротеза, где эндопротез состоит из гидрогеля, содержащего менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля. Гидрогель может быть таким, как описано выше.
В другом варианте осуществления изобретения протез включает клетки, например, стволовые клетки. Полиакриламид предоставляет отличные темплат и матрицу для роста клеток. Хотя гидрогель по данному изобретению позволяет, как таковой, чтобы тонкий слой соединительной ткани из тела пациента окружал протез, использование клеток в комбинации с гидрогелем по данному изобретению при получении протеза дает возможность клеточного приживления к окружающей ткани.
Способ по данному аспекту изобретения обычно состоит во введении гидрогеля по данному изобретению путем инъекции гидрогеля в подкожный слой в вариантах осуществления изобретения, в которых эндопротез предназначен для косметической или реконструктивной хирургии лица и контурной пластики. В варианте осуществления изобретения, в котором эндопротез предназначен для увеличения объема губ или реконструкции губ, инъекцию делают над мышечной тканью губы.
Дополнительной целью данного изобретения является применение гидрогеля, содержащего (i) более 9,5 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) апирогенную воду или физиологический раствор, для получения эндопротеза для контурной пластики. Этот способ косметического изменения тела млекопитающих (контурная пластика), включающий имплантацию эндопротеза из полиакриламидного гидрогеля, который содержит (i) более 9,5 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) апирогенную воду или физиологический раствор, может быть осуществлен путем инъекции или имплантации гидрогеля в мягкие ткани пациента.
Как было указано, другой вариант осуществления данного аспекта изобретения состоит во введении гидрогеля по данному изобретению в комбинации с клетками, например, стволовыми клетками, чтобы дать возможность клеточного приживления протеза.
Способ по данному аспекту изобретения может включать более одной инъекции для того, чтобы охватить нужную область или достичь желаемого эффекта. Гель для инъекций обычно хранят в шприце, подходящем для инъекции такого количества, которое требуется для лечения в один сеанс. В зависимости от пораженной области, количество геля и, следовательно, объем шприца могут изменяться, например, шприц объемом 0,25-25 мл, например шприц, выбранный из шприцев на 0,5 мл, 0,7 мл, 1,0 мл, 1,5 мл, 2,0 мл, 2,5 мл, 5,0 мл, 7,5 мл, 10 мл, 12,5 мл, 15 мл, 20 мл, 25 мл. Очевидно, протез для применения в хирургии лица и для увеличения объема губ, будет предоставлен в виде набора шприцев с гелем различного объема, который обычно меньше объемов, предлагаемых для протеза, предназначенного для контурной пластики. Например, протез для увеличения объема губ может предоставляться в объемах 0,5 мл, 0,7 мл или 1,0 мл, тогда как протез для контурной пластики может предоставляться в объемах 2,0 мл, 5,0 мл или 10 мл. Эти примеры даны как чисто иллюстративные и не предназначены для ограничения объема изобретения каким-либо образом - протез по данному изобретению может быть предложен в любом объеме, необходимом для осуществления способа.
Как было указано, гель является биосовместимым. Способ по данному изобретению не включает прибавление к гидрогелю антибиотиков, анальгетиков или противовоспатительных средств.
В предпочтительном варианте осуществления изобретения, в котором способ состоит в инъекции эндопротеза, а инъекция включает использование шприца с тонкой иглой, например, иглы 21-29 G. Нужное количество геля вводят подкожно с обратно-поступательным ходом иглы. После осуществления инъекции, может потребоваться несложная процедура для того, чтобы получить равномерное распределение геля. Послеоперационный отек можно лечить прикладыванием льда к месту отека, а в течение первых 2-3 дней после инъекции пациент может испытывать слабую боль и может появиться покраснение.
В варианте осуществления данного изобретения, включающем инъекцию эндопротеза для увеличения губ или коррекции лица, игла шприца обычно является особенно тонкой, например, 25-29 G. Для контурной пластики могут использоваться иглы 21-23 G.
Полиакриламидный гидрогель для пластики молочной железы
Применение гидрогеля, содержащего (i) менее 3,5 мас.% полиакриламида и не менее 95% апирогенной воды или физиологического раствора, для получения эндопротеза для пластики молочной железы является предпочтительным вариантом осуществления этого аспекта данного изобретения. Наиболее предпочтительно, если эндопротез является имплантируемым и дополнительно содержит силиконовую оболочку, в которую помещен гидрогель.
В варианте осуществления изобретения, в котором гидрогель содержит менее 3,5 мас.% полиакриламида, гидрогель предпочтительно содержит не менее 1 мас.% полиакриламида, считая на общую массу гидрогеля, предпочтительно не менее 1,5 мас.%, например, не менее 1,6 мас.% полиакриламида, считая на общую массу гидрогеля.
Гидрогели, применяемые для пластики молочной железы, которые содержат менее 3,5 мас.% полиакриламида, предпочтительно являются инъецируемыми. Указанные инъецируемые эндопротезы по данному изобретению предпочтительно имеют комплексную вязкость от около 2 до 90 Па·с, например, 5-80 Па·с, предпочтительно от около 6 до 76 Па·с, например, от около 6 до 60, от 6 до 40, от 6 до 20, например, от 6 до 15 Па·с.
Еще одна цель данного изобретения базируется на получении авторами данного изобретения гидрогеля с высоким содержанием твердых веществ. Применение гидрогеля, содержащего (i) более 9,5 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) апирогенную воду или физиологический раствор, для получения эндопротеза для пластической операции увеличения или реконструкции молочных желез является дополнительной целью изобретения. Другими словами, дополнительной целью изобретения является способ изменения молочной железы млекопитающих или осуществления частичной или полной реконструкции молочной железы женщин, включающий имплантацию эндопротеза из полиакриламидного гидрогеля; причем указанный гидрогель содержит более 9,5 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) не менее 75% апирогенной воды или физиологического раствора.
В варианте осуществления изобретения, в котором гидрогель для пластики молочной железы содержит более 9,5 мас.% полиакриламида, считая на общую массу гидрогеля, гидрогель обычно содержит менее 25 мас.% полиакриламида, считая на общую массу гидрогеля, например, менее 20%.
Протез для пластики молочной железы, в котором гидрогель содержит более 9,5 мас.% полиакриламида, обычно является имплантируемым. В вышеописанных вариантах осуществления данного изобретения эндопротез может дополнительно включать силиконовую оболочку.
В случае коррекции последствий частичной или полной ампутации молочной железы, эндопротез может быть инъецируемым или имплантируемым. Когда эндопротез является имплантируемым, эндопротез может содержать гидрогель по данному изобретению как таковой. Размер и форма геля могут фиксироваться путем получения гидрогеля в форме или отливке или приданием гидрогелю нужной формы и размера. В качестве альтернативы можно до или во время имплантации геля поместить его в силиконовую оболочку, которая частично служит для того, чтобы в нее помещали вышеуказанный гидрогель.
В вариантах осуществления данного изобретения, в которых предпочтительным является имплантируемый эндопротез, включающий силиконовую оболочку, гидрогель может быть до некоторой степени текучим или какой-либо фиксированной формы. В вариантах осуществления данного изобретения, в которых эндопротез дополнительно включает силиконовую оболочку и гидрогель имеет фиксированную форму, размер и форму приспосабливают к нуждам пациента, и они могут фиксироваться путем получения геля в форме или отливке или приданием гидрогелю нужной формы и размера. Оболочку также можно приспособить к размерам и форме гидрогеля, который в нее будет помещен. В вариантах осуществления данного изобретения, в которых имплантируемый эндопротез не включает дополнительно силиконовую оболочку, а гидрогель имплантируется как таковой, гидрогель обычно имеет фиксированную форму. Как было указано, форма и размер могут быть приспособлены к нуждам пациента, и они могут фиксироваться путем получения геля в форме или отливке или приданием гидрогелю нужной формы и размера.
Когда эндопротез инъецируют для коррекции частичной или полной ампутации молочной железы, эндопротез предпочтительно получают из гидрогеля, содержащего 2,0-3,0% полиакриламида, например, 2,2-3,0% полиакриламида и обладающего комплексной вязкостью от около 10 до 90 Па·с, например, от 20 до 90, 30 до 90 или от 40 до 90 Па·с, и модулем упругости от около 50 до 700 Па, например, от 75 до 600, от 100 до 500, предпочтительно от около 200 до 500 Па. Обычно гидрогель имеет комплексную вязкость не менее 10 Па·с, например, не менее 15 Па·с, предпочтительно не менее 20 Па·с, более предпочтительно не менее 30 Па·с, наиболее предпочтительно не менее 40 Па·с.
Полиакриламидный гидрогель для лечения недержания и пузырно-лоханочного рефлюкса
Потеря сознательного управления мышцами сфинктера лежит в основе недержания мочи и кала. Недержание мочи, неспособность сознательно удержать мочу в мочевом пузыре, является распространенным заболеванием у пожилых людей. Сокращение мышцы-сжимателя мочевого пузыря может быть самопроизвольным, вызванным стрессом, рефлекторным или вынужденным. Сокращение мышцы-сжимателя, вызванное стрессом, приводит к невольному мочеиспусканию, если не происходит управляемого сокращения мышцы сфинктера мочевого пузыря. В случае, когда потеряно управление мышцей сфинктера мочевого пузыря, мочеиспускание может быть вызвано легким стрессом, например, слабыми абдоминальными сокращениями во время деятельности днем, чиханием, кашлем, смехом, выделением газов, неожиданными событиями и бесчисленным множеством других стимулов, которые могут привести к сокращению мышцы-сжимателя. Недержание мочи и кала могут быть вызваны возрастом, травмой (например, параплегия) или связаны с наследственностью.
Пузырно-лоханочный рефлюкс является результатом уменьшенной мочеточниковой резистентности, когда моча из мочевого пузыря отливается назад в почку. Это может привести к переносу бактерий из мочевого пузыря обратно через мочеточник, почечную чашку (calyceal dilation), почечные пирамиды и почки, а это может привести к инфекциям и рецидивному пиелонефриту, а также вызвать физиологическое повреждение почечной паренхимы. Это может привести к почечной недостаточности.
Недержание мочи, недержание кала и пузырно-лоханочный рефлюкс можно лечить путем увеличения резистентности прохода через мочеиспускательный канал, толстую кишку или прямую кишку (или canalis analis), и мочеточник, соответственно; известных под названием процессов объемоувеличения.
Попытки лечения недержания мочи включают использование гидравлических аппаратов (например, описанных в опубликованной заявке на международный патент WO 01/50833 и патенте США №4969474) и другой управляемой аппаратуры, например, протезных сфинктеров с надувной манжеткой (например, описанных в патенте США №4571749 и заявке на международный патент WO 01/47433), снижение веса, физические упражнения, лекарственную терапию и хирургическую операцию, обычно подразумевающие подъем шейки мочевого пузыря или создание увеличенной резистентности через мочеточник, с помощью окружающих тканей или протезного материала. Для этой цели обычно используют такие материалы, как коллаген, политетрафторэтилен (ПТФЭ), силикон и тефлон.
Для лечения недержания кала предназначены управляемые и регулируемые устройства, например, описанные в публикации международной заявки WO 01/47431. C пузырно-лоханочным рефлюксом борются хирургическим путем (расширением мочеточника, обычно в детстве) и с помощью антибиотиков.
Главная цель данного аспекта изобретения состоит в предложении полиакриламидного гидрогеля, для увеличения резистентности в соответствующих каналах при лечении недержания и пузырно-лоханочного рефлюкса.
В патенте США №6129761 сообщают о применении инъецируемого геля и клеточных композиций для этой цели. Композиции представляют собой суспензии клеток, смешанных с биосовместимым и биорасщепляемым полимером. Полимер предоставляет среду и матрицу для роста клеток и клеточного приживления к окружающим тканям. Рост клеток совпадает с расщеплением полимера и приводит в результате к нужному росту тканей. Полимерные материалы, о которых сообщают в патенте США №6129761, состоят из альгинатов, например, модифицированных альгинатов, бактериальных полисахаридов, например, gellan gum, растительных полисахаридов, например, каррагинанов, гиалуроновых кислот, блоксополимеров полиэтиленоксида и полипропиленгликоля, белков, например, фибрина, коллагена и желатина, смесей полиэтиленоксида и полиакриловой кислоты, сшитого хитозана, фотохимически сшитых ненасыщенных этиленовых групп, макромеров, например, ПЭГ-олиголактилакрилатов, полиэтиленимина, полилизина, поли(виниламина) и поли(аллиламина). В патенте США №6129761 не сообщается о применении устойчивых полиакриламидных гидрогелей, но имеются данные о применении способного к расщеплению поли(виниламина). Биостабильные полимеры, например, биостабильный полиакриламид по данному изобретению, непригодны для способа, описанного в патенте США №6129761, учитывая требования к полимеру по изобретению, изложенному в этом патенте США, разлагаться, по способу в соответствии с указанным изобретением.
Российский патент №2148957 относится к способу лечения случаев пузырно-лоханочного рефлюкса с помощью полиакриламидного гидрогеля.
Веществами для инъекции, используемыми до сих пор с этой целью, являются синтетические вещества (тефлон, силикон, частицы угля) и природные вещества (экстракт соединительной ткани, жир). Долговременный эффект для приблизительно половины лечившихся пациентов после наблюдения в течение одного года был относительно слабым с рецидивами недержания. Таким образом, существует потребность в веществе, которое является биосовместимым с тканью, но в то же время не поглощается и не выделяется организмом (биологически стабильно). Кроме того, вещество должно иметь соответствующие реологические характеристики, чтобы эффективно работать.
Цель этого аспекта данного изобретения состоит в том, чтобы предложить биосовместимый и биологически стабильный полиакриламидный гидрогель для увеличения резистентности каналов для лечения недержания и пузырно-лоханочного рефлюкса.
Подразумевается, что термин "биостабильный" означает, что вещество не разрушается в сколько-нибудь значительной степени в интерстициальной жидкости или тканях организма.
Одна сторона данного аспекта изобретения относится к биостабильному гидрогелю, получаемому путем объединения акриламида и метилен-бис-акриламида в таких количествах, чтобы полиакриламид составлял около 0,5-25 мас.%, считая на общую массу гидрогеля; радикального иницирования и промывания апирогенной водой или физиологическим раствором, для применения в лечении и профилактике недержания и пузырно-лоханочного рефлюкса. Молекулярная масса биостабильного гидрогеля составляет от 0,01×106 до 20×106. Полимер устойчив к биологическому расщеплению и не проникает сквозь биологические мембраны. Полиакриламидный гидрогель по данному изобретению является полностью биосовместимым (по стандартному тесту ISO: ISO-10993). Полиакриламидный гидрогель не обладает цитотоксическим действием на фибробласты человека, он нетоксичен, не является канцерогеном, аллергеном и мутагеном; устойчив к ферментативному и микробиологическому расщеплению. Кроме того, полимер не растворяется в воде.
Авторы данного изобретения обнаружили, что биостабильный гидрогель эффективен в качестве наполнителя и пригоден для лечения недержания и пузырно-лоханочного рефлюкса, принимая во внимание, что этот гель биосовместим, не подвергается биологическому расщеплению и не перемещается из места введения в канал.
Биостабильный гидрогель по данному аспекту изобретения обычно получают путем объединения акриламида и метилен-бис-акриламида при молярном соотношении реагентов от 150:1 до 1000:1. В предпочтительном варианте осуществления данного изобретения гидрогель содержит менее 15 мас.% полиакриламида, считая на общую массу гидрогеля, предпочтительно менее 10%, более предпочтительно менее 7,5%, еще более предпочтительно менее 5%, наиболее предпочтительно менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля.
Учитывая, что гидрогель по этому аспекту данного изобретения предназначен для применения в качестве постоянного эндопротеза, он должен быть стабильным. Кроме того, принимая во внимание, что гидрогель по данному изобретению предназначен для применения в качестве эндопротеза для избранных частей человеческого тела, гидрогель обычно содержит не менее 0,5 мас.% полиакриламида, считая на общую массу гидрогеля, предпочтительно не менее 1 мас.% полиакриламида, более предпочтительно не менее 1,5 мас.% полиакриламида, например, не менее 1,6 мас.% полиакриламида, считая на общую массу гидрогеля. Обычно гидрогель по данному изобретению может иметь массовое содержание твердых веществ (сухого остатка) 1,5; 1,6; 1,7; 1,8; 1,9; 2,0; 2,1; 2,2; 2,3; 2,4; 2,5; 2,6; 2,7; 2,8; 2,9; 3,0; 3,1; 3,2; 3,3; 3,4 или 3,5 мас.% полиакриламида (считая на общую массу гидрогеля).
Для лечения пузырно-мочеточникового рефлюкса гидрогель предпочтительно содержит менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля, и приблизительно 96,5% апирогенной воды или физиологического раствора, как, например, 97,5% апирогенной воды или физиологического раствора.
Вязкость биостабильного гидрогеля обычно такова, что его можно вводить путем инъекции. В подходящем варианте осуществления данного изобретения комплексная вязкость гидрогеля составляет приблизительно от 2 до 50 Па·с, например, около 2-40 Па·с, предпочтительно около 2-30 Па·с, более предпочтительно около 2-20 Па·с.
Протез может иметь такую вязкость, чтобы его можно было ввести путем инъекции. В одном из вариантов осуществления данного изобретения, где гидрогель инъецируют, комплексная вязкость гидрогеля составляет приблизительно от 2 до 30 Па·с, например, около 2-20 Па·с, предпочтительно около 3-18 Па·с, наиболее предпочтительно около 3-15 Па·с, например, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15 Па·с.
Протез также обладает упругими свойствами, обусловленными, по меньшей мере частично, высокой способностью гидрогеля связывать воду. Это очень важно, по крайней мере, с точки зрения долговечности и способности обеспечивать сопротивление движению через каналы. В предпочтительном варианте осуществления изобретения модуль упругости гидрогеля по данному изобретению составляет от 1 до 200 Па, например, около 2-175 Па, обычно около 5-150 Па, например, 10-100 Па.
Обычно отношение модуля упругости к комплексной вязкости протеза составляет 5,8-6,4. Данное изобретение, следовательно, обеспечивает гидрогель с выгодным сочетанием характеристик: вязкости, приемлемой для инъекции геля, и упругости, обеспечивающей увеличение сопротивления (резистентности). В комбинации предпочтительных вариантов осуществления изобретения гидрогель имеет комплексную вязкость менее 25 Па·с, а модуль упругости менее 200 Па, предпочтительно, комплексную вязкость менее 15 Па·с, а модуль упругости менее 100 Па.
В примере 1 и таблицах 1-4 показаны соответствующие условия для получения иллюстративных примеров гидрогелей. Как можно видеть, в предпочтительном комбинированном варианте осуществления изобретения вязкость гидрогеля составляет менее 25 Па·с, а модуль упругости менее 200 Па; гидрогель может иметь множество значений содержания сухого остатка (мас.%).
Кроме того, в рамках предпочтительного комбинированного варианта осуществления изобретения с вязкостью гидрогеля менее 25 Па·с и модулем упругости менее 200 Па; например, в случае гидрогеля с вязкостью менее 15 Па·с и модулем упругости менее 100 Па, гидрогель может быть получен путем объединения акриламида и метилен-бис-акриламида в молярном соотношении около 275-1000, обычно 300-800, предпочтительно около 300-500.
Гидрогель по данному изобретению практически не содержит веществ, которые вносят вклад в содержание твердых веществ, кроме акриламида и N,N'-метилен-бис-акриламида и остаточных количеств инициатора (если они имеются). Гидрогель практически не содержит никаких других полимеров. Гидрогель, кроме того, содержит не менее 75 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды. В приемлемом варианте осуществления данного изобретения гидрогель содержит не менее 80 мас.% апирогенной воды или физиологического раствора, предпочтительно не менее 85%, более предпочтительно не менее 90%, еще более предпочтительно не менее 95 мас.% апирогенной воды или физиологического раствора. Приемлемый физиологический раствор имеет осмолярность, аналогичную осмолярности тканевой (интерстициальной) жидкости. Приемлемые физиологические растворы включают группу (но не ограничиваются ею), выбранную из 0,25-1% водного раствора хлорида натрия, раствора Рингера-Локка, раствора Эрла, раствора Хэнкса, среды Игла, 0,25-1% раствора глюкозы, раствора хлорида калия и раствора хлорида кальция. В предпочтительном варианте осуществления данного изобретения физиологический раствор представляет собой приблизительно 0,8-1% водный раствор хлорида натрия, например, 0,8; 0,9 или 1% водный раствор хлорида натрия.
В особенно предпочтительном варианте осуществления данного аспекта изобретения гидрогель содержит около 2,5 мас.% полиакриламида, считая на общую массу гидрогеля, и около 97,5% апирогенной воды.
Апирогенная вода или физиологический раствор используются для процесса промывания геля. Процесс промывания частично служит для удаления почти всех, даже следовых количеств мономеров акриламида и N,N -метилен-бис-акриламида. Эти мономеры токсичны для пациента, а также плохо влияют на стабильность гидрогеля. Процесс промывания предпочтительно проводить так, чтобы концентрации мономеров акриламида и N,N -метилен-бис-акриламида. Эти мономеры токсичны для пациента, а также плохо влияют на стабильность гидрогеля. Процесс промывания предпочтительно проводить так, чтобы концентрации мономеров акриламида и N,N -метилен-бис-акриламида в гидрогеле были ниже 50 млн-1, более предпочтительно ниже 40 млн-1, например, ниже 30 млн-1, наиболее предпочтительно ниже 20 млн-1, обычно ниже 10 млн-1, обычно ниже 5 млн-1. -метилен-бис-акриламида в гидрогеле были ниже 50 млн-1, более предпочтительно ниже 40 млн-1, например, ниже 30 млн-1, наиболее предпочтительно ниже 20 млн-1, обычно ниже 10 млн-1, обычно ниже 5 млн-1.
Процесс промывания может быть приемлемым образом осуществлен в течение 50-100 ч, например, в течение 20-225 ч. В таблицах 2 и 3 можно видеть, что процесс промывания обычно проводят в течение 50-100 ч, в более типичном случае в течение 70-100 ч.
В еще одном варианте осуществления этого аспекта данного изобретения протез содержит клетки, например, стволовые клетки. Полиакриламид предоставляет отличные матрицу для синтеза и матрикс для роста клеток. Применение клеток с гидрогелем по данному изобретению для получения протеза делает возможным клеточное приживление к окружающим тканям мочеточника, мочеиспускательного канала или analis canalis. Протез, состоящий из гидрогеля по данному изобретению, и соответствующих клеток дает возможность большей резистентности и большей эффективности в обеспечении резистентности.
В предпочтительном варианте осуществления данного аспекта изобретения гидрогель по данному изобретению предназначен для применения в лечении недержания мочи и кала, более предпочтительно недержания мочи.
Недержание мочи может быть стрессовым или рефлекторным или вынужденным. Обычно гидрогель по данному изобретению пригоден для лечения стрессового или рефлекторного недержания мочи.
Дополнительная цель этого аспекта данного изобретения состоит в применении данного гидрогеля для получения эндопротеза. Таким образом, еще одной целью данного изобретения является применение гидрогеля, как описано выше, содержащего около 0,5-25 мас.% полиакриламида, считая на общую массу гидрогеля, для получения эндопротеза для лечения и профилактики недержания и пузырно-мочеточникового рефлюкса.
Эндопротез в подходящем случае готовится в виде суспензии для инъекций. Суспезия содержит гомогенизированный гидрогель. Обычно этой суспезией заполняют шприц.
Еще одна цель этого аспекта данного изобретения относится к способу лечения или профилактики недержания и пузырно-мочеточникового рефлюкса, состоящему во введении млекопитающим указанного гидрогеля, содержащего около 0,5-25 мас.% полиакриламида, считая на общую массу гидрогеля. Гидрогель в любом из описанных выше вариантах осуществления изобретения пригоден для способа по данному изобретению.
При введении гидрогеля тонкий слой соединительной ткани окружает эндопротез, что позволяет эндопротезу стать постоянной частью соединительной ткани. Благодаря стабильности гидрогеля и тонкому слою соединительной ткани, эндопротез может быть удален из организма пациента. Это преимущество, по крайней мере частично, обусловлено стабильностью гидрогеля, которая, в свою очередь, по крайней мере частично, определяется процессом промывания.
Несколько факторов влияют на реологические характеристики гидрогеля, например, относительное количество используемых мономеров, относительное количество инициатора, температура и другие параметры процесса полимеризации и процесс промывания. Таким образом, процесс полимеризации может обеспечить получение гидрогелей с множеством значений вязкости. Данное изобретение предназначено для получения эндопротеза обычно для мочеиспускательного канала, прямой кишки или толстой кишки (или canalis analis) или для мочеточника и, таким образом, его можно изготавливать в соответствии с требованиями в отношении канала.
Важная цель данного изобретения состоит в том, чтобы обеспечить протез для увеличения резистентности каналов, выбранных из группы, состоящей из мочеиспускательного канала, прямой кишки или толстой кишки (или canalis analis) и мочеточника, для лечения недержания мочи, недержания кала и пузырно-мочеточникового рефлюкса, соответственно; где указанный протез вводится инъекцией и содержит гидрогель, как здесь описано.
Способ по этому аспекту изобретения предпочтительно включает введение гидрогеля путем инъекции гидрогеля в соответствующий канал. При лечении недержания мочи, обычно делают инъекцию гидрогеля в мочеиспускательный канал, конкретно под подслизистую оболочку мочеиспускательного канала. Инъекцию делают через внешнюю поверхность мочеиспускательного канала, в направлении подслизистой оболочки.
Авторы данного изобретения обнаружили, что обычно приемлемым является количество в 2-5 мл гидрогеля, чтобы обеспечить соответствующую резистентность в мочеиспускательном канале путем заполнения этого канала. Обычно инъецируют 3 мл гидрогеля, и предпочтительно 2-5 мл распределяют, размещая гель в более чем одно поперечное положение вдоль одного положения в продольном направлении мочеиспускательного канала. В особенно приемлемом варианте осуществления данного изобретения три или более порций геля помещают (делают 3 или более депо) вдоль одного положения в продольном направлении мочеиспускательного канала. Авторы данного изобретения нашли, что особенно подходящими являются порции геля (депо) на расстоянии 0,5 см от шейки мочевого пузыря.
Авторы данного изобретения показали, что инъекции в подслизистую в положения 10, 2 и 6-часовой стрелки в поперечном сечении мочеиспускательного канала являются особенно подходящими для лечения недержания мочи.
Депо обычно делают с помощью шприца или с использованием цитоскопа либо катетера. Для этих инъекций подходят иглы 21-27 G.
Для лечения недержания кала инъекцию гидрогеля обычно делают в толстую кишку или прямую кишку (canalis analis), конкретно под подслизистую оболочку толстой кишки или прямой кишки. Приемлемы инъекции 2-6 мл гидрогеля. Предпочтительно, когда гидрогель распределяют в более чем одно поперечное положение вдоль одного положения в продольном направлении толстой кишки или прямой кишки. В особенно приемлемом варианте осуществления данного изобретения делают три или более депо вдоль одного положения в продольном направлении толстой кишки или прямой кишки, предпочтительно в положениях 10, 2 и 6-часовой стрелки поперечного сечения толстой кишки или прямой кишки.
Для лечения пузырно-мочеточникового рефлюкса требуются инъекции в подслизистую мочеточника. Приемлемы инъекции 2-5 мл. Гидрогель распределяют предпочтительно более чем в одном поперечном положении для одного положения в продольном направлении мочеточника. В особенно подходящем варианте осуществления данного изобретения делают 3 или более депо вдоль одного положения в продольном направлении мочеточника, предпочтительно в положениях 10, 2 и 6-часовой стрелки поперечного сечения мочеточника.
В другом варианте осуществления данного изобретения способ включает использование протеза, содержащего клетки, например, стволовые клетки. Полиакриламид обеспечивает отличные темплат и матрицу для роста клеток. Применение клеток в сочетании с гидрогелем по данному изобретению для получения протеза делает возможным клеточное приживление к окружающим тканям мочеточника, мочеиспускательного канала или analis canalis. Способ, включающий гидрогель по данному изобретению и соответствующие клетки, дает возможность большей резистентности и большей эффективности в обеспечении резистентности.
Полиакриламидный гидрогель для лечения артрита
Артрит является дегенеративным состоянием, которое, поражая суставы, несущие массу тела, например, тазобедренный и коленный суставы, вызывает боль и приводит к ограниченной подвижности. Артрит может поражать все суставы. Дегенерация суставных и менискового хрящей может привести к повреждению поверхностей, которые разделяет хрящ, и соответственно, вызвать боль. Старение является первичной причиной дегенерации хряща. Дегенерация может быть результатом, например, врожденной предрасположенности или травмы, например, повторяющейся артикуляцией в суставе.
Артрит лечат традиционно физиотерапевтическими методами, а также применяют более радикальные методы лечения, например, хирургическую ортопедию и введение искусственных компонентов суставов. С некоторым успехом используются нестероидные противовоспалительные агенты, но эти агенты могут приводить к обратным результатам, препятствуя синтезу протеогликана в коллагене и в суставе, а также дают нежелательные побочные эффекты. Инъекции кортизона также со временем ослабляют суставный хрящ.
Мягкие эластичные материалы, которые используют для замены сустава, созданы для того, чтобы они принимали на себя нагрузку сустава и равномерно распределяли эту нагрузку. В патенте США №4344193 описан протез из силиконового каучука. Единственная проблема при работе с этими протезами состоит в закреплении протеза на месте, и разработаны различные системы для фиксации протеза (см. патенты США №5171322, №4502161 и №4919667).
Другие протезы, например, описанные в патенте США №5344459, являются надувными. Протез коленного сустава Macintosh является жестким протезом и вызывает боль при использовании.
В публикации заявки на международный патент WO 00/78356 описана инъецируемая композиция для стимулирования роста кости и/или сустава, содержащая гиалуроновую кислоту, поперечно-сшитую с сульфатированными полисахаридами.
В публикации заявки на международный патент WO 00/24129 сообщают о протезе для суставов кистей рук и ступней ног, состоящем из биосовместимого материала, например, смеси биосовместимых смолы и пластмасс. Конкретные материалы, которые упомянуты, включают полиметилметакрилатный полимер. Протез имплантируют в сустав. В публикации заявки на международный патент WO 00/59411 описан протез колена, который имплантируют хирургическим путем, в котором протез для распределения нагрузки делают из материала, содержащего отверждаемый при нагревании полимер или термопластичный полимер. Гиалуронаты и гиалуроновые кислоты используют для протезов и вводят путем инъекции в интраартикулярную полость колена для длительного ослабления боли и улучшения функционирования коленного сустава. Протез обладает достаточными вязкостью и упругостью, но он имеет тенденцию к отклонению от нужного положения, является биологически расщепляемым, и в этом случае сталкиваются с проблемами рассасывания (резорбции).
Существует потребность в дополнительных материалах для применения в качестве искусственного хряща, например, в суставах, несущих массу тела. Целью данного изобретения является материал и протез для применения в лечении артрита и для дополнения или замены хряща.
Полиакриламидный гидрогель устойчив в отношении биологического расщепления и не проникает через биологические мембраны. Полиакриламидный гидрогель по данному изобретению является полностью биосовместимым (согласно стандартному тесту ISO: ISO-10993). Полиакриламидный гидрогель не обладает цитотоксическим действием на фибробласты человека, нетоксичен, не является канцерогеном, аллергеном и мутагеном; устойчив к ферментативному и микробиологическому расщеплению. Кроме того, полимер не растворяется в воде. Что важно для настоящего изобретения, полимер обладает упругостью при механической нагрузке.
Гидрогель по этому аспекту изобретения предназначен для применения для лечения и профилактики артрита, гидрогель получают путем объединения акриламида и метилен-бис-акриламида; инициирования радикальной полимеризации и промывания апирогенной водой или физиологическим раствором, причем соединяют такие количества реагентов и промывание осуществляют таким образом, чтобы содержание полиакриламида составляло приблизительно 0,5-25 мас.%, считая на общую массу гидрогеля. Авторы данного изобретения показали, что полученный гидрогель является как биоустойчивым, так и биосовместимым, и не рассасывается в организме. Кроме того, авторы данного изобретения продемонстрировали, что гидрогель обладает упругостью при механической нагрузке.
Обычно гидрогель по данному аспекту изобретения получают путем объединения акриламида и метилен-бис-акриламида в молярном соотношении от 150:1 до 1000:1. Условия получения гидрогеля можно изменять в соответствии, например, с типом сустава, в который гидрогель предполагается вводить. Нужные реологические характеристики, например, упругость и вязкость, могут регулироваться, по крайней мере частично, содержанием твердых веществ в гидрогеле. В подходящих вариантах осуществления данного изобретения гидрогель содержит менее 15 мас.% полиакриламида, считая на общую массу гидрогеля, предпочтительно менее 10%, более предпочтительно менее 7,5%, еще более предпочтительно менее 5%, наиболее предпочтительно менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля.
Принимая во внимание, что гидрогель по данному изобретению предназначен для применения в качестве эндопротеза, он должен быть стабильным. Обычно, например, из соображений увеличенной стабильности, гидрогель содержит не менее 1 мас.% полиакриламида (считая на общую массу гидрогеля), предпочтительно не менее 1,5 мас.% полиакриламида, например, 1,6 мас.% полиакриламида (считая на общую массу гидрогеля). В подходящих вариантах осуществления данного изобретения содержание твердых веществ в гидрогеле по данному изобретению составляет 1,5; 1,6; 1,7; 1,8; 1,9; 2,0; 2,1; 2,2; 2,3; 2,4; 2,5; 2,6; 2,7; 2,8; 2,9; 3,0; 3,1; 3,2; 3,3 и 3,4 мас.% полиакриламида (считая на общую массу гидрогеля).
Смешивание предполагает смешивание составных частей реагентов акриламида и метилен-бис-акриламида, обычно дегазированных и обычно таким образом, чтобы свести к минимуму контакт с оператором. Составные части реагентов предварительно можно смешать (это необязательно) и получить инертную смесь. Инертная смесь является смесью, в которой между составляющими ее реагентами не идут химические реакции. Смешивание подразумевает объединение акриламида, метилен-бис-акриламида и компонента, являющегося радикальным инициатором. В приемлемом варианте осуществления данного изобретения предварительно приготовленную смесь акриламида, метилен-бис-акриламида (сшивающего агента) и TEMED смешивают с раствором инициатора персульфата аммония (AMPS). Однако, эти компоненты можно смешивать по отдельности или в виде множества других предварительно приготовленных смесей.
Акриламид и метилен-бис-акриламид смешивают в молярном соотношении приблизительно от 100:1 до 1000:1, обычно приблизительно от 100:1 до 900:1, предпочтительно от около 175:1 до 800:1, более предпочтительно от около 200:1 до 600:1, наиболее предпочтительно от около 250:1 до 500:1. Как показано в Таблицах 2 и 3, можно регулировать процесс и получать гидрогели с различным содержанием твердых веществ и требуемыми реологическим характеристиками. Гидрогель с нужными реологическими характеристиками получен смешиванием акриламида и метилен-бис-акриламида в соотношении около 250:1, около 260:1, около 270:1, около 280:1, около 290:1, около 300:1, около 310:1, около 320:1, около 330:1, около 340:1, около 350:1, около 360:1, около 370:1, около 380:1, около 390:1, около 400:1, около 410:1, около 420:1, около 430:1, около 440:1, около 450:1, около 460:1, около 470:1, около 480:1, около 490:1 и около 500:1.
Как можно видеть в таблицах 2 и 3, относительное количество мономера (акриламида и метилен-бис-акриламида) по отношению к TEMED остается довольно-таки постоянным от рецептуры к рецептуре. Таким образом, в предпочтительном варианте осуществления способа по данному изобретению соотношение мономеров и TEMED является относительно постоянным от партии к партии, и его не используют для регулирования реологических характеристик полимера. В варианте осуществления изобретения, в котором полимером является полиакриламид, отношение мономеров акриламида и метилен-бис-акриламида к TEMED составляет приблизительно от 100:1 до 700:1, например, от 200:1 до 600:1, обычно от 200:1 до 500:1, предпочтительно от 200:1 до 400:1, наиболее предпочтительно от 200:1 до 350:1.
Аналогично, относительное количество мономера (акриламида и метилен-бис-акриламида) по отношению к количеству инициатора остается довольно постоянным от рецептуры к рецептуре. Таким образом, в предпочтительном варианте осуществления способа по данному изобретению, соотношение мономеров и инициатора является относительно постоянным от партии к партии, и его не используют для регулирования реологических характеристик полимера. В варианте осуществления изобретения, в котором полимером является полиакриламид, отношение мономеров акриламида и метилен-бис-акриламида к инициатору составляет приблизительно от 100:1 до 700:1, например, от 200:1 до 600:1, обычно от 200:1 до 500:1, предпочтительно от 200:1 до 400:1, наиболее предпочтительно от 200:1 до 350:1.
Вязкость гидрогеля соответственно должна быть такой, чтобы его можно было инъецировать. В типичном варианте осуществления изобретения комплексная вязкость гидрогеля составляет приблизительно от 2,0 до 20 Па·с, например, от около 3 до 18 Па·с, предпочтительно от около 3 до 15 Па·с, наиболее предпочтительно от около 2 до 13 Па·с.
Гидрогель по данному изобретению практически не содержит веществ, которые вносят вклад в содержание твердых веществ, кроме акриламида, метилен-бис-акриламида и остаточных количеств инициатора (если они имеются). Гидрогель практически не содержит никаких других полимеров. Гидрогель, кроме того, содержит не менее 75 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды. В приемлемом варианте осуществления данного изобретения гидрогель содержит не менее 80 мас.% апирогенной воды или физиологического раствора, предпочтительно не менее 85%, более предпочтительно не менее 90%, еще более предпочтительно не менее 95 мас.% апирогенной воды или физиологического раствора.
Приемлемый физиологический раствор имеет осмолярность, аналогичную осмолярности интерстициальной жидкости. Приемлемые физиологические растворы включают группу (но не ограничиваются ею), выбранную из 0,25-1% водного раствора хлорида натрия, раствора Рингера-Локка, раствора Эрла, раствора Хэнкса, среды Игла, 0,25-1% раствора глюкозы, раствора хлорида калия и раствора хлорида кальция. В предпочтительном варианте осуществления данного изобретения физиологический раствор представляет собой 0,8-1% водный раствор хлорида натрия, например, 0,8; 0,9 или 1% водный раствор хлорида натрия, наиболее предпочтительно 0,9% водный раствор хлорида натрия.
Для специалиста в данной области техники ясно, что в варианте осуществления изобретения, где физиологический раствор используют и для получения, и для промывания геля, содержание твердых веществ в геле будет выше, чем вклад полиакриламида, но обычно не больше чем дополнительно 1%.
В особенно подходящем варианте осуществления изобретения гидрогель содержит приблизительно 2,5 мас.% полиакриламида, считая на общую массу гидрогеля, и приблизительно 97,5% апирогенной воды.
Апирогенную воду или физиологический раствор используют для процесса промывания геля. Процесс промывания частично служит для удаления почти всех (даже следовых) количеств мономеров акриламида и N,N'-метилен-бис-акриламида. Эти мономеры токсичны для пациента, а также плохо влияют на стабильность гидрогеля. Процесс промывания предпочтительно проводить так, чтобы концентрации мономеров акриламида и N,N'-метилен-бис-акриламида в гидрогеле составляли меньше 50 млн-1, более предпочтительно меньше 40 млн-1, например, меньше 30 млн-1, наиболее предпочтительно меньше 20 млн-1, обычно меньше 10 млн-1, особенно предпочтительно меньше 5 млн-1.
В другом варианте осуществления изобретения гидрогель имеет более твердую консистенцию, которая позволяет имплантировать его в полость сустава. В таких вариантах осуществления изобретения, где гель имеет твердую консистенцию, поверхность геля можно модифицировать таким образом, чтобы уменьшить соскальзывание геля из места, куда его имплантируют. Модификация поверхности может быть химической или физической по своей природе. Получены гидрогели с таким содержанием твердых веществ, которые похожи на твердые вещества и подходят скорее для имплантации, чем для инъекции, и их поверхность легко модифицировать.
В варианте осуществления данного изобретения, где гидрогель является имплантируемым, вязкость твердого образца очевидно очень высока. В варианте осуществления данного изобретения, где гидрогель является имплантируемым, комплексная вязкость гидрогеля составляет приблизительно от 20 до 1500 Па·с, обычно от 20 до 1000 Па·с.
В варианте осуществления этого аспекта данного изобретения, где гидрогель является имплантируемым и, кроме того, его поверхность модифицирована, в случае модификации поверхности геля химической обработкой ожидается, что химическая обработка будет касаться менее чем 1% от массы гидрогеля, считая на общую массу гидрогеля. Химическая обработка может включать агент, покрывающий поверхность, или агент, действие которого состоит в том, чтобы химически модифицировать полиакриламид на поверхности гидрогеля.
Гидрогель по этому аспекту данного изобретения применяют для получения эндопротеза, который вставляют в интраартикулярную полость сустава. Гель предназначен для применения в качестве протеза для лечения артрита. Протез по данному изобретению состоит из полиакриламидного гидрогеля, содержащего от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля, его вводят в интраартикулярную полость сустава.
Протез может состоять из любого варианта воплощения гидрогеля, как описано выше. Соответственно протез предназначен для наращивания или замены хряща в интраартикулярной полости сустава, при этом указанный протез состоит из полиакриламидного гидрогеля, содержащего от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля. Протез из гидрогеля по данному изобретению обычно, кроме того, содержит не менее 75 мас.% апирогенной воды или физиологического раствора, предпочтительно апирогенной воды. Его можно вводить имплантацией или инъекцией в интраартикулярную полость сустава. Предпочтительным является инъецируемый протез.
Протез может иметь такую вязкость, которая делает возможным его введение путем инъекции. В одном из вариантов осуществления изобретения, где гидрогель является инъецируемым, комплексная вязкость гидрогеля составляет приблизительно от 2,0 до 25 Па·с, например от около 3 до 20 Па·с, предпочтительно от около 3 до 18 Па·с, наиболее предпочтительно от около 3 до 15 Па·с, например, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15 Па·с.
Упругость гидрогеля и протеза имеет важное значение, особенно для такого варианта осуществления изобретения, где гидрогель инъецируют в сустав, несущий массу тела. В предпочтительном варианте модуль упругости гидрогеля по данному изобретению составляет приблизительно от 1 до 200 Па, например, от около 2 до 175 Па, обычно от около 5 до 150 Па, например, 10-100 Па.
Обычно отношение модуля упругости протеза к его комплексной вязкости составляет 5,8-6,4. Данное изобретение, следовательно, обеспечивает гидрогель с выгодным сочетанием характеристик: вязкости, подходящей для инъецируемости геля, и упругости, обеспечивающей способность нести нагрузку массы тела. В комбинации предпочтительных вариантов осуществления изобретения гидрогель имеет комплексную вязкость менее 25 Па·с, а модуль упругости менее 200 Па, предпочтительно, комплексную вязкость менее 15 Па·с, а модуль упругости менее 100 Па.
В примере 1 и таблицах 1, 2 и 3 представлены соответствующие условия для получения показательных примеров гидрогелей. Как можно видеть, в предпочтительном комбинированном варианте осуществления изобретения, где вязкость гидрогеля составляет менее 25 Па·с, а модуль упругости менее 200 Па, например, комплексная вязкость составляет менее 15 Па·с, а модуль упругости меньше 100 Па, гидрогель может иметь множество значений содержания сухого остатка (мас.%).
Кроме того, в предпочтительном комбинированном варианте осуществления изобретения с вязкостью гидрогеля менее 25 Па·с и модулем упругости менее 100 Па, например, в случае гидрогеля с вязкостью менее 15 Па·с и модулем упругости менее 200 Па; гидрогель получают путем объединения акриламида и метилен-бис-акриламида в молярном соотношении от около 275 до 1000, обычно 300-800, предпочтительно в соотношении около 300-500.
Гидрогель по данному изобретению обладает упругостью при механической нагрузке, а также обеспечивает смазку внутри сустава. Этим имитируется сочетание естественного хряща и синовиальной жидкости в суставе. Синовиальная жидкость продуцируется синовиальной оболочкой и образуется на границе раздела синовиальной оболочки и суставного хряща. Функцией синовиальной жидкости является питание хряща, смазка, несение нагрузки и поглощение толчков и ударов (см. Gomez and Thurston, Biorheology 30, 409-427 (1933)). Синовиальная жидкость представляет собой раствор очень сложного полимерного комплекса, имеющего каркас линейной гиалуроновой кислоты и белковые ответвления; она имеет модуль упругости G', равный 60 Па, и комплексную вязкость около 1-10 Па·с. Некоторые варианты гидрогеля по данному изобретению обладают аналогичным модулем упругости и близким значением вязкости.
Синовиальная жидкость, являясь текучей, обладает очень продолжительным временем релаксации (около 100 сек). Время релаксации определяется как время, которое требуется для того, чтобы нагрузка уменьшилась до 37% ее первоначальной величины в эксперименте по релаксации нагрузки. Это продолжительное время релаксации означает, что для быстрых движений (когда нагрузка прилагается быстро), синовиальная жидкость реагирует как очень эластичный материал, тогда как при низкой скорости приложения нагрузок она ведет себя как смазочное масло. Рецептуры гидрогеля с низкой вязкостью по данному изобретению похожи на жидкости, например, тогда, когда они гомогенизированы, и подобно жидкостям, имеют очень продолжительное время релаксации и свойства, подобные свойствам синовиальной жидкости. Данное изобретение, следовательно, обеспечивает превосходную альтернативу известным технологиям для замещения синовиальной жидкости, например, с помощью инъекций изотонической (NaCl) воды, которые проводятся лишь в течение 1-3 дней, или с помощью инъекции растворов гиалуроновой кислоты, в этом случае сталкиваются с проблемами резорбции.
Как было указано, в тех вариантах осуществления изобретения, в которых гидрогель представляет собой рецептуру с низкой вязкостью, с помощью гидрогеля пытаются имитировать, по крайней мере частично, характеристики синовиальной жидкости. В тех вариантах осуществления изобретения, в которых гидрогель представляет собой рецептуру с более высокой вязкостью, например, с вязкостью выше 10 Па·с, например, выше 15 Па·с, гидрогель имитирует в большей степени объединенные характеристики синовиальной жидкости и хряща, что выражается в том, что гидрогели являются более упругими материалами с бесконечно большими временами релаксации.
С точки зрения упругости по отношению к механической нагрузке гидрогель по данному изобретению продемонстрировал поведение полностью упругого материала. Кроме того, упругие свойства гидрогеля позволяют ему вернуться в исходное положение после снятия нагрузки в экспериментах по исследованию ползучести.
Протез можно вводить во множество интраартикулярных полостей, где указанный сустав или хрящ, присутствующий в указанном суставе, могут нуждаться в усиленной смазке, увеличенной способности выдерживать массу тела или усиленной защите противостоящих костей в суставе, как, например, в группе (но не ограничиваясь этой группой), включающей коленный сустав, тазобедренный сустав, локтевой сустав, пястно-фаланговый и межфаланговый суставы рук и ног (принимаются замечания, касающиеся других важных суставов).
При введении протеза пациенту очень важным является надлежащее положение и размещение гидрогеля. Для помощи в размещении геля очень полезна визуализация локализации протеза для индивидуального выполнения процедуры. Может быть полезно, например, в варианте осуществления изобретения, где протез вводят инъекцией, визуализировать протез с целью определить его положение и требуемое количество. Визуализации гидрогеля во время введения может способствовать радиоактивная метка гидрогеля. Так, в одном интересном варианте осуществления данного изобретения гидрогель помечают радиоактивным изотопом.
Как было указано, обработка поверхности гидрогеля может помочь удержать протез на месте внутри полости сустава. Однако, в варианте инъецируемого гидрогеля протез может удерживаться костной тканью, которая определяет границы полости, в которую инъецируют гель.
Как было также указано, один аспект данного изобретения относится к применению гидрогеля, содержащего приблизительно от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля, для получения эндопротеза для частичного снятия или профилактики симптомов, связанных с артритом. Соответственно, способ по данному изобретению можно охарактеризовать как способ лечения или профилактики артрита, состоящий во введении гидрогеля млекопитающему, причем вышеуказанный гидрогель содержит от 0,5 до 25 мас.% полиакриламида, считая на общую массу гидрогеля. Способ включает применение гидрогеля, как определено выше, и применение протеза, как определено выше.
Способ может включать первую серию или курс лечения инъекциями или имплантациями с последующим анализом, оценкой или заключением об уровне помощи, предоставляемой протезом, и последующие дополнительные серии или курсы лечения, если требуется. В варианте осуществления изобретения, в котором требуется прежде всего увеличенная способность сустава переносить нагрузку массы тела, упругость или поддержка, которые обеспечивает протез, могут со временем уменьшиться. Однако, одно преимущество способа по данному изобретению состоит в том, что инъецируемый протез можно вводить как дополнение к существующему протезу. Процедуру можно повторять так часто, как требуется пациенту, чтобы облегчить боль, связанную с его состоянием. Аналогично, в случае, когда протез вводят, прежде всего для того, чтобы усилить смазку сустава и способность протеза смазывать сустав со временем уменьшается; способ по данному изобретению, например, простую инъекцию, можно повторять, когда требуется.
Полиакриламидный гидрогель для фаллопластики
Еще одной целью данного изобретения является применение гидрогеля, содержащего (i) менее 1,6 мас.% полиакриламида, считая на общую массу гидрогеля, для получения эндопротеза для увеличения полового члена. Этот способ увеличения размера полового члена, состоящий во введении полиакриламидного гидрогеля, где гидрогель содержит менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля, обычно осуществляют посредством инъекции. Введение путем инъекции производят в кавернозную ткань.
Гидрогель обычно дополнительно содержит не менее 95% апирогенной воды или физиологического раствора. Таким образом, особенно интересный вариант осуществления данного изобретения состоит в применении гидрогеля, содержащего (i) менее 1,6 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) не менее 95% апирогенной воды или физиологического раствора для получения эндопротеза для увеличения полового члена, предпочтительно инъецируемого эндопротеза. Инъецируемые эндопротезы для увеличения полового члена обычно имеют комплексную вязкость менее 20 Па·с, например, менее 18 Па·с, предпочтительно менее 15 Па·с. Кроме того, вышеуказанные эндопротезы обычно имеют модуль упругости менее 150 Па, обычно менее 100 Па.
Еще одной целью данного изобретения является применение гидрогеля, содержащего (i) более 9,5 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) апирогенную воду или физиологический раствор, для получения имплантируемого эндопротеза для увеличения полового члена. Этот способ наращивания размера полового члена, состоящий в имплантации протеза из полиакриламидного гидрогеля, где гидрогель содержит (i) более 9,5 мас.% полиакриламида, и (ii) апирогенную воду или физиологический раствор, может быть осуществлен путем имплантации или инъекции эндопротеза.
Гидрогель протеза для увеличения полового члена, содержащий не менее 9,5 мас.% полиакриламида, имеет комплексную вязкость не менее 10 Па·с, например, не менее 15 Па·с, предпочтительно не менее 20 Па·с, более предпочтительно не менее 30 Па·с, наиболее предпочтительно не менее 40 Па·с. Гели с высокой вязкостью подходят для имплантации и имеют плотную консистенцию от полумягкой до полужесткой, соответствующую данной цели.
Полиакриламидный гидрогель для лечения эзофагита
Еще одна цель данного изобретения состоит в применении гидрогеля, содержащего (i) более 6 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) апирогенную воду или физиологический раствор, для получения эндопротеза для лечения (рефлюкс) эзофагита. В приемлемом варианте осуществления изобретения гидрогель содержит более 7, 8 или 9% полиакриламида. Этот способ лечения (рефлюкс) эзофагита, состоящий в имплантации или инъекции эндопротеза из полиакриламидного гидрогеля, где гидрогель содержит более 6 мас.% полиакриламида, считая на общую массу гидрогеля, может быть осуществлен путем имплантации или инъекции эндопротеза, обычно посредством его инъекции или имплантации в подслизистый слой ткани.
Еще одна цель данного изобретения состоит в применении гидрогеля, содержащего (i) менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля, и (ii) апирогенную воду или физиологический раствор, для получения эндопротеза для лечения (рефлюкс) эзофагита. Этот способ лечения (рефлюкс) эзофагита может осуществляться посредством имплантации или инъекции гидрогеля, где гидрогель содержит менее 3,5 мас.% полиакриламида, считая на общую массу гидрогеля. При лечении (рефлюкс) эзофагита с помощью гидрогеля, содержащего (i) менее 3,5 мас.% полиакриламида, гидрогель обычно дополнительно содержит не менее 95% апирогенной воды или физиологического раствора, и лечение обычно проводят путем инъекции. В этих вариантах осуществления данного изобретения степень сшивания может быть такой, что вязкость составляет не менее 6 Па·с, например, от 6 до 90 Па·с, например, от 10 до 80 Па·с, предпочтительно от 20 до 80 Па·с. Степень сшивания гидрогеля, используемого для получения эндопротеза для лечения (рефлюкс) эзофагита, может быть такова, что модуль упругости гидрогеля составит приблизительно от 50 до 700 Па, например, от 75 до 600 Па, например, от 100 до 500 Па, предпочтительно от около 200 до 500 Па. Обычно гидрогель имеет комплексную вязкость не менее 20 Па·с, более предпочтительно не менее 30 Па·с, наиболее предпочтительно не менее 40 Па·с.
Изобретение далее раскрывается с помощью примеров, которые не предназначены ограничивать объем изобретения каким-либо образом.
ПРИМЕРЫ
Пример 1
Получение гидрогеля
Гель представляет собой полиакриламидный гель, полученный полимеризацией мономеров акриламида и N,N'-метилен-бис-акриламида. Конечный продукт может иметь различную вязкость.
Гидрогель имеет эмпирическую формулу [C3H5NO]x[C7H10N2O2]y и структурную формулу, изображенную на фиг.1.
Гидрогель обычно содержит приблизительно 95% воды. Как было показано, концентрация мономеров акриламида и N,N'-метилен-бис-акриламида составляет меньше 10 млн-1, часто меньше 5 млн-1 и соответствует требуемой стабильности конечного продукта.
Конечный продукт должен соответствовать требованиям, касающимся величины pH, отсутствия тяжелых металлов, величины показателя преломления, стабильности, отсутствия пирогенных веществ, он должен быть стерильным, практически инертным и по существу не содержать мономеров.
Получение 1.1
Синтез гидрогеля в подходящем случае состоит из следующих операций:
1. Готовят две смеси А1 и А2. А1 содержит воду, акриламид, N,N'-метилен-бис-акриламид и N,N,N',N'-тетраметиленэтилендиамин (TEMED). А2 состоит из воды и персульфата аммония.
2. Эти две смеси соединяют в таком соотношении: 1990 мл А1 и 10 мл А2; выдерживают при 45°С и дегазируют азотом в течение 20 сек.
3. Реакционную смесь разливают в несколько лабораторных стаканов (на 100 мл).
4. Проводят полимеризацию в течение 0,5-1,5 ч.
5. Гель вынимают из формы.
6. Оставшиеся мономеры экстрагируют при помощи приведения в равновесие с WFI-водой в течение 92 ч, меняя воду несколько раз, обычно 8 раз в течение 92 ч.
7. Очищенные гели гомогенизируют путем измельчения на решетке, совершающей колебательные движения в вертикальном направлении.
8. Наполняют шприц гомогенизированным гелеобразным материалом.
9. Шприц стерилизуют в автоклаве.
Общий способ получения гидрогеля может быть кратко изложен следующим образом:
Получение 1.2
Краткое изложение способа. Гель готовят путем смешивания водного раствора мономеров - акриламида (AM) и N,N'-метилен-бис-акриламида (BISAM), используемого в качестве сшивающего агента, с N,N,N',N'-тетраметиленэтилендиамином (TEMED) в качестве соинициатора, и персульфатом аммония (APS), используемым в качестве инициатора свободно-радикальной полимеризации (окислительно-восстановительная система). Посредством дегазации объема раствора азотом начинают полимеризацию. После окончания полимеризации гель переносят в промывной бак с поддонами из сетчатого материала, на которые помещают гель. Во время промывания водой гель набухает, а остатки мономера экстрагируют. Набухший гель подают и закачивают в устройство для наполнения, где гелем заполняют шприц, который подвергают стерилизации в автоклаве.
Получают два различных состава - с низкой и высокой конечной вязкостью. Оба состава имеют содержание твердых веществ менее 3,5 мас.% и комплексную вязкость в интервале от 2 до 50 Па·с, обычно от 3 до 20 Па·с.
| Таблица 1 |
| Химический компонент |
Низкая конечная вязкость |
Высокая конечная вязкость |
| Акриламид |
502 г |
547 г |
N,N -метилен-бис-акриламид -метилен-бис-акриламид |
2,2 г |
4,6 г |
| TEMED |
3,0 г |
2,6 г |
| Пиросульфат аммония (APS) |
5,4 г |
5,0 г |
| Апирогенная вода |
Добавить 10 л |
Добавить 10 л |
Показанные выше методики являются типичными для получения гидрогеля, и их можно регулировать в определенных пределах.
Получение 1.3
Полиакриламидные гидрогели, полученные в процессе сшивания на автоматической линии
Особенно интересный способ получения гидрогелей по данному изобретению включает процесс сшивания на входе. Два отдельных и окончательно дегазированных потока, один из которых представляет собой премикс акриламида, метилен-бис-акриламида (сшивающего агента) и TEMED, а другой представляет собой раствор инициатора APS, закачивают в статический смеситель для перемешивания, химического инициирования и последующей экструзии далее в трубчатый реактор, изготовленный из тефлона или стали, в котором происходит полимеризация. Промывание геля упрощается, благодаря большой площади поверхности геля из реактора.
Путем подбора концентраций мономера, сшивающего агента и инициатора и их молярных соотношений и путем регулирования скоростей двух потоков и температуры полимеризации возможно получение гелей, которые отличаются степенью сшивания и содержанием твердых веществ.
Получение 1.4
Реагенты смешивают в соотношениях, показанных в таблицах 2, 3 и 4, промывают как описано в таблицах (апирогенной водой, если не указано другое) и получают гидрогели с низкой, средней и высокой вязкостью. Получают гидрогели с содержанием твердых веществ от 0,5 до 25 мас.% полиакриламида.
Таблица 2
Параметры процесса и характеристики полученного геля (составы с низкой вязкостью (lv) |
| |
lv1 |
lv2 |
lv3 |
lv4 |
lv5 |
lv6 |
lv7d |
lv8e |
| Время промывания (ч) |
a) |
19,5 |
73,75 |
92 |
94,3 |
72,8 |
93,6 |
93,9 |
| Содержание сухого остатка (%) |
2,55 |
2,08 |
2,63 |
2,87 |
2,89 |
3,15 |
3,68 |
3,17 |
| |
2,36 |
2,58 |
2,67 |
2,82 |
2,90 |
3,57 |
3,52 |
| |
|
2,09 |
|
|
|
|
|
| Молярное отношение AM:BISAM |
b) |
976 |
700 |
488 |
366 |
3239 |
488 |
488 |
| Молярное отношение (AM+BISAM): TEMED |
252 |
252 |
253 |
251 |
252 |
249 |
252 |
252 |
| Молярное отношение (AM+BISAM): APS |
298 |
299 |
298 |
298 |
298 |
299 |
298 |
298 |
| Оставшийся мономер (млн-1) |
с) |
89 |
5 |
2,97 |
2 |
5 |
1,4 |
0,97 |
| Упругость G' (Па) |
0,16 |
5,23 |
14,32 |
26,6 |
57,05 |
71,7 |
39,2 |
28,5 |
| 20,1 |
| Вязкость (Па·с) |
0,045 |
0,88 |
2,35 |
4,37 |
9,1 |
11,5 |
6,29 |
4,55 |
| 3,30 |
| Время образования геля (мин) |
Жидкость |
Жидкость с высокой вязкостью |
12 |
2 |
2 |
2 |
2,5 |
2,5 |
| Таблица 2 (продолжение) |
| |
lv9 |
lv10 |
lv11 |
lv12 |
lv13 |
| Время промывания (ч) |
121 |
96,4 |
|
|
|
| Содержание сухого остатка (%) |
2,18 |
(5,10)f |
(10,2)f |
(10,1)f |
(20,2)f |
| Молярное отношение AM:BISAM |
701 |
701 |
488 |
488 |
488 |
| Молярное отношение (AM+BISAM):TEMED |
252 |
252 |
252 |
504 |
2016 |
| Молярное отношение (AM+BISAM):APS |
298 |
298 |
298 |
596 |
2385 |
| Оставшийся мономер (млн-1) |
0,97 |
|
|
|
|
| Упругость G' (Па) |
28,5 |
11,1 |
(911)g |
(1240)g |
(9460)g |
| Вязкость (Па·с) |
4,55 |
1,8 |
(145)g |
(197)g |
(1505)g |
| Время образования геля (мин) |
|
3,17 |
0,00 |
1,21 |
3,5h |
(а) вещество было жидким, так что промывание было разбавлением;
(b) бесконечно большая величина;
(с) так как промывание было не экстракцией, а разбавлением, содержание оставшегося мономера просто снижалось в соответствии с коэффициентом разбавления (с 508 млн-1 до 254 млн-1);
(d) заливку в формы и промывание выполняют с использованием 0,9% водного раствора NaCl;
(e) заливку делают с помощью воды; промывание выполняют с использованием 0,9% водного раствора NaCl;
(f) значения до промывания - промывание обычно уменьшает эти значения на 30-55%;
(g) значения до промывания - промывание обычно уменьшает эти значения на 20-40%;
(h) высокочувствителен к надрезу;
(i) изменения в величинах могут быть обусловлены методами осуществления измерений или расположением в партии, из которой был взят образец.
Таблица 3
Параметры процесса и свойства полученного геля (составы со средней вязкостью (mv)) |
| |
mv1 |
mv2 |
mv3 |
mv4 |
mv5 |
| Время промывания (ч) |
97 |
211,5 |
96 |
94,8 |
90,3 |
| Содержание сухого остатка (%) |
3,14 |
2,49 |
3,25 |
3,29 |
3,22 |
| Молярное отношение AM:BISAM |
310 |
310 |
290 |
289 |
289 |
| Молярное отношение (AM+BISAM):TEMED |
252 |
252 |
252 |
251 |
252 |
| Молярное отношение (AM+BISAM):APS |
299 |
299 |
299 |
299 |
299 |
| Оставшийся мономер (млн-1) |
1,6 |
|
1,5 |
|
|
| Упругость G' (Па) |
108,5 |
|
129 |
133,5 |
|
| Вязкость (Па·с) |
17,4 |
|
20,6 |
21,30 |
|
| Время образования геля (мин) |
2,5 |
2,5 |
2,18 |
|
|
Таблица 4
Параметры процесса и свойства полученного геля (составы с высокой вязкостью (hv)) |
| |
hv1 |
hv2 |
hv3 |
hv4 |
hv5 |
| Время промывания (ч) |
119,5 |
516 |
122 |
95,5 |
116,7 |
| Содержание сухого остатка (%) |
3,47 |
2,5 |
3,56 |
3,83 |
3,42 |
| Молярное отношение AM:BISAM |
260 |
260 |
260 |
260 |
260 |
| Молярное отношение (АМ+BISAM):TEMED |
315 |
315 |
604 |
313 |
314 |
| Молярное отношение (АМ+BISAM):APS |
376 |
376 |
755 |
375 |
376 |
| Оставшийся мономер (млн-1) |
0,2 |
|
|
|
|
| Упругость G' (Па) |
343 |
274 |
|
314,5 |
|
| Вязкость (Па·с) |
54,7 |
43,65 |
|
50,1 |
|
| Время образования геля (мин) |
2,18 |
2,18 |
7,5 |
|
|
Пример 1а (дополнительный)
Экстракция остаточных мономеров промыванием комьев геля WFI-водой («вода для инъекций»)
В таблице 4а ниже приводятся данные по изменению содержания остаточных мономеров в комьях геля при промывании апирогенной «водой для инъекций» в процессе получения пилотной партии геля Aquamid® по изобретению.
Представлены данные для пилотной партии СР199100, за исключением значения в начальный (нулевой) момент времени, которые являются расчетными (содержание сухого твердого вещества, исходя из методики получения) или измеренными (остаточный акриламид) в аналогичных экспериментах СР200794 и СР200801. Отношение гель/вода составляет около 1:10.
| Таблица 4А |
| Время смены воды (часы) |
Содержание сухого твердого вещества в комьях геля, мас.% |
Остаточный акриламид в комьях геля, ч/млн |
| 0 |
5,11 |
1001 |
| 16 |
н/о |
н/о |
| 24 |
н/о |
н/о |
| 40 |
н/о |
н/о |
| 48 |
3,3 |
23,6 |
| 64 |
н/о |
н/о |
| 72 |
2,9 |
4,6 |
| 88 |
н/о |
н/о |
| 92 |
2,7 |
2,3 |
| 140 |
1,4 |
1,1 |
| н/о - не определяли |
Пример 2
Анализ гидрогеля
Характеристики гидрогеля
Промытые гидрогели будут иметь характерные свойства, показанные в табл. 5.
| Таблица 5 |
| Характеристика |
Вариант с низкой вязкостью |
Вариант с высокой вязкостью |
| Плотность сшивания |
0,25% |
0,40% |
| Величина набухания |
80-120% |
50-70% |
| Реологический модуль упругости, G' (Па) |
10-80 Па |
250-700 Па |
Реологическая комплексная вязкость,  * (Па·с) * (Па·с) |
2-10 Па·с |
50-90 Па·с |
| Содержание сухого остатка (%) |
1,6-3% |
3-5% |
| Показатель преломления |
1,335-1,338 |
1,338-1,340 |
Пример 3
Набухание происходит во время процедуры промывания и будет обычно давать профиль набухания, как изображено на фиг.2 и 3.
Пример 4
Способ введения для лечения рефлюкс-эзофагита
Лечение путем инъекций
Делают инъекцию полиакриламидного гидрогеля (с содержанием твердых веществ 2,5 мас.% и апирогенной воды приблизительно 97,5 мас.%) под слизистую оболочку трахеи или связывающих каналов желудка таким образом, чтобы обеспечить увеличенную плотность канала. Лечение проводят с помощью непродолжительной по времени процедуры, предполагающей незначительное количество осложнений.
Пример 5
Способ введения гидрогеля для контурной пластики
Лечение с помощью инъекций
(а) инъекцию геля можно проводить под местной анестезией;
(b) процедура должна осуществляться в стерильных условиях. В гель не должны инъецироваться фармацевтические препараты;
(с) гель, которым заранее заполнены стерильные шприцы на 1 мл с люэровским наконечником, следует вводить подкожно тонкой калиброванной иглой, например, 27 G. Иглы должны быть CE-маркированы;
(d) введите необходимое количество геля подкожно обратным способом, инъецируя гель во время обратного хода иглы. Этикетка для записи данных пациента является частью упаковки, ее можно удалить и прикрепить к истории болезни пациента, чтобы обеспечить отслеживание применения продукта;
(е) после инъекции можно осуществить легкую обработку с целью получить равномерное или требуемое распределение геля. Введенный гель должен образовать устойчивый и мягкий сегмент в соединительной ткани и привести к удовлетворительной с косметической точки зрения внешности на длительный период времени;
(f) возможны дополнительные курсы инъекций для достижения желаемого эффекта.
Лечение путем имплантации
Гель в оболочке из силикона (необязательно в запаянной) помещают под кожу в мягкие ткани пациента.
Пример 6
Способ введения гидрогеля для лечения рефлюкс-эзофагита
Лечение путем инъекций
Делают инъекцию полиакриламидного гидрогеля (с содержанием твердых веществ 2,5 мас.% и апирогенной воды приблизительно 97,5 мас.%) под слизистую оболочку канала между пищеводом и желудком, например, чтобы укрепить сфинктер, таким образом, чтобы обеспечить увеличенную плотность канала. Лечение проводят с помощью непродолжительной по времени процедуры, предполагающей незначительное количество осложнений.
Пример 7
Способ введения гидрогеля для контурной пластики
(а) инъекцию геля можно проводить под местной анестезией;
(b) процедура должна осуществляться в стерильных условиях. В гель не должны инъецироваться фармацевтические препараты;
(с) гель, которым заранее заполнены стерильные шприцы на 1 мл с люэровским наконечником, следует вводить подкожно тонкой калиброванной иглой, например, 27 G. Иглы должны быть CE-маркированы;
(d) введите необходимое количество геля подкожно обратным способом, инъецируя гель во время обратного хода иглы. Этикетка для записи данных пациента является частью упаковки, ее можно удалить и прикрепить к истории болезни пациента, чтобы обеспечить отслеживание применения продукта;
(е) после инъекции можно осуществить легкую обработку с целью получить равномерное или требуемое распределение геля. Введенный гель должен образовать устойчивый и мягкий сегмент в соединительной ткани и привести к удовлетворительной с косметической точки зрения внешности на длительный период времени;
(f) возможны дополнительные курсы инъекций для достижения желаемого эффекта.
Лечение путем имплантации
Гель в оболочке из силикона (необязательно в запаянной) помещают под кожу в мягкие ткани пациента.
Пример 8
Способ введения для наполнения мягких тканей
(а) инъекцию геля можно осуществлять под местной анестезией, но для коррекции морщин и складок местная анестезия не обязательна. При увеличении объема губ рекомендуется проводниковая анестезия;
(b) процедура должна осуществляться в стерильных условиях. В гель не должны инъецироваться фармацевтические препараты;
(с) гель, которым заранее предварительно заполнены стерильные шприцы на 1 мл с люэровским наконечником, следует вводить подкожно тонкой калиброванной иглой, например, 27 G. Иглы должны быть CE-маркированы;
(d) введите необходимое количество геля подкожно обратным способом, инъецируя гель во время обратного хода иглы. Этикетка для записи данных пациента является частью упаковки, ее можно удалить и прикрепить к истории болезни пациента, чтобы обеспечить отслеживание применения продукта;
(е) после инъекции можно осуществить легкую обработку с целью получить равномерное или требуемое распределение геля. Введенный гель должен образовать устойчивый и мягкий сегмент в соединительной ткани и привести к удовлетворительной с косметической точки зрения внешности на длительный период времени;
(f) возможны дополнительные курсы инъекций для достижения желаемого эффекта.
Послеоперационные процедуры
Если появляется отек, можно местно прикладывать лед. Не рекомендуются прямое солнечное облучение, чрезмерный холод или тепло до тех пор, пока не рассосется первоначальная припухлость и не пройдет краснота.
Неприятные явления/Побочные эффекты
Обычно пациенты испытывают боль в течение первых 2-3 послеоперационных дней. У некоторых пациентов возможно появление небольшого отека в течение первых 2-3 дней после инъекции.
Правильная техника инъекций является решающим фактором для окончательного результата лечения, и инъекции должны выполняться персоналом, которому дано право это делать.
Гель стерилизуют (например, паром или обработкой в автоклаве). В случаях, когда упаковка повреждена или вскрыта, стерильность может быть под угрозой, и содержимое упаковок следует выбросить. Повторная стерилизация не рекомендуется.
Пример 9
Опыт применения в клинике для наполнения мягких тканей
(1) Коррекцию лица с помощью геля проводили приблизительно 900 пациентам. Общие косметические результаты были отличные и частота неблагоприятных случаев составляла 0,02% (Kovanskaya V.A.; Scientific conference, 13-16 October 2000).
(2) В общей сложности 150 взрослых подвергались коррекции дефектов лица путем лечения с использованием инъекций геля. Количество геля, которое вводилось инъекциями, составляло от 0,2 до 11 мл.
Предусмотренные графиком лечения визиты пациента имели место в день проверки (за три дня до дня 0), в день 0 (первая инъекция), на 7-й день, на 28-й день, через 3 месяца, через 6 месяцев, на и в конце исследования через 12 месяцев, и при этих посещениях пациентов подвергали объективному обследованию, проводили тесты жизненно важных показателей, тесты на беременность, делали анализ крови и сывороточную реакцию, гематологический и иммунологический тесты, анализ мочи, проводили сопутствующую терапию, анализ побочных эффектов и явлений, рассмотрение косметического результата пациентом и хирургом, а также заполнение опросного листа, в соответствии с графиком в таблице 6.
Результаты
Общая оценка результатов хирургии была от очень хорошей до хорошей, как пациентами, так и хирургами. В некоторых случаях пациенты хотели продолжить лечение и получить дополнительные инъекции. Несколько хирургов добровольно указали в опросном листе, что пациенты были довольны результатом, и что с гелем легко работать и его легко вводить пациенту.
Гель оказался очень хорошо переносимым. Было зарегистрировано только несколько случаев побочного действия, и пациенты сообщали, что имели место неблагоприятные побочные явления - отек и воспаление, - которые через несколько дней рассосались сами по себе.
| Таблица 6 |
| |
Скрининг (не менее 3 дней) |
День 0 (коррекция лица) |
День 7±1 день |
День 28±2 дня |
3 месяца ±7 дней |
6 месяцев ±7 дней |
12 месяцев ±7 дней |
| до операции |
после операции |
| информация/согласие на основе полной информации |
× |
|
|
|
|
|
|
| объективное обследование |
|
× |
× |
× |
× |
× |
× |
| показатели жизненно важных функций |
|
× |
× |
× |
| тест на беременность |
|
× |
|
|
| анализ крови и сывороточная реакция |
взятие проб |
× |
|
|
|
× |
× |
| гематология |
взятие проб |
× |
|
|
|
× |
× |
| иммунология |
взятие проб |
× |
|
|
|
× |
× |
| анализ мочи |
|
× |
|
|
|
× |
× |
| сопутствующее лечение |
|
× |
× |
× |
× |
× |
× |
× |
| побочные эффекты и явления |
|
|
× |
× |
× |
× |
× |
× |
| опросный лист (жалобы) |
|
|
× |
× |
× |
× |
× |
× |
| косметический результат |
|
|
|
|
|
|
|
| пациент |
|
|
|
× |
× |
× |
× |
| хирург |
|
|
|
× |
× |
× |
× |
Пример 10
Способ введения и клинические результаты лечения недержания
Лечение путем инъекций
Полиакриламидный гидрогель (с содержанием сухого остатка 2,5% и апирогенной воды приблизительно 97,5%) инъекцируют под слизистую оболочку мочеиспускательного канала, таким образом, чтобы обеспечить увеличенную плотность мочеиспускательного канала; процедура непродолжительна и дает мало осложнений.
Методика включает инъекцию полиакриламидного геля под слизистую оболочку мочеиспускательного канала женщин, страдающих недержанием. Инъекцию осуществляют через внешнюю поверхность мочеиспускательного канала и по направлению к подслизистой оболочке. Вводят 3 мл гидрогеля в три места, расположенных в одном и том же положении в продольном направлении мочеиспускательного канала. Порции вводят на расстоянии 0,5 см от шейки мочевого пузыря.
Инъекции проводят под местной анестезией, позволяя затем мочевому пузырю наполниться, а пациенту кашлянуть, чтобы сразу же установить, достигнута ли достаточная плотность для удержания мочи. При отсутствии эффекта инъекцию можно повторить, что является обычным при лечении инъекциями.
Обследование женщин показало, что лечение с помощью инъекций является приемлемым по стандартам и условиям Отделения акушерства и гинекологии Копенгагенской Amstsygehus (больницы графства) в Глострупе. Результаты лечения и любые осложнения контролируют проверочными обследованиями, которые проводят каждые три месяца в течение одного года после лечения.
Формула изобретения
1. Биологически устойчивый гидрогель для использования в качестве эндопротеза, состоящий по существу из следующих компонентов: полиакриламида, который включает полимер акриламида, сшитый метилен-бис-акриламидом, в котором акриламид и метилен-бис-акриламид соединены в молярном соотношении от 150:1 до 1000:1, где гидрогель промыт водой или физиологическим раствором так, чтобы в результате содержать около 0,5-3,5 мас.% полиакриламида, считая на общую массу гидрогеля, и воды или водного раствора, где гидрогель содержит менее 50 ч./млн мономеров акриламида и метилен-бис-акриламида, и где модуль упругости гидрогеля составляет примерно от 10 до 700 Па, а его комплексная вязкость составляет примерно от 2 до 90 Па·с.
2. Гидрогель по п.1, где гидрогель содержит, по меньшей мере, 95 мас.% воды или водного раствора, считая на общую массу гидрогеля.
3. Гидрогель по п.1, в котором полиакриламидная главная цепь полимера имеет формулу [С3Н5NO)]X.
4. Гидрогель по п.1, содержащий, по меньшей мере, 1 мас.% полиакриламида, считая на общую массу гидрогеля.
5. Гидрогель по п.1, комплексная вязкость которого составляет примерно от 5 до 80 Па·с.
6. Гидрогель по п.1, модуль упругости которого составляет не менее 20 Па.
7. Гидрогель по п.1, модуль упругости которого составляет примерно от 35 до 480 Па.
8. Гидрогель по п.1, в котором плотность полимерной сетки составляет около 0,2-0,5%.
9. Гидрогель по п.1, в котором акриламид и метилен-бис-акриламид соединены при молярном соотношении от 175:1 до 800:1.
10. Гидрогель по п.1 для использования в качестве имплантируемого эндопротеза.
11. Гидрогель по п.1 для использования в качестве инъецируемого эндопротеза.
12. Гидрогель по п.1, комплексная вязкость которого составляет от 6 до 40 Па·с.
13. Гидрогель по п.1 для использования в качестве имплантируемого эндопротеза, содержащего оболочку на основе силикона.
14. Гидрогель по п.1, который содержит 0,5-3,4 мас.% полиакриламида в расчете на общую массу гидрогеля.
15. Протез для наполнения мягких тканей, где протез является инъецируемым в мягкие ткани, состоящий по существу из полимерного гидрогеля, причем указанный полимерный гидрогель содержит менее 50 ч./млн мономерных звеньев, воду или водный раствор и, по меньшей мере, 0,5 мас.% полиакриламида и менее чем 3,5 мас.% полиакриламида, в расчете на общую массу полимерного гидрогеля, где указанный полиакриламид получен способом, включающим объединение акриламида и метилен-бис-акриламида и промывание водой или физиологическим раствором, так что в результате содержание полиакриламида составляет, по меньшей мере, 0,5 мас.% и менее 3,5 мас.%.
16. Протез по п.15, в котором полимерный гидрогель содержит, по меньшей мере, 0,5 мас.% полиакриламида в расчете на общую массу полимерного гидрогеля.
17. Протез по п.15, в котором полиакриламидная главная цепь полимера имеет формулу [С3Н5NO]X.
18. Протез по п.15, содержащий около 1,9-2,9 мас.% полиакриламида в расчете на общую массу полимерного гидрогеля.
19. Протез по п.15, в котором полимерный гидрогель содержит, по меньшей мере, 95 мас.% воды или водного раствора в расчете на общую массу гидрогеля.
20. Протез по п.15, в котором полимерный гидрогель содержит, по меньшей мере, 1,5 мас.% полиакриламида в расчете на общую массу полимерного гидрогеля.
21. Протез по п.15, комплексная вязкость которого составляет примерно от 2 до 100 Па·с.
22. Протез по п.15 для, по меньшей мере, одного из следующих видов хирургии: косметической или реконструктивной хирургии лица, контурной пластики или наполнения и реконструктивной хирургии губ.
23. Протез по п.22 для косметической или реконструктивной хирургии лица, комплексная вязкость которого составляет примерно от 2 до 20 Па·с.
24. Протез по п.22 для контурной пластики, комплексная вязкость которого составляет примерно от 5 до 50 Па·с.
25. Протез по п.22 для наполнения или реконструктивной хирургии губ, комплексная вязкость которого составляет примерно от 2 до 10 Па·с.
26. Протез по п.15 для использования при коррекции дефектов лица, возникших вследствие, по меньшей мере, одной из следующих причин: старения, угрей, травмы, хирургического вмешательства, инфекции или врожденной деформации.
27. Протез по п.26, где коррекцию дефектов лица выбирают из группы, состоящей из коррекции скуловых костей, коррекции носогубных складок, коррекции хмурых гримас над переносицей, коррекции вдавленной формы рта, коррекции подбородка, коррекции размера или формы губ и коррекции других недостатков мягких тканей лица.
28. Протез по п.15, в котором вода является апирогенной.
29. Протез по п.15, в котором полимерный гидрогель содержит менее 20 ч./млн мономерных звеньев.
30. Протез по п.15, в котором модуль упругости полимерного гидрогеля составляет не менее 10 Па.
31. Протез по п.15, в котором модуль упругости полимерного гидрогеля составляет примерно от 10 до 700 Па.
32. Протез по п.15, в котором модуль упругости полимерного гидрогеля составляет примерно от 35 до 480 Па.
33. Применение гидрогеля, который можно получить в несколько стадий, включающих объединение акриламида и метилен-бис-акриламида, инициирование радикальной полимеризации и промывание водой или физиологическим раствором так, что в результате содержание полиакриламида составляет, по меньшей мере, 0,5 мас.% и содержание полимера составляет менее 3,5 мас.%, в расчете на общую массу гидрогеля, для получения эндопротеза для наполнения мягких тканей путем инъекции млекопитающим, причем комплексная вязкость эндопротеза составляет 2-90 Па·с и модуль упругости составляет от 35 до 480 Па.
34. Применение по п.33 для получения эндопротеза для коррекции косметического или функционального дефекта лица путем инъекции, причем комплексная вязкость эндопротеза составляет 2-90 Па·с и модуль упругости составляет от 35 до 480 Па.
35. Применение по п.33 для получения эндопротеза для коррекции косметического или функционального дефекта губ путем инъекции, причем комплексная вязкость эндопротеза составляет 2-90 Па·с и модуль упругости составляет от 35 до 480 Па.
36. Применение по п.33 для получения эндопротеза для контурной пластики.
37. Применение по п.33, где эндопротез представляет собой протез для коррекции дефектов лица, возникающих вследствие старения, угрей, травмы, хирургического вмешательства или врожденной деформации.
38. Применение по п.33, где эндопротез представляет собой протез для коррекции скуловых костей, носогубных складок, коррекции хмурых гримас над переносицей, вдавленной формы рта или подбородка, для лечения морщин, складок, асимметрии лица или для изменения формы носа.
39. Применение по п.35, где эндопротез представляет собой протез для коррекции размера или формы губ.
40. Применение по любому из пп.33-39, где эндопротез представляет собой протез для коррекции эстетических дефектов, вызванных врожденными, травматическими или возрастными изменениями.
41. Применение по любому из пп.33-40, где объединение акриламида и метилен-бис-акриламида проводят при их молярном соотношении 150:1-1000:1.
42. Применение по любому из пп.33-41, где гидрогель содержит менее 3,5 мас.% полиакриламида, в расчете на общую массу гидрогеля, сшитого метилен-бис-акриламидом, и, по меньшей мере, 95% апирогенной воды или физиологического раствора.
43. Применение по любому из пп.33-41, где гидрогель содержит, по меньшей мере, 1 мас.% полиакриламида, в расчете на общую массу гидрогеля.
44. Применение по любому из пп.33-41, где полиакриламидная главная цепь полимера имеет формулу [С3Н5NO]X.
45. Применение по любому из пп.33-41, где комплексная вязкость гидрогеля составляет от 6 до 60 Па·с.
46. Применение по любому из пп.33-45, где концентрация акриламида и N,N'-метилен-бис-акриламида в гидрогеле составляет менее 50 ч./млн.
47. Применение по п.41, где молярное соотношение составляет от 225:1 до 600:1.
48. Способ наполнения мягких тканей, включающий инъекцию гидрогеля, который получают в несколько стадий, включающих объединение акриламида и метилен-бис-акриламида, инициирование радикальной полимеризации и промывание гидрогеля апирогенной водой или физиологическим раствором так, что в результате содержание полиакриламида составляет, по меньшей мере, 0,5 мас.% и содержание полимера составляет менее 3,5 мас.%, в расчете на общую массу гидрогеля; причем указанный полимерный гидрогель содержит менее 50 ч./млн мономерных звеньев, его модуль упругости составляет примерно от 10 до 700 Па, а комплексная вязкость гидрогеля - примерно от 2 до 90 Па·с.
49. Применение эндопротеза, который включает в себя гидрогель, для лечения недержания мочи или анального недержания, причем указанный гидрогель содержит примерно от 0,5 до 25 мас.% полимера, полученного способом, включающим объединение акриламида и метилен-бис-акриламида, промывание гидрогеля апирогенной водой или физиологическим раствором, где указанный гидрогель содержит менее 50 ч./млн мономерных звеньев, и где комплексная вязкость указанного гидрогеля составляет примерно от 2 до 90 Па·с, а модуль упругости составляет примерно от 1 до 200 Па.
50. Применение по п.49, где для лечения недержания мочи эндопротез вводят в уретру или шейку мочевого пузыря.
51. Применение по п.49, где полимер получают путем объединения акриламида и метилен-бис-акриламида при молярном соотношении 150:1-1000:1.
52. Применение по п.49, где гидрогель содержит менее 15 мас.% полимера в расчете на общую массу гидрогеля.
53. Применение по п.49, где гидрогель содержит по меньшей мере 1 мас.% полимера в расчете на общую массу гидрогеля.
54. Применение по п.49, где главная цепь полимера имеет формулу [С3Н5NO]X.
55. Применение по п.49, где комплексная вязкость гидрогеля составляет примерно 2-40 Па·с.
56. Применение по п.49, где гидрогель содержит, по меньшей мере, 80 мас.% воды или водного раствора.
57. Применение по п.49, где введение включает инъекцию гидрогеля.
58. Применение по п.49, где инъецирование гидрогеля включает инъекции в положениях, соответствующих положениям 10, 2 и 6 ч на циферблате часов, вокруг оси поперечного сечения уретры для лечения недержания мочи, или инъекции в положениях, соответствующих положениям 10, 2 и 6 ч на циферблате часов, вокруг оси поперечного сечения толстой кишки или прямой кишки.
59. Применение по п.49, где гидрогель содержит менее 10 мас.% полимера в расчете на общую массу гидрогеля.
60. Применение по п.49, где гидрогель содержит менее 7,5 мас.% полимера в расчете на общую массу гидрогеля.
61. Применение по п.49, где гидрогель содержит менее 5 мас.% полимера в расчете на общую массу гидрогеля.
62. Применение по п.49, где гидрогель содержит менее 3,5 мас.% полимера в расчете на общую массу гидрогеля.
63. Применение по п.49, где гидрогель содержит, по меньшей мере, 1,5 мас.% полимера в расчете на общую массу гидрогеля.
64. Применение по п.49, где комплексная вязкость гидрогеля составляет примерно от 2 до 50 Па·с.
65. Применение по п.49, где комплексная вязкость гидрогеля составляет примерно от 2 до 30 Па·с.
66. Применение по п.49, где сшивающий агент представляет собой метилен-бис-акриламид.
67. Применение по п.49, где полимер состоит по существу из сшитого полиакриламида.
68. Применение по п.49, где полимер состоит по существу из полимера, полученного полимеризацией акриламида в присутствии сшивающего агента.
69. Применение по п.33, где полиакриламидная главная цепь полимера имеет формулу [С3Н5NO]X.
70. Применение гидрогеля, содержащего 0,5-25 мас.% полиакриламида в расчете на общую массу гидрогеля, для получения протеза для лечения или профилактики недержания мочи.
71. Применение гидрогеля, содержащего 0,5-25 мас.% полиакриламида в расчете на общую массу гидрогеля, для получения протеза для лечения или профилактики анального недержания.
72. Применение гидрогеля, получаемого в несколько стадий, включающих объединение акриламида и метилен-бис-акриламида в таких количествах, что содержание полимера составляет примерно от 0,5 до 25 мас.% в расчете на общую массу гидрогеля, инициирование радикальной полимеризации, и промывание апирогенной водой или физиологическим раствором, для получения протеза для лечения или профилактики недержания мочи.
73. Применение гидрогеля, получаемого в несколько стадий, включающих объединение акриламида и метилен-бис-акриламида в таких количествах, что содержание полимера составляет примерно от 0,5 до 25 мас.% в расчете на общую массу гидрогеля, инициирование радикальной полимеризации, и промывание апирогенной водой или физиологическим раствором, для получения протеза для лечения или профилактики анального недержания.
74. Применение гидрогеля, получаемого в несколько стадий, включающих объединение акриламида и метилен-бис-акриламида в таких количествах, что содержание полимера составляет примерно от 0,5 до 25 мас.% в расчете на общую массу гидрогеля, инициирование радикальной полимеризации, и промывание апирогенной водой или физиологическим раствором, для получения протеза для лечения или профилактики пузырно-мочеточникового рефлюкса у млекопитающих.
75. Применение по любому из пп.70-74, где полиакриламидная главная цепь полимера имеет формулу [C3H5NO]X.
76. Применение по любому из пп.70-75, где модуль комплексной вязкости гидрогеля составляет примерно от 2 до 50 Па·с, например примерно от 2 до 40 Па·с, предпочтительно примерно от 2 до 30 Па·с, более предпочтительно примерно от 2 до 20 Па·с.
77. Применение по любому из пп.70-76, где модуль упругости гидрогеля составляет примерно от 1 до 200 Па, например примерно от 2 до 175 Па, обычно примерно от 5 до 150 Па, более предпочтительно примерно от 10 до 100 Па.
|