
СПИСОК ПАТЕНТОВ С УПОМИНАНИЕМ ГИАЛУРОНОВОЙ КИСЛОТЫ
-
- 2017751 Способ получения гиалурона
- 2192150 БАД для профилактики йодной недостаточности
- 2112542 Препарат для лечения патологий соединительных тканей
- 2225206 Препарат для лечения рака молочной железы
- 2299733 Лечение опорно-двигательного аппарата
- 2299732 Способ лечения глаукомы
- 2299726 Противоинфекционная губная помада
- 2299725 Косметическое средство для ухода за кожей
- 2198878 Ароматическое соединение
- 2198702 Способ подготовки трофических язв к аутодермапластике
- 2198653 Вагинальные суппозитории
- 2197946 Композиция для ухода за волосами
- 2197923 Фармацевтическая композиция для лечения отеков роговицы
- 2298410 Биотрансплантант и способ лечения ревматических и аутоиммунных заболеваний
- 2197501 Фотоотверженный гель на основе сшитой гиалуроновой кислоты
- 2197228 Твердые лекарственные формы
- 2197222 Водная компазиция для ухода за волосами, лица и тела
- 2297425 Полипептиды
- 2297240 Композиция с гиалуроновой кислотой
- 2297230 Фармацевтическая компазиция с ксантоновой смолой
- 2196588 Глазные капли
- 2195955 Применение биологически активных веществ
- 2195926 Дерматологические композиции
- 2295954 Микрочастицы для доставки нуклеиновых кислот
- 2295951 Косметика для ухода за кожей лица и век
- 2195262 Фармакологическое средство на основе гиалуроновой кислоты
- 2194512 Способ профилактики и коррекции процесса старения кожи
- 2194478 Лечение экземы
- 2294716 Расширяемый стент
- 2194055 Сшитые сополимеры
- 2099350 Ассоциаты депротонированной гиалуроновой кислоты
- 2293557 Средство для лечения кожи и слизистых
- 2292878 Приготовление микроцастиц, содержащих метопропол
- 2292746 БАД
- 2192256 Защита кишечника
- 2191782 Получение модифицированной гиалуроновой кислоты
- 2292219 Паратиреоидный гормон человека
- 2291686 Микроцастицы
- 2191000 Косметическая маска
- 2290921 Фармацевтические и косметические средства против старения кожи
- 2290900 Модифицированный биоматериал для использования в офтальмологии
- 2290899 Получение биоматерьяла
- 2290397 Новые инданилиденовые соединения
- 2290186 Лечение сирингомиелии
- 2288702 Иррингационный раствор для офтальмологии
- 2288699 Гель для лечения стоматологических заболеваний
- 2188011 Активирующая остеогенез фармацевтическая композиция
- 2187327 Средство с антисептиком
- 2187325 Средство с радиопротекторным действием
- 2287330 Композиции миноксидила
- 2186786 Способ получения гиалуроновой кислоты
- 2186593 Лечение раненого процесса кожи
- 2286801 Очищение воды
- 2286781 Лечение ожогов пищевода у детей
- 2286764 Средство лечения воспалений полости рта
- 2185840 Лечение инфекционных заболеваний
- 2286151 Альфа-2-Дельта-Лиганда
- 2185149 Ранозаживляющий гель
- 2285527 Лечение ИЛ-6 заболеваний
- 2184448 Раствор хранения роговицы, включающий гиалуроновую кислоту
- 2090179 Крем для кожи
- 2183961 Способ лечения кожи
- 2284331 Соли алифотических аминов
- 2284187 Производные амида
- 2089191 Снизить внутрение давление
- 2283320 Получение гликозаминогликанов
- 2283129 Лечение опухолей
- 2283098 Косметические средства с Q
- 2182574 Ароматические соединения
- 2088257 Средство с гипохолестеролемическим действием
- 2088218 Состав для гигиенических салфеток
- 2088206 Способ получения препарата, создающего исскуственный загар
- 2282462 Противомикробные средства
- 2182008 Интровагинальная компазиция
- 2181999 Препарат с отсроченным высвобождением
- 2181998 Новые композиции липидов
- 2181995 Лечение болевого синдрома
- 2181295 Вирионная вакцина
- 2087144 Витамин Е
- 2379336 Способ стирки
- 2379052 Вакцинация
- 2180855Композиция в виде ионного комплекса
- 2379025 Противоинфекционный гель
- 2180825 Лечение травм роговицы
- 2281082 Способ коррекции эстетических и возрастных проблем кожи
- 2180576 Биоактивная добавка для косметических средств
- 2280459 Средство для изменения скорости роста или репродукции клеток
- 2179981 Соли переходного металла
- 2378010 Жидкие вакцины
- 2378008 Комбинированные вакцины
- 2378007 Анаболическое средство
- 2377973 Растительные экстракты
- 2280041 Способ получения водорастворимых комплексов гиалурил
- 2280038 Биополимеры
- 2323733 Йодный обмен
- 2377260 Гель
- 2178693 Противовирусное средство на основе гиалуроновой кислоты
- 2178692 Облегчающие зуд косметическое средство
- 2377022 Гемостатические спреи
- 2376982 Увлажняющая сыворотка для лица
- 2376974 Трансдермальный гель для лица
- 2362784 Гипо-и гиперацетилированные менингокковые капсульные сахариды
- 2177789 Устройство для доставки лекарства к шейке матки
- 2277954 Крем для лица омолаживающий
- 2376378 Способ получения метионина
- 2177332 Биоматериал для предотвращения послеоперационных спаек, с производной гиалуроновой кислотой
- 2177310 Способ получения таблеток
- 2376011 Средство для позвоночника
- 2277410 Косметическое средство
- 2323748 Медицинская повязка
- 2276998 Гидрогелевые композиции
- 2082416 Способ получения препарата с коллагенном из животного сырья
- 2375081 Адсорбирующее изделие
- 2375049 Охлаждающий пластырь
- 2346049 Способ получения гиалурона
- 2275913 Фармацевтические средства
- 2174985 Полисахарид с антиоксидантом
- 2373957 Носитель для лекарственных средств и биологически активных веществ
- 2373941 Способ коррекции возрастных и патологических изменений кожных покров
- 2174845 Композиции и способы доставки генетического материала
- 2174830 Средство для укрепления волос
- 2373769 Синбиотическая композиция
- 2274472 Лечение апорно-двигательного аппарата и болевых синдромов
- 2372929 Профилактическая композиция на основе веществ фенольной природы в липосомной форме
- 2173563 Способ нанесения на поверхность предметов покрытия на основе гиалуроновой кислоты, её производных и полусинтетических полимеров
- 2079304 фармацевтическая композиция, обладающая иммуносупрессорной и антимикробной активностью
- 2273645 Полипептид ожирения
- 2173154 Фракция кератансульфатолигосахаридов и содержащий ее фармацевтический препарат
- 2173136 Грязная мазь
- 2173128 Способ хирургического лечения центральных разрывов сечатки
- 2078561 Косметическое средство предотвращающее старение кожи
- 2172490 Способ прогнозирования воспалительных заболеваний молочной железы при эндопластике
- 2272645 Способ лечения ЦМВ-Инфекции у детей раннего возроста
- 2272636 Фармацевтическая композиция для местного лечения воспаления
- 2272635 Фармацевтически активная субстанция для офтальмологии
- 2272599 Биоматерьял для стабилизации прогрессирующей миопии "Коллаплант"
- 2172168 Средство для заживления ран на основе гиалуроновой кислоты
- 2371172 Фармацевтическая композиция для лечения нервной системы на основе стефаглабрина
- 2171470 Способ прогнозирования послеоперационной трансформации доброкачественных опухолей нервной системы
- 2077317 Состав для ванн
- 2271213 Комбинированные композиции, содержащие экстракты из растений и морских животных
- 2076872 Способ получения окрашенной гиалуроновой кислоты
- 2076671 Раствор для защиты роговицы
- 2370281 Конъюгаты гидроксиалкилкрахмал
- 2370275 Способ лечения (коррекции) косметических и возрастных дефектов кожи
- 2370258 Фармацевтическая композиция для парентальной доставки в форме лиофилизата
- 2270023 Способ экстракции и очистки протеогликана хрящего типа (варианты)
- 2369408 Гемостатическая композиция, включающая гиалуроновую кислоту
- 2369387 Фармацевтическая композиция для лечения нервной системы
- 2369379 Нетаблитированные жевательные формы для индивидуального введения
- 2169136 Производное коричной кислоты
- 70792 Медицинский аппликатор
- 20741717 Способ стабилизации аскорбиновой кислоты
- 2074712 Способ получения препарата, препятствующего преждевременной эякуляции
- 2367954 Способ прогнозирования развития кожной патологии у женщин с синдромом склерополикистозных яичников (СПКЯ)
- 2268075 Устройство для электрокинетической доставки
- 2268052 Средство для лечения воспалительных и дегенеративных заболеваний суставов
- 2167649 Способ получения твердой дисперсии умеренного водорастворимого лекарственного вещества
- 2167647 Гель для бритья
- 2073520 Лечение урологических инфекций
- 2367476 Биопластический материал
- 2367475 Мембрана для использования при направленной регенерации тканей
- 2367469 Фармацевтическая композиция на основе лизоамидазы
- 2367456 Фармацевтическая композиция обладающая антибактериальным и некролитическим действием
- 2367455 Фармацевтическая композиция обладающая некролитическим и антибактериальным действием
- 2267324 Применение антиадгезивных углеводов, препарат для уменьшения и /или блокирования адгезии патогенных веществ
- 2166934 Композиции включающие биологический агент
- 2166510 Псевдодипептиды
- 2366460 Композиции, имеющие высокую противовирусную и антибактериальную активность
- 2360901 Производные феноксиуксусной кислоты
- 2165749 Способ восстановления эндотелия роговицы
- 2265441 Способ укрепления склеры
- 2365382 Композиции и способы для регуляции развития сосудов
- 2070879 Соли гликозаминогликанов
- 2164914 Циклические и гетероциклические N - замещенные - иминогидроксамовые карбоновые кислоты
- 2264627 Хламидийный конъюктивит
- 2364399 Фармацевтический препарат на основе стефаглабрина
- 2264230 Препарат с замедленным высвобождением активного вещества
- 2363497 Фармацевтические композиции
- 2363496 Способ увеличения объема мягких тканей
- 2363473 Способ антифлогистической активации в эксперементе
- 2363461 Фармацевтический препарат на основе сигетина
- 2363459 Средства для введения в роговицу глаз для предотвращения офтальмологических нарушений
- 2363448 Фармацевтические композиции
- 2163123 Глазные капли
- 2162687 Усовершенствованнная лекарственная форма индуктора интерферана
- 2162343 Биосовместимый полимерный материал и способ его получения
- 2162327 Лечение рака
- 2067841 Способ получения ароматизатора
- 2161478 Способ консервированого лечения гонартроза
- 2361617 Вольфрамовые частицы в качестве рентгеноконтрастных веществ
- 2361552 Способы и устройства для дренирования жидкостей и понижения внутриглазного давления
- 2066996 Способ изготовления пленочного материала для офтальмохирургии
- 2361417 Корм с глюкозамином и экстрактом ивы для профилактики артроза у животных
- 2161002 Пищевой общеукрепляющий лечебно-профилактический продукт из хрящевой ткани акул
- 2360928 Комплексная матрица для медико-биологического применения
- 2160574 Способ лечения глаукомы
- 2360688 Способ лечения повреждений переферических нервов
- 2360670 Фармацевтическая композиция при климактерических расстройствах
- 2360646 Эндолюминальный протез
- 2260445 Способ усовершенствования транспортировки через легко прспосабливаемый полупроницаемый барьер
- 2260007 Производные амида
- 2359975 Способ получения модифицированных арабиногалактанов
- 2359974 Антигенные Пептиды
- 2159775 Псевдопептидный продукт
- 2259833 Фармацевтическая композиция для лечения роговицы глаза
- 2259816 Ранозаживляющее средство
- 2259815 Способ коррекции возрастных изменений, связанных с процессами старения кожи
- 2359706 Способ сохранения офтальмологических растворов
- 2359704 Антисептическое средство
- 2359662 Микрокапсулы
- 2159253 Катионные полимеры
- 2159111 Средство для ухода за кожей лица
- 2159105 Композиция для защиты кожи от опасных химических веществ Получение
- 2158593 Биосовместимый водный раствор
- 2358728 Способ лечения и предупреждения потери костной ткани
- 2258517 Способ хирургического лечения травмотических повреждений селезенки пленкой на основе гиалуроновой кислоты
- 2357968 Кристалические формы производной имидазола
- 2357957 Ингибиторы P38 и их применение
- 2157647 Пищевая добавка и ее получение
- 2357758 Препараты для чрескожной и чересслизистой добавки
- 2063244 Способ стабилизации растворов
- 2063140 Способ получения препарата для консервирования мяса
- 2157381 Способ получения гиалуроновой кислоты
- 2257198 Композиции микроцастиц
- 2356909 Белковый комплекс
- 2356570 Косметическая композиция
- 2256434 Способ закрытия перфорации барабанной перепонки
- 2356520 Способ лечения постконтузионного повреждения сечатки глаза
- 2156133 Гель
- 2255945 Полимерная композиция
- 2355761 Средства повторной дифференцировки
- 2061043 Способ повышения устойчивости урокиназы к нагреванию
- 2061005 Способ получения красителей для гистологических исследований
- 2355420 Зубная паста
- 2355385 Композиции пролонгированного действия с контролируемым высвобождением
- 2355240 Способ получения пищевого препарата хондропротекторного действия
- 2155057 Пихтово репейный бальзам
- 2354409 Способ производства высвобождающих лекарственные средчтва медицинских устройств
- 2254145 Раневое покрытие на основе коллаген-хитозанового комплекса
- 2254133 Лечение и профилактика ВИЧ-инфекции у человека
- 2253439 Фармацевтическая композиция для защиты и улучшения оптических свойств роговици при проведении эндовитреальных вмешательств
- 2253437 Способ омоложения кожи
- 2153352 Фармацевтическая композиция обладающая ранозаживляющим и противовоспалительным действием
- 2353354 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2252787 Способ получения искусственной матрицы кожи
- 2252767 Способ нормализации иммунобиохимического гомеостаза коров в предродовом и послеродовом периодах
- 2352583 Фармацевтическая композиция содержащая Fc-область иммуноглобулина в качестве носителя
- 2152403 Модифицированные полисахариды
- 2352356 Иммуногенная композиция
- 2352342 Исскусственный физиологический солевый раствор Способ его получения
- 2352330 Фармацевтический препарат на основе низкомолекулярного индуктора интерферона
- 2352323 Фармацевтический препарат с модифицированным высвобождением
- 2152027 Способ подготовки ткани мозга для определения гликозаминогликанов
- 2251842 Интектицидный состав для борьбы с личинками оводов
- 2151580 Способ активации пролиферации эндотелия роговицы
- 2351648 Дифференцировка стромальных клеток, полученных из жировой ткани, в эндокринные клетки поджелудочной железы и их использование
- 2351595 N - гидроксиформамидные соединения в качестве ингибиторов металлопротеина
- 2251411 Косметическое средство в лиофилизированной фармацевтической форме
- 2251405 Косметика...ее композиции для косметических препаратов
- 2251367 Средство со сшитой гиалуроновой кислотой для наращивания тканей
- 2351359 Косметика для профилактики и лечения избыточной массы тела
- 2351322 Препарат на основе низкомолекулярного индуктора интерферона
- 2351153 Диета при остеортрите собак
- 2350958 Способ определения групповой принадлежности синовальной жидкости
- 2350625 Производные гиалуроновой кислоты с пониженной биодеградируемостью
- 2150266 Крем после бритья
- 2350354 Фармацевтическое средство содержащие антагонист и фактор некроза
- 2350340 Способ коррекции процессов регенерации
- 2350309 Способ лечения избыточной массы тела с помощью рефлексотерапии
- 2250047 Профилактический продукт из хрящевой ткани гидробионтов
- 2249467 Медицинский матерьял и изделия на его основе
- 2055079 Способ получения препарата гиалуроновой кислоты
- 2349599 Биоадгезив мидии
- 2054903 Способ лечения коллагеноза у бычков на откорме
- 2249210 Способ прогнозирования предрасположенности к развитию и тяжести течения деформирующего остеоартроза коленного сустава у взрослых
- 2349339 Средство для соединительной ткани
- 2148988 Человеческий интерферона
- 2148399 Лечение атеросклероза
- 2148396 Способ определения активного вещества в дифильных мазевых основах
- 2148375 Способ диагностики близорукости
- 2348415 Способ противоспаечной терапии после хирургического вмешательства
- 2348400 Препарат на основе низкомолекулярного индуктора интерферона
- 2348386 Способ непроникающего хирургического лечения первичной открытоугольной глаукомы
- 2248213 Лечение Галактозидальной А недостаточности
- 2347586 Микрофлюидизированные эмульсии типа "масло в воде" и вакцинные средства
- 2147243 Контрастное средство
- 2146526 Лечебный препарат дисбактериоза и урогенитальных инфекций
- 2146148 Терапевтическое применение фактора роста кератиноцитов (ФРК)
- 2146139 Способ повышения активности макрофагов и комбинации для его осуществления
- 2346277 Способ диагностики специфического синовита
- 2345793 Ультразвуковые контрастные вещества и их получение
- 2345782 Терапевтические комбинации на основе PORIFERA для лечения и предотвращения кожных заболеваний
- 2245131 Способ коррекции косметических недостатков кожи
- 2245130 Способ активации восстановительных процессов в коже
- 2144833 Хондроитиназа
- 2344809 Получение твердых дозированных форм с использованием сшитого нетермопластичного носителя
- 2244540 Косметический гель для ухода за кожей лица
- 2244536 Способ лечения дегенеративно-дистрофических заболеваний тазобедренного сустава
- 2344167 Хмелевый экстракт
- 2143884 Агент регулирования дифференциации клеток кожи, культурная среда для клеток или тканей и способ регулирования дифференциации клеток кожи
- 2343932 Способ получения обладающих пониженной растворимостью в воде пленночных материалов
- 2343903 Устройство доставки лекарств для контролируемого введения препаратов
- 2048817 Способ получения материала для лечения ожогов и гнойно - некронических ран
- 2048803 Гидратантный крем
- 2242974 Средства и способы лечения воспалительных заболнваний
- 2142816 Способ получения антигерпетической вакцины
- 2342923 Средство для обработки рук с увлажняющим эффектом
- 2142781 Косметика для макияжа ресниц и бровей и агент ингирирующий рост микроорганизмов в косметических средствах
- 2242251 Трансплантируемые стенты с биоактивными покрытиями
- 2142257 Способ обработки глазных имплантантов и контакных линз
- 2342389 Мононатриевая соль
- 2342107 Способ устранения западения верхнего века при анофтальме
- 2141828 Средство, пролонгирующее эффективность чесночного порошка
- 2241489 Косметическое средство матриксных протеинов для залечивания ран
- 2241443 Средство для лечения герпеса
- 2241414 Способ получения протезов кровеносных сосудов
- 2341539 Гидрогель
- 2141324 Регулятор скорости воздействия препарата для инъекций
- 2141312 Косметическое средство для ухода за кожей лица
- 2341296 Средства и способы покрытия медицинских имплантантов
- 2341272 Средство для неспецифической иммунотерапии
- 2341266 Стенты с нанесенным покрытием содержащим N - (5-(4-(4-
- 2341257 Иммуномодулирующее средство
- 2341255 Средство для лечения климактерических расстройств
- 2240821 Способ лечения урологических инфекций
- 2140786 Способ лечения лишая
- 2140243 Способ хирургического лечения диабетической ретинопатии и отслоек сечатной оболочки
- 2240140 Медицинская многослойная повязка и изделия на ее основе
- 2240135 Культура клеток, содержащая клетки - предшественники остеонегеза, имплантант на ее основе и его использование для восстановления целостности кости
- 2240123 Экзогенные биологически активные коньюгирующие вещества
- 2139886 Фотоотвержаемое производное гликозаминогликата, сшитое производное гликозаминогликата и способы их получения, способ предотвращения клеточной и тканевой адгезии
- 2139729 Вакцина. Способ стимулирования иммунной системы
- 2339386 Средство обладающее радио - и химиозащитным действием
- 2339369 Лечение офтальмологических нарушений с использованием мочевины и ее производных
- 2139041 Гидратантный регенерирующий крем и способ его получения
- 2139039 Косметический суперкрем для ухода за кожей
- 2139017 Способ получения боисовместимого материала
- 2138503 Производные камптотецина, способы их получения, уникальное средство
- 2338556 Средство содержащие антагонист Р2Х - рецептора и нестероидное противоспалительное лекарственное средство
- 2338514 Косметическое средство для профилактики старения кожи
- 2138297 Медицинские устройства, подверженные вызываемому разложению
- 2138295 Покрытие для ран
- 2337906 Ингибиторы цитозольной фосфолипазы А2 Применение физиологически допустимого корпускулярного ферримагнитного или ферромагнитного материала. Способ формирования магнитометрического изображения
- 2137501 Устройство формирования изображения
- 2137477 Способ лечения заболеваний характеризующихся аутоиммунной агрессией
- 2137467 Крем для кожи лица и тела
- 2137449 Способ коррекции дефектов преломления в глазу млекопитающего
- 2137402 Пищевая Добавка БАД
- 2336899 Способ стимуляции миелопоэза
- 2336862 Способ получения раствора для лечения роговицы
- 2336830 Способ восстановления костных структур челюсти
- 2136696 Новый полипептид и средство против ВИЧ - Инфекции
- 2336092 Биоадгезивное средство, по существу свободное от воды
- 2336089 Средство и способ лечения заболеваний периодонтальных и пульпы
- 2336074 Средства и способы лечения заднего сегмента глаза
- 2235548 Ранозаживляющее средство
- 2135186 Способ лечения рефлекторных синдромов при остеохондрозе
- 2234945 Стабилизатор водного раствора и водосодержащего сырья
- 2334762 Растворимая ассоциативная карбоксиметилцеллюлоза
- 2234514 Макропористые хитозановые гранулы и способ их получения. Способ культивирования клеток
- 2133615 Средство для лечения неврологических заболеваний
- 2233164 Способ профилактики развития послеоперационных спаек брюшной полости
- 2133127 Неткатный материал, способ его получения и способ лечения
- 2333223 Альдегидные производные сиаловой кислоты и средства на их основе
- 2333007 Полипептидные вакцины для широкой защиты против рядов поколений менингококов с повышенной вирулентностью
- 2332985 Дозированные формы анестезирующих средств с длительным высвобождением для обезболивания
- 2132677 Косметическая маска
- 38603 Пленочный аппликатор
- 2232594 Средство содержащие ингибирующие остеокластогенез фактор и полисахарид
- 2332238 Средство для прокладок, раневых повязок и других изделий, контактирующих с кожей
- 2331668 Стромальные клетки, получение из жировой ткани, для заживления дефектов роговицы и внутриглазных дефектов и их использование
- 2331438 Альфа - 2 - Дельта Лигант для лечения симптомов нижних мочевыводящих путей
- 2331411Электропряденые аморфные фармоцевтические средства
- 2331367 Способ профилактики образования спаек и их рецидива
- 2130767 Масло в воде для получения косметических и дерматологических средств, способ косметической обработки
- 2230752 Поперечносшитые гиалуроновые кислоты и их применение в медицине
- 2230558 Способ восстановления и сохранения здоровья скмьи
- 2230550 Средства длительного высвобождения, способ их получения и применения
- 2230458 Поддержания здоровья суставов
- 2330290 Способ определения состояния метаболических процессов в ткани суставного хряща
- 2230073 Способ поперечного сшивания карбоксилированных полисахаридов
- 2329059 Способ лечения полипозного риносинусита
- 2329037 Комбинированная терапия для лечения иммуновоспалительных заболеваний
- 2128666 Гиалуроновая кислота и ее соли, способ очистки гиалуроновой кислоты, способ получения гиалуроновой кислоты. Фармацевтический препарат с гиалуроновой кислотой и средства с гиалуроновой кислотой используемые в офтальмологии
- 2328740 Способ экспресс - оценки действия зубных паст
- 2128502 Косметический гель
- 2328272 Суппозитории индуктора интерферона
- 2328268 Косметика содержащая амфолитный сополимер
- 2128057 Композиционная мембрана, способ ее получения и способ направленной регенерации тканей с ее применением
- 2128055 Средство замедленного освобождения и способ его получения
- 2128049 Свечи
- 2227743 Полипептидные варианты с повышенной гепаринсвязывающей способностью
- 2326893 Ковалентное и нековалентное сшивание гидрофильных полимеров
- 2326697 Новый перевязочный материал для быстрого заживления раневой поверхности кожи
- 2126264 Фармацевтическое средство с гиалуроновой кислотой
- 2326137 Способ получения содержащих альгинат пористых формованных изделий
- 2325902 Способ выделения гликозаминогликанов из минерализованной соединительной ткани
- 2225195 Репелленты против насекомых
- 2325193 Сосудистый стент
- 2325184 Улучшенные везикулы наружной мембраны бактерий
- 2325153 Многокомпонентная фармацевтическая дозированная форма
- 2325152 Удерживаемая в желудке система регулируемой доставки лекарственного средства
- 2029955 Способ предоперационного определения помутнения задней капсулы хрусталика при экстракции катаракты
- 2324688 Производные бисбензизоселеназолонила с противоопухолевым, противовоспалительным и антитромбоническим действием
- 2323017 Устройство и способ контролируемый доставки активных веществ в кожу
- 2323011 Содержащий Коллаген I и Коллаген II способный к рассасыванию внеклеточный матрикс, предназначенный для реконструирования хряща
- 2322955 Способ изготовления имплантанта для пластики дефектов хрящевой ткани
- 2322454 Антитело против CCR5
- 2322263 Система продолжительного высвобождения растворимого лекарственного средства
- 2221561 Витамин Е и его сложные эфиры
- 2321634 Гены участвующие в метаболизме углерода и продуцировании энергии
- 2321597 Биоматерьял, способ его приготовления и его применение, медицинское средство, имплантант и вкладыш
- 2121340 Средство для похудения
- 2220737 Средство для улучшения состояния опорно-двигательного аппарата
- 2220729 Гель используемый в стоматологии
- 2320720 Способ культивирования фибропластов для заместительной терапии
- 2320378 Накожный аппликатор
- 2320369 Средства, содержащие Альфа - 2 - Дельта Лиганды и ингибиторы обратного захвата серотонина/норадреналина
- 2320362 Местные фармацевтические средства, содержащие проантоцианидины, для лечения дерматитов
- 2320322 Биоадгезивная доставка лекарств
- 2320318 Чувствительное к температуре изменяющие состояние средство гидрогеля
- 2025120 Способ получения препарата, содержащего Фактор /G-CSF/, стимулирующий рост колоний гранулоцитов
- 2319490 Средство для введения железа при лечении синдрома беспокойных ног
- 25995 Содержащее адгезив приспособление для фиксации зубных протезов в полости рта
- 2218907 Средство для ухода за кожей лица и веками
- 2318830 Способ получения модифицированного дерматансульфата
- 2118153 Косметика - туш для ресниц
- 2217441 Способ получения полимера
- 2317296 Изетионатная соль селективного ингибитора CDK4
- 2217171 Мембрана для использования при направленной регенерации тканей
- 2317095 Экстракты ECHINACEA ANGUSTIFOLIA
- 2216332 Препарат для лечения астроза
- 2216314 Крем - маска для обезвоженной кожи
- 2316333 Средство оздоровительно-восстановительных косметических панто-магниевых ванн
- 2021304 Способ получения биологически активного средства
- 2115662 Способ получения гиалуроновой кислоты
- 2315627 Впрыскиваемые имплантанты на керамической основе для заполнения морщин, кожных впадин, шрамов
- 2315623 Средство получаемое путем лиофилизации препарата
- 2114862 Способ получения гиалуроновой кислоты
- 2314791 Лечебно-Косметическое средство
- 2314791 Косметический крем-бальзам для ухода за кожей лица и шеи
- 2214600 Способ оценки эффективности лечения неврологических проявлений
- 2114602 Способ косметической обработки
- 2114587 Раствор для защиты роговицы
- 2214283 Имплантант для подкожного или внутрикожного введения
- 2313370 Медицинские протезы, имеющие улучшенную биологическую совместимость
- 2313356 Препарат для лечения демодекоза
- 2313338 Средство на основе этиллинолеата и триэтилцитрата для лечения себореи и угрей
- 2313328 Косметика содержащая тонкодисперный и пористый порошок
- 2212880 Способ получения препарата содержащего антибиотик, с замедленным высвобождением активного вещества
- 2312640 Способ лечения Блефароконьюнктивальной формы синдрома сухого глаза
- 2017751 Способ получения гиалуроновой кислоты
- 2312145 Гены CORYNEBACTERIUM GLUTAMICUM, кодирующие белки, участвующие в синтезе мембран и мембранном транспорте
- 2311458 Белки вызывающие измененную иммуногенную реакцию. Способ их получения и использования
- 2311183 Улучшенное разделение с использованием гталуроновой кислоты
- 2311177 Ингибиторы интегрина для лечения заболевания глаз
- 2300069 Косметическая маска
- 2211024 Уход за сухой кожей
- 2310440 Раствор для защиты роговицы от повреждений
- 2309684 Лечение межфалангового остеоатроза узелковой формы
- 2309406 Способ мониторинга фиброза печени у больных хроническим гепатитом с (ХГС)
- 2209088 Опосредованная рецепторами доставка генов с использованием векторов на основе бактериофагов
- 2308967 Уменьшение объема ткани
- 2308962 Средство для опорно-дигательного аппарата
- 2308957 Способ получения препарата для мезотерапии
- 2308954 Средство для лечения ран, содержащее плазму или сыворотку крови
- 2308951 Комплексный способ профилактики вагинальных дисбактериозов
- 2308937 Косметическая биологически активная добавка и косметический литофитокомплекс на ее основе
- 2208638 ДНК (варианты), способ получения белка
- 2207885 Способ подачи небольшого объема лечебного раствора к целевому месту
- 2207858 Лишенные побочных эффектов производные простагландинов для лечения глаукомы
- 2207845 Твердая лекарственная форма пролонгированного действия
- 2207844 Препарат для местного неинвазивного применения
- 2207841 Средства с антиферментативным действием
- 2306335 Стволовые клетки и решетки полученные из жировой ткани
- 2306140 Новые рецепторы для Helicobacter pylori и их применение
- 2205612 Способ эндотелизации IN VITRO протезов кровеносных сосудов
- 2105540 Депигментирующее средство
- 2304960 Косметическое средство для кожи
- 2304616 Гены участвующие в гомеостазе и адаптации
- 2204550Способ получения длинноцепочечной N-Ацилированной кислотой Аминокислот
- 2204415 Способ получения изображения
- 2204394 Средство для лечения грибковых инфекций, желудочных язв
- 2204366 Способ хирургического лечения глаукомы
- 2104034 Вагинальное увлажняющие средство, способ его получения
- 2303991 Биологически активная добавка
- 2303990 БАД
- 2303973 Адсорбирующее изделие
- 2203676 Средство обладающее иммунокорригирующим действием
- 2203672 Способ предупреждения беременности
- 2303635 Гены кодирующие белки резистентности и толерантности к стрессам
- 2303529 Способ фиксации альгинатного геля на твердой фазе, способ получения клеточного чипа на его основе
- 2203078 Способ лечения гнойных ран
- 2302412 Гидразоно-малонитрилы
- 2102400 Способ получения гиалуроновой кислоты
- 2202356 Способ стимуляции репаративных процессов длительно незаживающих ран и трофических язв
- 2202336 Средство для ухода за кожей
- 2302231 Глазные капли
- 2102082 Способ магнитометрического исследования тела человека или животного
- 2301814 Полиакриламидный гидрогель
- 2201765 Гибридные матричные имплантанты и эксплантанты
- 2301677 Биотрансплантант для лечения дегенеративных и трвматических заболеваний хрящевой ткани и способ его получения
- 2301676 Способ лечения ревматизма
- 2301674 Способ лечения больных с переломами нижней челюсти
- 2301661 Средство с регулируемым освобождением и способ его получения
- 2005488 Средство для лечения болезней соединительной ткани
- 2200001 Крем для кожи
|
РОССИЙСКАЯ ФЕДЕРАЦИЯ

ФЕДЕРАЛЬНАЯ СЛУЖБА
ПО ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ
ПАТЕНТАМ И ТОВАРНЫМ ЗНАКАМ
|
Патент №2373769 |
(54) СИНБИОТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ДЕТЕЙ
(57) Реферат:
Препарат для применения в качестве питания содержит Bifidobacterium breve в количестве 1×104-1×1010 cfu/г и смесь неусваиваемых углеводов. Углеводы выбирают из неусваиваемых моносахаридов вплоть до гексасахаридов одинаковой углеводной структуры и из неусваиваемых гептасахаридов и высших полисахаридов одинаковой структуры, включающей инулин. Предложены добавка в питание детей и детское питание, содержащие вышеописанный препарат, а также его применения для лечения или профилактики иммунных нарушений у детей, и для детей, получающих искусственное или частично грудное питание. Применение препарата для изготовления композиции для профилактики и лечения недостаточного поглощения энергии. Применение препарата для изготовления композиции для ингибирования инфильтрации эозинофилов при аллергических заболеваниях. 7 н. и 9 з.п. ф-лы, 7 табл., 2 ил.
Область техники
Настоящее изобретение относится к препаратам, содержащим пробиотик и пребиотик, для младенцев, в особенности не получающих грудного кормления.
Предшествующий уровень техники
Младенцы не имеют кишечной флоры при рождении. В результате контакта с матерью при рождении и последующего грудного кормления происходит быстрое развитие и разрастание кишечной флоры. В ходе развития кишечная флора остается незрелой, находящейся в хрупком равновесии с окружающей средой, предрасположенной к быстрым изменениям и, следовательно, к заболеваниям, и поражению в присутствии патогенов. Известно, что младенцы, вскармливаемые грудью, в меньшей мере подвержены инфекциям или болезням, чем дети, получающие искусственное питание. Следовательно, младенцы, вскормленные грудью, менее подвержены желудочно-кишечным инфекциям в том, что касается как заболеваемости, так и длительности болезни, у них реже наблюдаются такие атопические заболевания, как аллергия, экзема, аллергическая астма, и они реже подвержены запорам, чем младенцы, получающие негрудное питание. Обычно кишечная флора младенцев, получающих грудное питание, главным образом, состоит из бифидобактерий и молочнокислых бактерий. Грудное молоко содержит олигосахариды материнского молока (НМО), являющиеся фактором роста для бифидобактерий в кишечнике младенцев. Флора младенцев, питающихся молочной смесью, более разнообразна и содержит обычно большее число видов Bacteroides, Clostridium и Enterobacteriaceae. В организме младенцев, получающих молочную смесь, содержится от одной десятой до двух третей от количества бифидобактерий в организме младенцев, получающих грудное питание. Считается, что бифидобактерии являются важными микроорганизмами, способствующими поддержанию хорошо сбалансированной кишечной микрофлоры, и постулируется, что бифидобактерии оказывают оздоровляющее действие, включающее профилактику и/или лечение диареи и кишечных инфекций. Кроме того, показано, что бифидобактерии играют определенную роль в иммунной системе хозяина.
Кишечная флора детей может быть модифицирована изменением состава питания путем потребления пробиотиков или пребиотиков. В качестве примера пробиотического подхода в EP-A-0904784 описано применение смеси штаммов микроорганизмов, включающей штаммы Bifidobacterium. Однако связанная с этим проблема состоит в том, что смесь микробов, обеспечивая некоторое полезное воздействие на здоровье, также может оказывать вредное действие на все еще незрелую кишечную флору младенцев, получающих искусственное питание, что связано с широким спектром действия такой смеси. Кроме того, многие пробиотические добавки имеют короткий срок годности и содержат слишком мало живых микроорганизмов, в результате чего они не способны оказывать ожидаемое пробиотическое действие.
Пребиотики определяются как неусваиваемые пищевые ингредиенты, которые селективно стимулируют рост и/или активность одной или более бактерий, находящихся в толстой кишке и в результате этого оказывают благоприятное влияние на хозяина (Gibson and Roberfroid, J. Nutr. 125:1401-1412, 1995). Предпочтительный путь улучшения кишечной флоры искусственно вскормленных детей заключается в стимуляции бифидобактерий, уже присутствующих в кишечнике детей, получающих искусственное питание, специфическими неперевариваемыми олигосахаридами, т.е. пребиотиками. Также в качестве пребиотиков была предложена смесь олигосахаридов и полисахаридов, например, согласно WO 00/08948. Примером такой смеси может служить комбинация галактоолигосахаридов с фруктополисахаридами. Было показано, что уровень содержания бифидобактерий в организме младенцев, питающихся молочной смесью, содержащей эти пребиотики, оказался выше, чем в случае питания стандартной молочной смесью (см. Moro et al., J. Pediatr. Gastroenterol. Nutr. 34:291-295, 2002).
Существующий до настоящего времени подход состоял в общей стимуляции бифидобактерий, т.е. на уровне рода. Род Bifidobacterium состоит из множества различных видов, отличающихся по метаболизму, ферментной активности, утилизации олиго- и полисахаридов, составу клеточной оболочки и взаимодействию с иммунной системой хозяина. В связи с этим можно ожидать, что не каждый вид Bifidobacterium оказывает одинаковое функциональное действие на ребенка. Примерами различных видов Bifidobacterium могут служить B. longum, B. breve, B. infantis, B. adolescentis, B. bifidum, B. animalis и B. dentium. Вид B.adolescentis превалирует во флоре взрослых людей и редко встречается в кале здоровых младенцев и детей. B. animalis и B. lactis не встречаются у людей, и B. dentium представляет собой патогенную бактерию. У здоровых младенцев бифидобактериальная флора в основном состоит из Bifidobacteriuminfantis, B. breve и B. longum. Kalliomaki et al. (Cur Opin Allergy Clin Immunol. 2003 Feb; 3(1):15-20 и цитированные там ссылки) сообщили, что страдающие аллергией младенцы имеют Bifidobacterium флору, подобную взрослым, тогда как типично детская Bifidobacterium флора была обнаружена у здоровых детей, что указывает на корреляцию между наличием некоторых видов Bifidobacterium и вероятностью развития аллергии. Эти результаты указывают на то, что стимуляция рода Bifidobacterium в толстой кишке ребенка может оказаться недостаточной. Целью изобретения является обеспечение у младенцев, получающих искусственное питание, флоры, напоминающей флору детей, вскормленных грудью, на уровне вида.
В настоящем изобретении термин «ребенок, вскормленный грудью», относится к младенцам, получающим исключительно материнское молоко. Термин «ребенок, не вскормленный или частично вскормленный грудью», относится к младенцам, не получающим или не исключительно получающим материнское молоко. Такое определение относится к младенцам, которые получают, по меньшей мере, содержимое бутылочки искусственного питания в день, т.е., по меньшей мере, 80 мл молочной смеси в день, остальное питание, если оно имеется, обеспечивается твердой пищей или жидкой пищей, такой как материнское молоко, т.е. определение относится к младенцам, частично питающимся материнским молоком.
Сущность изобретения
Обнаружено, что повышение уровня содержания Bifidobacterium при использовании смесей неусваиваемых углеводов также регулирует популяцию Bifidobacterium в сторону популяции, более подобной детской, т.е. обедненной B. catenulatum, B. pseudocatenulatum и B. adolescentis, тогда как младенцы, питающиеся стандартной молочной смесью, имеют флору, в большей мере подобную взрослым, в которой доминируют B. catenulatum, B. pseudocatenulatum и B. adolescentis. Также обнаружено, что популяция Bifidobacterium у младенцев, питание которых включает пребиотики, содержит недостаточное количество одного конкретного микроорганизма, а именно Bifidobacterium breve.
В соответствии с одним аспектом изобретение предусматривает препарат, содержащий Bifidobacterium breve и смесь неусваиваемых углеводных пребиотиков. Обнаружено, что такой препарат полезен и очень подходит для регулирования популяции Bifidobacterium на уровне видов в желудочно-кишечном тракте детей. Кроме того, неожиданно было обнаружено, что добавление других видов Bifidobacterium, помимо B. breve, не является обязательным, поскольку уже проведена достаточная регуляция самим препаратом.
Согласно другому аспекту изобретение предусматривает препарат, содержащий Bifidobacterium breve и смесь неусваиваемых углеводных пребиотиков, которая содержит, по меньшей мере, два различных, достаточно растворимых углеводных компонентов А и В.
Другой аспект изобретения предусматривает применение препарата для детей, не получающих полностью или частично грудное питание.
Согласно еще одному аспекту изобретение предусматривает применение препарата для производства композиции, предназначенной для регулирования популяции видов Bifidobacterium в желудочно-кишечном тракте детей, не получающих полностью или частично грудное питание.
Согласно еще одному аспекту изобретение предусматривает применение препарата для производства композиции, предназначенной для профилактики или лечения состояния иммунной системы.
Согласно другому аспекту изобретение предусматривает применение смеси углеводов для регулирования популяции Bifidobacteriumcatenulatum, B. pseudocatenulatum и/или Bifidobacterium adolescentis в желудочно-кишечном тракте детей, не получающих полностью или частично грудное питание.
Согласно еще одному аспекту изобретение предусматривает способ видоспецифичного детектирования и количественного определения видов рода Bifidobacterium, обнаруженных в организме человека, в особенности детей, а также диагностический набор для обнаружения и количественного определения видов Bifidobacterium.
Подробное описание изобретения
Препарат
1) Bifidobacterium breve
Bifidobacterium breve является необходимым ингредиентом изобретения. Методом определения, предложенным авторами, было обнаружено, что эта бактерия присутствует в ограниченных количествах у младенцев, получающих искусственное питание. Соответственно, введение этой бактерии совместно со смесью углеводов позволяет нормализовать популяцию видов Bifidobacterium до уровня, эквивалентного тому, который имеется в желудочно-кишечном тракте ребенка, вскармливаемого грудью.
Предпочтительные штаммы Bifidobacterium breve могут быть выбраны из изолятов кала здоровых младенцев, вскармливаемых грудью. Обычно эти штаммы коммерчески доступны от производителей молочнокислых бактерий, но они могут быть непосредственно выделены из кала, идентифицированы, охарактеризованы и продуцированы. Примерами коммерчески доступного B. breve может служить B. breve Bb-03 от Rhodia, B. breve MV-16 от Morinaga и B. breve от Institut Rossel, Lallemad, но B. breve также может быть получен из таких коллекций культур, как DSM 20091 и LMG 11613.
Количество B. breve в препарате изобретения основывается на общем количестве растворимых неусваиваемых углеводов и предпочтительно составляет 107-1011, более предпочтительно 108-1010 cfu (колониеобразующих единиц) бактерий на г общего количества углеводов. В том случае, когда препарат применяют в качестве добавки, предпочтительно, чтобы Bifidobacterium breve присутствовал в количестве 1·106-1,5·1011 cfu/г, предпочтительно 3·107-5·1010 cfu/г, более предпочтительно 5·108-1·1010 cfu/г. В случае применения препарата в качестве (полного) детского питания, наиболее предпочтительно, чтобы количество B. breve в пище составляло 1·104-1·1010 cfu/г, предпочтительно 5·106-3·109 cfu/г, более предпочтительно 1·107-5·108 cfu/г детского питания. Эту концентрацию выбирают таким образом, чтобы суточная доза составляла 1·106-1,5·1011 cfu/г, предпочтительно 3·107-5·1010 cfu/г, более предпочтительно 5·108-1·1010 cfu/г.
2) Смесь неусваиваемых углеводных пребиотиков
Смесь неусваиваемых углеводных пребиотиков также является существенным элементом изобретения. Термин «неусваиваемые» означает, что углеводы в желудочно-кишечном тракте остаются непереваренными и попадают в толстую кишку в нересорбированной форме.
Согласно изобретению смесь неперевариваемых углеводов содержит, по меньшей мере, два различных, достаточно растворимых углеводных компонента А и В, которые не перевариваются в желудочно-кишечном тракте и попадают в толстую кишку в нересорбированном виде. Смесь углеводов согласно изобретению также может состоять исключительно из этих двух углеводных компонентов А и В.
В смеси, по меньшей мере, из двух неусваиваемых растворимых углеводных компонентов А и В углеводный компонент А присутствует в количестве 5-95% мас. от суммы углеводных компонентов А и В. Более того, по меньшей мере, 50%, предпочтительно, по меньшей мере, 75% от общего количества неусваиваемых растворимых углеводов компонентов А и В выбирают из дисахаридов вплоть до эйкозасахаридов (полисахариды, содержащие 20 моносахаридных звеньев); оставшееся количество может относиться к неусваиваемым моносахаридам и неусваиваемым полисахаридам, содержащим более 20 звеньев. Также предпочтительно, чтобы более 95%, предпочтительно более 98% от общего количества растворимых неусваиваемых углеводов имели длину цепи не более 100 звеньев. При указании в описании процентных и средних значений подразумеваются массовые проценты и средние значения, кроме очевидного использования другого базиса или особо оговоренных случаев.
Углеводы в компонентах могут различаться в трех аспектах:
(i) по (среднему) числу моносахаридных звеньев в углеводе, причем средняя длина цепи компонента А, по меньшей мере, на 5 моносахаридных звеньев короче, чем средняя длина цепи компонента В; это означает, что если углеводы А и В содержат одинаковые структурные звенья, т.е. образуют смесь гомологов, отличающихся только длиной цепи, то распределение гомологов должно иметь два максимума, один из которых соответствует значению менее 7, а другой более 7, причем два таких максимума расположены на расстоянии, по меньшей мере, 5 звеньев друг от друга; в этом случае углеводы, содержащие до 6 звеньев (гексасахариды) составляют часть компонента А, а углеводы из 7 звеньев (гептасахариды) являются частью компонента В;
(ii) по структуре моносахаридных звеньев углевода, причем компонент А построен из различных структурных звеньев компонента В; в том случае, когда А и/или В построены из повторяющихся комбинаций различных моносахаридных звеньев, например, в случае галактоманнанов и арабиногалактанов, по меньшей мере, 50% моносахаридных звеньев указанных двух компонентов должны отличаться друг от друга (в приведенном выше примере или один, или оба компонента должны содержать менее 50% ангидрогалактозных звеньев);
(iii) оба компонента А и В отличаются друг от друга по (средней) длине цепи и структуре; такое воплощение является предпочтительным.
Предпочтительно, компонент А выбирают из неусваиваемых моносахаридов вплоть до гексасахаридов одинаковой углеводной структуры, а компонент В выбирают из гептасахаридов и высших полисахаридов с одинаковой углеводной структурой. Таким образом, углеводный компонент А состоит, по меньшей мере, из одного неусваиваемого моносахарида или, по меньшей мере, одного неусваиваемого олигосахарида. Под термином «олигосахариды» понимают углеводы, содержащие от 2 до 6 моносахаридных звеньев включительно. Предпочтительно, углеводный компонент А также может быть образован смесью двух или более указанных сахаридов. Следовательно, он может состоять из любого числа моносахаридов и/или олигосахаридов такого типа, т.е. одинаковой структуры.
Согласно такому предпочтительному варианту осуществления углеводный компонент В состоит, по меньшей мере, из одного полисахарида, включающего 7 или более моносахаридных звеньев. Под термином «полисахариды» понимают углеводы, начиная от гептасахарида (например, гептасахарид, октасахарид, нонасахарид, декасахарид и т.д.). Верхний предел длины цепи полисахаридов специально не оговаривается, и они могут иметь длину в несколько сотен и даже несколько тысяч моносахаридных звеньев. Однако согласно изобретению цепи длиной более 100 (около 16 кДа), особенно более 700 (около 100 кДа) менее предпочтительны. Предпочтительно, компонент В содержит не более 5% или даже не более 2% гомологов, состоящих из более чем 100 моносахаридных звеньев. Углеводный компонент В также должен состоять лишь из одного полисахарида такого типа или, предпочтительно, из двух или более полисахаридов указанного типа с различной длиной цепи, т.е. имеющих одинаковую структуру.
Углеводный компонент А составляет до 95% мас. от суммарного количества углеводного компонента А и углеводного компонента В (А+В=100% мас.). Углеводный компонент В составляет 5-95% мас. от суммарного количества углеводного компонента А и углеводного компонента В. Согласно предпочтительному варианту осуществления количество компонента А составляет 95-60% мас., предпочтительно 95-80% мас. и особенно предпочтительно 95-90% мас., и количество компонента В составляет 5-40% мас., предпочтительно 5-20% мас. и особенно предпочтительно 5-10% мас. от суммарного количества углеводов, при условии, что А+В=100% мас.
Термин «растворимый углевод» в контексте изобретения относится к углеводам с растворимостью, по меньшей мере, 50% согласно методу, описанному L.Prosky et al., J.Assoc. Anal. Chem. 71:1017-1023, 1988.
По меньшей мере, 80% углеводов или сахаридов из суммы углеводных компонентов А и В обладают пребиотическим действием. Предпочтительно, по меньшей мере, 80% углеводов, входящих в состав углеводного компонента А, а также, по меньшей мере, 80% углеводов, относящихся к углеводу В, проявляют пребиотический эффект. Другими словами, предпочтительно, чтобы, по меньшей мере, 80% мас. каждого углевода или сахарида из углеводных компонентов А и В достигали толстой кишки в неусваиваемом (следовательно, не способном к поглощению в тонких кишках) состоянии. Таким образом, рассматриваемые углеводы или сахариды углеводных компонентов А и В, находящиеся в желудочно-кишечном тракте, не поглощаются и не перевариваются в желудке или тонких кишках, и попадают в толстую кишку в неизмененном виде.
Согласно изобретению термин «пребиотически активный углевод» относится к углеводу, который попадает в толстую кишку в непереваренном виде (и, следовательно, не поглощается в тонких кишках), и селективно стимулирует рост и/или активность одного или ограниченного числа бактериальных видов, присутствующих в кишечнике, и, таким образом, способствует сохранению здоровья. Рассматриваемый пребиотический эффект таких углеводов и специфические механизмы их действия подробно описаны в работе  G.F. Gibson & M.B. Roberfroid, J. Nutr. 1995; 125: 1401-1412 G.F. Gibson & M.B. Roberfroid, J. Nutr. 1995; 125: 1401-1412 , на которую специально сделана ссылка и содержание которой включено в настоящее описание. , на которую специально сделана ссылка и содержание которой включено в настоящее описание.
Максимальное количество пребиотически неактивных углеводов или сахаридов в углеводных компонентах А и В составляет 20%. Такие углеводы или сахариды относятся к растворимым веществам, которые могут быть выделены в непереваренной форме. Такие углеводы способны производить физический эффект, состоящий, например, в увеличении объема фекалий или ускоренном поглощении воды.
Для оценки соотношения углеводных компонентов А и В в диетическом или фармацевтическом продукте осуществляли следующие стадии. На первой стадии растворимые углеводы экстрагировали из продукта водой. Жиры и белки удаляли из экстракта. На второй стадии растворимые углеводы или экстракт, соответственно, отрабатывали человеческими ферментами, например человеческой амилазой, соком поджелудочной железы или препаратами реснитчатого края клеток тонких кишок. В результате получали неусваиваемые углеводы (за исключением in vivo поглощаемых моносахаридов, полученных в эксперименте in vitro), представляющие собой два углеводных компонента А и В. Предполагается, что 80% от их количества обладает пребиотической активностью.
Таким образом, смеси углеводов, предназначенные для применения в препарате изобретения, представляют собой смеси, в которых углеводы, растворимые и неусваиваемые в описанном выше смысле, удовлетворяют указанному выше критерию и составляют компоненты А и В.
Углеводный компонент А может состоять, например, из одного или нескольких следующих углеводов:  -галактоолигосахаридов, -галактоолигосахаридов,
 -галактоолигосахаридов, фруктоолигосахаридов, -галактоолигосахаридов, фруктоолигосахаридов,
инулоолигосахаридов, фукоолигосахаридов, манноолигосахаридов,
ксилоолигосахаридов, сиалилолигосахаридов,
N-гликопротеинолигосахаридов, О-гликопротеинолигосахаридов,
гликолипидолигосахаридов, целоолигосахаридов,
хитозанолигосахаридов, хитинолигосахаридов,
галактуронолигосахаридов, глюкуроноолигосахаридов,
 -глюкан (например, 1,3-) олигосахаридов, -глюкан (например, 1,3-) олигосахаридов,
арабиноксилоолигосахаридов, арабиногалактоолигосахаридов,
ксилоглюкоолигосахаридов, галактоманноолигосахаридов,
рамноолигосахаридов,
соевых олигосахаридов (стахиоза, раффиноза, вербаскоза) и
лакто-N-неотетраоз, и углеводный компонент В может, например, включать один или более следующих углеводов или сахаридов, таких как фрукт(оз)аны, включая инулины, галактаны, фукоиданы, арабинаны, ксиланы, ксантаны,  -глюканы, неусваиваемая полидекстроза, неусваиваемый мальтодекстрин, галактуронаны, N-гликаны, О-гликаны, гиалуроновая кислота, хондроитины, ксилоглюканы, арабиногалактаны, гуммиарабик, альгинаты, каррагенаны, галактоманнаны, глюкоманнаны, арабиноксиланы, гликолипидгликаны, гликопротеингликаны, протеогликаны, соевые полисахариды. Следует отметить, что усваиваемые углеводы не являются частью компонентов А и В. Так, глюкоза, фруктоза, галактоза, сахароза, лактоза, мальтоза и мальтодекстрины не входят в состав указанных компонентов даже в том случае, если они являются низшими гомологами галактоолигосахаридов, фруктоолигосахаридов, (инулин) и т.п. Неусваиваемые углеводы изобретения, как правило, не содержат значительных количеств глюкозных звеньев, связанных по альфа 1,4 и/или альфа 1,6 положениям, как в производных крахмала, поскольку такие углеводы являются усваиваемыми. Однако некоторые полисахариды и мальтодекстрины крахмального типа могут стать неусваиваемыми или «устойчивыми» с помощью физических и ферментативных способов; такие олиго- и полисахариды охватываются настоящим изобретением до тех пор, пока они обладают существенной растворимостью. -глюканы, неусваиваемая полидекстроза, неусваиваемый мальтодекстрин, галактуронаны, N-гликаны, О-гликаны, гиалуроновая кислота, хондроитины, ксилоглюканы, арабиногалактаны, гуммиарабик, альгинаты, каррагенаны, галактоманнаны, глюкоманнаны, арабиноксиланы, гликолипидгликаны, гликопротеингликаны, протеогликаны, соевые полисахариды. Следует отметить, что усваиваемые углеводы не являются частью компонентов А и В. Так, глюкоза, фруктоза, галактоза, сахароза, лактоза, мальтоза и мальтодекстрины не входят в состав указанных компонентов даже в том случае, если они являются низшими гомологами галактоолигосахаридов, фруктоолигосахаридов, (инулин) и т.п. Неусваиваемые углеводы изобретения, как правило, не содержат значительных количеств глюкозных звеньев, связанных по альфа 1,4 и/или альфа 1,6 положениям, как в производных крахмала, поскольку такие углеводы являются усваиваемыми. Однако некоторые полисахариды и мальтодекстрины крахмального типа могут стать неусваиваемыми или «устойчивыми» с помощью физических и ферментативных способов; такие олиго- и полисахариды охватываются настоящим изобретением до тех пор, пока они обладают существенной растворимостью.
В результате селективной комбинации олигосахаридов и полисахаридов и одновременного присутствия углеводных компонентов А и В в толстой кишке могут стимулироваться положительно влияющие на здоровье микроорганизмы и/или могут подавляться патогенные микроорганизмы, причем такие воздействия осуществляются значительно более эффективно, чем при применении только одного из указанных углеводных компонентов. При введении углеводной комбинации можно обеспечить очень быструю нормализацию флоры толстой кишки с целью ее поддержания или профилактики изменения кишечной флоры при различных стрессовых ситуациях и, таким образом, влиять на колонии бактерий в толстой кишке таким способом, который более эффективен, чем при использовании ранее известных углеводов.
Согласно предпочтительному варианту осуществления, по меньшей мере, 80% мас. углеводного компонента А, а также углеводного компонента В, входят в состав углеводов, которые являются бифидогенными и/или стимулируют молочнокислые бактерии. Как было неожиданно обнаружено, в результате использования комбинации олигосахаридов и полисахаридов, обладающей указанными выше свойствами, может стимулироваться более сильное воздействие на рост молочнокислых бактерий, чем в случае олигосахаридов или полисахаридов в отдельности. В результате стимулируются не только те молочнокислые бактерии, которые естественно присутствуют в кишечнике, но также оказывается стимулирующее, иногда селективное, воздействие на рост экзогенно вводимых бактерий.
Помимо рассматриваемого непрямого воздействия через сами бактерии и их метаболиты, такие как органические кислоты (ацетаты, лактаты и т.п.), изменение рН и стимулирование колонизатов, также оказывается непосредственное положительное физическое действие на перистальтику, содержание воды, количество фекалий и механическое воздействие на слизистую оболочку кишечника.
Таким образом, углеводные смеси характеризуются не только питательным действием, но также широким спектром активности. Помимо описанных выше биологических эффектов, с помощью смесей настоящего изобретения могут достигаться следующие эффекты: стабилизация естественной микрофлоры, профилактика срастания патогенных веществ/организмов, таких как токсины, вирусы, бактерии, грибки, трансформированные клетки и паразиты, растворение комплексов токсинов, вирусов, бактерий, грибков и других патогенов, содержащих эндогенные клетки, а также их удаление из организма и ускорение заживления ран.
Таким образом, рассматриваемые смеси могут применяться для профилактики и/или лечения симптомов или заболеваний, связанных с нарушением кишечной флоры, например, являющейся следствием ассоциации или адгезии указанных веществ и организмов с эпителием или другими эндогенными клетками.
Обнаружено, что углеводные смеси особенно эффективны в том случае, когда углеводный компонент А имеет структуру, отличающуюся от структуры компонента В. Такая различная структура может быть связана, например, с составом моносахаридов, когда, с одной стороны, используют фруктаны, а с другой - галактаны. Кроме того, структурные отличия могут быть связаны с характером гликозидной связи (например, отличия между связями в  -галактоолигасахаридах и -галактоолигасахаридах и  -галактоолигасахаридах, или в -галактоолигасахаридах, или в  -глюканах (крахмал) и -глюканах (крахмал) и  -глюканах (целлюлоза)). Состав мономеров, а также характер гликозидной связи могут оказывать влияние на химические свойства (например, растворимость) или физиологические характеристики (например, перевариваемость). -глюканах (целлюлоза)). Состав мономеров, а также характер гликозидной связи могут оказывать влияние на химические свойства (например, растворимость) или физиологические характеристики (например, перевариваемость).
Следует иметь в виду, что углеводы одинакового строения являются гомологами, которые могут отличаться длиной цепи, но состоят из одинаковых моносахаридных звеньев или их комбинаций. Как правило, последующий гомолог отличается от предыдущего добавлением одного моносахаридного звена, присутствующего в предыдущем гомологе. Тем не менее, одно звено, обычно концевое, может быть другим, как это имеет место в некоторых фруктанах, содержащих цепь из (ангидро)фруктозных звеньев с концевым глюкозным звеном.
Предпочтительно, чтобы длина полисахаридной цепи компонента В или средневзвешенная длина цепи в случае смеси полисахаридов была, по меньшей мере, на три, предпочтительно, по меньшей мере, на пять звеньев больше длины олигосахаридной цепи компонента А или средневзвешенной длины цепи смеси олигосахаридов. Предпочтительно, чтобы средняя длина цепи олигосахаридов А составляла 2-6 звеньев, а средняя длина цепи полисахаридов В составляла 7-30 звеньев, более предпочтительно 8-20 звеньев. В случае присутствия как олигосахаридов, так и полисахаридов одинакового строения, углеводы такой структуры рассматриваются как компонент А в том случае, когда средневзвешенная длина цепи имеет значение менее 6,5, и индивидуальные элементы с длиной цепи 7 и выше не относятся к компоненту А; с другой стороны, они рассматриваются как компонент В в том случае, когда средневзвешенная длина цепи имеет значение около 6,5 и в этом случае индивидуальные компоненты с длиной цепи 6 и ниже не относятся к компоненту В. В случае наличия олигосахаридов и полисахаридов одинакового строения в отсутствие сахаридов иной структуры должно существовать два максимума с каждой стороны от 7 звеньев, или иначе, как разъяснялось выше, не удовлетворяется условие наличия двух различных углеводных компонентов.
В таких углеводах inter alia может наблюдаться существенная часть смесей. При введении смесей углеводов различного размера и/или различных «классов», либо «структур» может наблюдаться синергетический эффект, по сравнению с пребиотическим действием веществ группы А и В в отдельности.
Углеводы компонента А могут принадлежать к одному классу соединений, но также могут состоять из нескольких классов (например, А может представлять собой смесь галактоолигосахаридов и фукоолигосахаридов), тогда как углеводы компонента В в равной степени могут происходить из соединений одного или нескольких классов (например, В может представлять собой смесь инулина с ксиланами).
Предпочтительная углеводная смесь состоит из галактоолигосахаридов и инулина.
Особенно эффективные смеси содержат, по меньшей мере, 60% мас., предпочтительно 80-100% мас. углеводных компонентов А, принадлежащих к группе галактоолигосахаридов. Предпочтительные смеси также могут содержать, по меньшей мере, 60% мас., предпочтительно 80-100% мас. углеводных компонентов В, принадлежащих к группе фруктополисахаридов. Для получения углеводных смесей могут использоваться известные углеводы и их смеси, применяемые для производства пищи или пищевых продуктов. Также можно использовать сырье, предварительно модифицированное специальными методами. Получение смесей может реализоваться в результате простого смешивания соответствующим образом выбранных углеводов или олигосахаридов с полисахаридами или смесями углеводов. Исходные компоненты должны смешиваться друг с другом таким образом, чтобы соответствовать параметрам готовых смесей. В качестве сырья могут использоваться резервные углеводы (фруктаны, галактоолигосахариды бобовых культур, фукоидан,  -глюкан, ламинарин, каррагенан, мананны, галактоманнаны, агар), природная смола, углеводы гликопротеинов с N-гликозидной связью, углеводы гликопротеинов с О-гликозидной связью, гликаны гликолипидов, углеводы, полученные ферментацией (галактоолигосахариды, глюкоолигосахариды, фруктоолигосахариды, ксилоолигосахариды), бактериальные углеводы (такие как ксантаны), а также олигосахариды (галактоолигосахариды, глюкоолигосахариды (с -глюкан, ламинарин, каррагенан, мананны, галактоманнаны, агар), природная смола, углеводы гликопротеинов с N-гликозидной связью, углеводы гликопротеинов с О-гликозидной связью, гликаны гликолипидов, углеводы, полученные ферментацией (галактоолигосахариды, глюкоолигосахариды, фруктоолигосахариды, ксилоолигосахариды), бактериальные углеводы (такие как ксантаны), а также олигосахариды (галактоолигосахариды, глюкоолигосахариды (с  1-2 и 1-2 и  1-3 глюкозными остатками), ксилоолигосахариды), а также скелетные углеводы, такие как целлюлоза, гемицеллюлоза (арабинаны, галактаны), пектины и хитины. Предпочтительно, чтобы такие вещества были пищевой степени чистоты (Complex Carbohydrates in Foods, British Nutrition Foundation; Chapman & Hall, London 1990). 1-3 глюкозными остатками), ксилоолигосахариды), а также скелетные углеводы, такие как целлюлоза, гемицеллюлоза (арабинаны, галактаны), пектины и хитины. Предпочтительно, чтобы такие вещества были пищевой степени чистоты (Complex Carbohydrates in Foods, British Nutrition Foundation; Chapman & Hall, London 1990).
Также возможно проведение ферментативной модификации сырья и продуктов с помощью гидролаз (например, глюкозидаз, трансгликозидаз и липаз), трансфераз, изомераз (например, альдолаз и кетолаз), оксидоредуктаз (например, оксидаз) и редуктаз (например, глюкозагидрогеназ), лиаз (например, полисахаридных лиаз) и лигаз. Кроме того, можно осуществлять технологическую модификацию сырья и продуктов посредством воздействия давления (например, при экструзии), температуры (например, при карамелизации), с помощью органических синтезов, органической модификации (например, карбоксиметилирование и перацетилирование), кислотного и/или основного гидролиза и фракционирования (например, по размеру и/или физико-химическим параметрам, таким как заряд и гидрофобность) или используя комбинацию модификаций.
Таким образом, углеводные смеси состоят, по существу, из следующих ниже моносахаридов и состоящих из них олигосахаридов и полисахаридов: D-глюкоза, D-фруктоза, D-галактоза, D-манноза, L-фукоза, D-N-ацетилглюкозамин, D-N-ацетилгалактозамин, D-ксилоза, L-рамноза, D-арабиноза, D-аллоза, D-талоза, L-идоза, D-рибоза, а также моносахариды, содержащие карбоксильные группы, такие как D-галакторуновая кислота, D-глюкуроновая кислота, D-маннуроновая кислота и/или их метилированные формы, такие как N-ацетилнейраминовая кислота, N-гликолилнейраминовая кислота и/или их О-ацетилированные производные. Кроме того, рассматриваемые мономеры и высшие звенья на их основе могут быть модифицированы группами -OSO3H и/или OPO3H.
Неусваиваемые углеводы согласно изобретению обычно применяют с суточной дозой 0,5-30 г, предпочтительно 2-15 г, более предпочтительно 3-9 г. Предпочтительно вводить препарат в виде добавки. Такая добавка подходит для приема детьми, получающими искусственное питание или частично грудное питание, включая недоношенных и доношенных детей, получающих искусственное или частично грудное питание.
Рассматриваемый препарат также может использоваться в качестве детского питания. В этом случае детское питание согласно изобретению дополнительно включает один или несколько ингредиентов, выбранных из усваиваемого углевода, источника липидов, источника белков и их смесей.
3) Прочие компоненты
Помимо углеводных компонентов А и В также могут присутствовать другие углеводы. К ним относятся 1) перевариваемые углеводы, которые усваиваются, как описано выше, и 2) нерастворимые углеводы, способные поглощаться/усваиваться, и даже те, которые не способны к ресорбции/перевариванию. Типичные нерастворимые, неперевариваемые углеводы, предназначенные для использования в качестве добавок к детскому питанию, представляют собой соевые полисахариды, а также устойчивый крахмал, целлюлозу и гемицеллюлозу; наиболее предпочтительные материалы выбирают из полисахаридов и устойчивого крахмала.
Типичные растворимые и усваиваемые углеводы, предназначенные для применения в качестве добавок к детскому питанию, выбирают из мальтодекстринов, крахмала, лактозы, мальтозы, глюкозы, фруктозы и сахарозы, и других моно- и дисахаридов, более предпочтительно из мальтодекстрина, лактозы, мальтозы, глюкозы, фруктозы, сахарозы и их смесей.
Помимо углеводных компонентов А и В, такие углеводы, пронумерованные как подпункты 1) и 2), могут присутствовать в смеси, как таковые, в любом произвольном количестве, причем в каждом случае в зависимости от желаемого конечного продукта. Предпочтительно, чтобы нерастворимые углеводы составляли 0-10% мас. от количества углеводных смесей.
Типичные ингредиенты, используемые в качестве источника липидов в пищевых добавках к детскому питанию, могут представлять собой любой липид или жир, подходящий для применения в детском питании. Предпочтительные источники липидов включают молочные жиры, подсолнечное масло, липид яичного желтка, масло канолы, оливковое масло, кокосовое масло, пальмовое масло, косточковое пальмовое масло, пальмовый олеин, соевое масло, подсолнечное масло, рыбий жир и масло, полученное микробной ферментацией, содержащее полиненасыщенные длинноцепочечные жирные кислоты. Такие масла могут быть в виде высших олеинов, как, например, в высоко олеиновом подсолнечном масле и высоко олеиновом саффлоровом масле. Кроме того, источник липидов может представлять собой фракции таких масел, как пальмовый олеин, триглицериды со средней длиной цепи (МСТ), и сложных эфиров жирных кислот, таких как арахидоновая кислота, линолевая кислота, пальмитиновая кислота, стеариновая кислота, докозагексаеновая кислота, линоленовая кислота, олеиновая кислота, лауриновая кислота, каприновая кислота, каприловая кислота, капроновая кислота и т.п.
Предпочтительный источник липидов для молочных смесей длительного хранения содержит триглериды со средней длиной цепи, предпочтительно в количестве 15-35% мас. от массы источника липидов.
Предпочтительно, источник липидов имеет молярное соотношение между n-6 и n-3 жирными кислотами в интервале 5:1-15:1, предпочтительно 8:1-10:1.
При наличии, предпочтительно, чтобы липид присутствовал в количестве 20-40% мас. от массы композиции или в количестве 0,8-1,5 г/100 кДж в детском питании.
Белки, которые могут использоваться в пищевых продуктах изобретения, включают любой белок или источник азота, подходящий для потребления человеком. Примеры подходящих источников белка для детского питания обычно включают казеин, сыворотку, сгущенное снятое молоко, обезжиренное молоко, сою, горох, рис, кукурузу, белковый гидролизат, свободные аминокислоты, источники белка, содержащие кальций в коллоидной суспензии белка или их смеси. Согласно изобретению предпочтительно использовать белок в виде гидролизата, что снижает вероятность развития аллергии у детей. Коммерческие источники белка являются легкодоступными и известны в данной области.
Гидролизаты детского питания на основе молока обычно содержат 100% сывороточный белок коровьего молока. В других молочных смесях для детского питания соотношение между казеином и сывороткой обычно составляет 1,8:0,3-3,0.
При наличии предпочтительно, чтобы источник белка присутствовал в количестве 9-19% мас. от массы композиции. Предпочтительное количество источника белка, используемого в детском питании, составляет 0,45-1,0 г/100 кДж.
Предпочтительная полноценная питательная смесь содержит диетологически значимые количества всех витаминов и минералов, необходимых для суточного рациона. К некоторым витаминам и минералам предъявляются минимальные требования. Примерами необязательных минералов, витаминов и других питательных веществ, присутствующих в детском питании, могут служить витамин А, витамин В, витамин В2, витамин В6, витамин В12, витамин Е, витамин К, витамин С, витамин D, фолиевая кислота, инозит, ниацин, биотин, пантотеновая кислота, холин, кальций, фосфористый йод, железо, магний, медь, цинк, марганец, хлорид, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минералы обычно добавляют в виде солей. Присутствие и количество конкретных минералов и других витаминов в значительной степени зависит от вида детской популяции, для которой предназначено питание.
При необходимости, детское питание может содержать эмульгаторы и стабилизаторы, такие как соевый лецитин, лимонная кислота, сложные эфиры моно- и диглицеридов и т.п. Эти компоненты особенно полезны для жидких смесей.
Детское питание может необязательно содержать другие вещества, оказывающие полезное действие, такие как (неуглеводные) волокна, лактоферин, иммуноглобулины, нуклеотиды, нуклеозиды и т.п.
Применение
Обнаружено, что препараты согласно изобретению особенно полезны для нормализации популяции Bifidobacterium в соответствии с видовым распределением у детей, получающих грудное кормление, считающегося «стандартом», в желудочно-кишечном тракте детей, получающих искусственное питание или частично вскармливаемых материнским молоком, в особенности у недоношенных детей, доношенных детей, а также детей в период адаптации к приему твердой пищи. Препараты изобретения также подходят для детей в период перехода от кормления грудью к искусственному вскармливанию.
Соответственно, предусматривается применение препарата или композиции согласно изобретению для производства композиции, предназначенной для нормализации популяции видов Bifidobacterium в желудочно-кишечном тракте детей, получающих искусственное питание или частично вскармливаемых материнским молоком. Также обнаружено, что препараты согласно изобретению особенно полезны для профилактики или лечения состояния иммунной системы. Предполагается, что иммунное состояние является следствием различия в составе видов Bifidobacterium в желудочно-кишечном тракте детей, получающих искусственное питание или частично вскармливаемых материнским молоком, по сравнению с детьми, питающимися материнским молоком. Обычно такие иммунные состояния включают состояния, выбранные из аллергии, атопического дерматита, экземы, астмы, атопии, аллергического ринита, пищевой аллергии, раздражения кожи от пеленок, диареи и комбинации указанных состояний.
Соответственно, изобретение предусматривает применение препарата для профилактики или лечения одного или нескольких состояний иммунной системы, предпочтительно выбранных из аллергии, атопического дерматита, экземы, астмы и раздражения кожи от пеленок. Кроме того, препарат изобретения может применяться для лечения (бактериальной) диареи и особенно вирусной диареи. Также предусматривается применение препарата согласно изобретению для профилактики и/или лечения нарушения поглощения энергии. Обнаружено, что препарат согласно изобретению может успешно применяться для ингибирования инфильтрации эозинофилов, нейтрофилов и одноядерных клеток при аллергических поражениях и/или ингибирования иммунной реакции Th2 типа, и/или стимуляции Th1 опосредованной иммунной реакции. Преимущественно предусматривается применение препарата или композиции согласно изобретению для производства композиции, предназначенной для ингибирования инфильтрации эозинофилов, нейтрофилов и одноядерных клеток при аллергических поражениях, ингибирования иммунной реакции Th2 типа и/или стимуляции Th1 опосредованной иммунной реакции.
Изобретение также предусматривает применение описанной выше углеводной смеси для регулирования популяции некоторых видов Bifidobacterium, отличных от B. breve, в особенности для уменьшения относительных количеств Bifidobacterium catenulatum, B. pseudocatenulatum и/или B. adolescentis.
Разработка зонда и диагностический набор
Изобретение также предусматривает способ количественного определения видов Bifidobacterium, в особенности обнаруженных у людей, т.е. Bifidobacterium catenulatum, B. pseudocatenulatum, B. adolescentis, B. breve, B. longum, B. bifidum, B. angulatum, B. infantis и B. dentium, с использованием видоспецифичных олигонуклеотидных праймеров и зондов.
Такие праймеры и зонды могут использоваться для идентификации бифидобактерий и бифидобактериальных видов с применением таких методов, как FISH, PCR, DGGE, TGGE, гибридизация методом дот-блоттинга и PCR в реальном времени. Общим во всех перечисленных методах является стадия гибридизации с использованием нуклеотидов. Особой целью является определение числа видов бифидобактерий с помощью PCR (полимеразная цепная реакция) в реальном времени
При функционировании в качестве зонда каждая из описанных ниже последовательностей может содержать дополнительные основания, связанные их 5'- или 3'-концами.
Такие олигонуклеотиды могут быть получены традиционными методами химического синтеза, например с использованием автоматического синтезатора ДНК. Фрагменты ДНК, содержащие указанные выше последовательности, могут быть получены ферментативным расщеплением генов соответствующих видов Bifidobacterium.
Согласно изобретению создание праймеров и зондов, специфичных к видам Bifidobacterium, для применения в 5'-нуклеазном анализе проводят следующим образом.
Были разработаны дуплексные 5'-нуклеазные анализы для Bifidobacterium adolescentis, B. angulatum, B. bifidum, B. breve, B. catenulatum, B. dentium, B. longum и B. infantis , в отношении ко всем бифидобактериям. Авторами было разработано 5'- нуклеазных анализов на межгенный спейсер 16S-23S rДНК вместо гена 16S rДНК, который обычно используют для филогенетического анализа и специфического определения бактерий. Выбор межгенного спейсера в значительной степени определяется тем фактом, что результаты, касающиеся загрязнений и чувствительности, были описаны для PCR в реальном времени при использовании 16S rДНК. Кроме того, описано большое сходство между последовательностями 16S rДНК различных видов Bifidobacterium (Leblond-Bourget et al. 1996), что делает практически невозможным создание серий праймеров и зондов, специфичных к различным видам Bifidobacterium. Неожиданно эти проблемы удалось решить с использованием межгенной спейсерной области.
Для создания праймеров и зондов отличающиеся последовательности 16S-23S межгенной спейсерной области различных видов Bifidobacterium (B. adolescentis [U09511 U09512 (1), U09513 (1) и U09514 (1)]a, B. angulatum [U09515 (1)]a, B. animalis [AY225132 (2), L26967 (1) и UO9858 (1)]a, B. asteroides [UO9516 (1)]a, B. breve [AJ245850 (3), UO9518 (1), UO9519 (1), UO9520 (1) и UO9521 (1)]a, B. bifidum [U09517 (1), UO9831 (1)]a, B. catenalatum [UO9522]a, B. choerinum [L36968]a, B. coryneforme [UO9523]a, B. cuniculi [UO9790]a, B. dentium [UO10434]a, B. indicum [UO9791]a, B. infantis [AJ245851 (3), UO9525 (1), UO9527 (1) и UO9792 (1)]a, B. longum [AJ245849 (3), UO9832 (1)]a, B. pseudolongum [UO9524 (1), UO9879 (1)]a, B. magnum [UO9878] (1)]a, B. thermophilum [UO9528 (1)]a) получали из Genbank, на основе баз данных EMBL и DDBJ. Все полученные последовательности выравнивали с использованием DNASIS для Windows V2,5 (Hitachi Software Engineering Co., Ltd., Wembly, UK) (a=код доступа, 1=Leblond-Bouget, N., H. Philippe, I. Mangin, B. Decaris. 1996.) В результате анализа 16S РНК и 16S-23S внутренних транскрибированных спейсерных последовательностей была установлена интер- и интраспецифическая филогенность относительно Bifidobacterium. См. Int. J. Syst. Bacteriol. 46:102-11, 2=Ventura, M. and R. Zink. 2002.  Rapid identification, differentiation, and proposed new taxonomic classification of Bifidobacterium lactis Rapid identification, differentiation, and proposed new taxonomic classification of Bifidobacterium lactis . Appl. Environ. Microbiol, 68: 6429-6434., 3=Brigidi, P., B. Vitali, E. Swennen, L. Altomare, M. Rossi, D. Matteuzzi. 2000. . Appl. Environ. Microbiol, 68: 6429-6434., 3=Brigidi, P., B. Vitali, E. Swennen, L. Altomare, M. Rossi, D. Matteuzzi. 2000.  Specific detection of Bifidobacterium strains in pharmaceutical probiotic product and in human faces by polymerase chain reaction. Specific detection of Bifidobacterium strains in pharmaceutical probiotic product and in human faces by polymerase chain reaction. Syst. Appl. Microbiol. 23:391-399). Полные консервативные области последовательностей использовали для создания праймеров и зондов для всех видов Bifidobacterium. Консервативные области последовательностей подвидов различных типов, показавших низкую гомологию с другими видами, использовали для конструирования праймеров и зондов с целью определения B. adolescentis, B. angulatum, B. breve, B. bifidum, B. catenulatum, (включая B. pseudocatenulatum), B. dentium, B. infatis и B. longum (включая B. pseudolongum, что связано с высокой гомологией последовательности между этими двумя видами). Syst. Appl. Microbiol. 23:391-399). Полные консервативные области последовательностей использовали для создания праймеров и зондов для всех видов Bifidobacterium. Консервативные области последовательностей подвидов различных типов, показавших низкую гомологию с другими видами, использовали для конструирования праймеров и зондов с целью определения B. adolescentis, B. angulatum, B. breve, B. bifidum, B. catenulatum, (включая B. pseudocatenulatum), B. dentium, B. infatis и B. longum (включая B. pseudolongum, что связано с высокой гомологией последовательности между этими двумя видами).
Праймеры и TagMan MGB зонды конструировали с помощью Primer Express 1,5a (Applied Biosystems, Nieuwerkerk a/d IJssel, NL). Применяли следующие критерии: праймеры и зонды должны иметь содержание GC 30-80% и должны быть исключены эксперименты с использованием более 3 идентичных нуклеотидов (особенно для гуанидина (G)). Температура плавления зондов должна составлять 68-70°С, тогда как праймеры должны иметь температуру плавления на 10°С ниже. Кроме того, на 5'-конце зонда не должен присутствовать G и при этом отбирают цепь, содержащую большее количество цитозина (С), чем количество G. Пять последних нуклеотидов на 3'-конце праймеров должны содержать не более двух G и/или С оснований. Наконец, длина ампликона должна быть не более 150 пар оснований. Сконструированные праймеры и TagMan MGB зонды представлены в таблице 1 и тестированы на специфичность с использованием Basic Local Alignment Search Tool (BLAST).
Зонд, сконструированный для обнаружения всех видов Bifidobacterium, состоит из олигонуклеотида с репортерным красителем VICTM в положении 5' (Applied Biosystem, NL) и гасителем NFQ-MGBTM в положении 3' (Applied Biosystem, NL), а также зондами для различных видов Bifidobacterium олигонуклеотидов с 5' репортерным красителем, 6-карбоксифлуоресцином (FAMTM) и 3' гасителем - NFQ-MGBTM (Applied Biosystem, NL). Для определения общей бактериальной нагрузки использовали (универсальный) зонд широкого назначения и набор праймеров, который описан Nadkarmi, M.A., F.E. Martin, N.A. Jacques и N. Hunter в  Determination of bacterial load by real-time PCR using a broad-range (universal) probe and primer set Determination of bacterial load by real-time PCR using a broad-range (universal) probe and primer set . Microbiology 148: 257-266 (2002). Универсальный зонд состоит из олигонуклеотидов с 5' репортерным красителем, 6-карбоксифлуоресцином (FAMTM), и 3' гасителем красителя, 6-карбокситетраметилродамином (TAMRATM). Сконструированные зонды представлены в таблице 1. . Microbiology 148: 257-266 (2002). Универсальный зонд состоит из олигонуклеотидов с 5' репортерным красителем, 6-карбоксифлуоресцином (FAMTM), и 3' гасителем красителя, 6-карбокситетраметилродамином (TAMRATM). Сконструированные зонды представлены в таблице 1.
| Таблица 1 |
| Сконструированные праймеры и зонды для использования в 5'- нуклеазных анализах |
| Мишень |
Праймеры и зонды |
Последовательность
(51 3*) 3*) |
Т.пл.
(°С) |
% GC |
BLAST номер |
Длина ампликона |
SEQ ID No |
| B. adolescentis |
F_adol_IS |
ATA GTG GAC GCG AGC AAG |
59 |
52 |
1015335678-6465-18906 |
71 п.о. |
1 |
 |
R_adol_IS |
AGA TTG AAG AGT |
59 |
43 |
1015335740-7519-1624 |
 |
2 |
 |
P_adol_IS |
TTG GCG AAA TCG CTG AAA GAA CGT TTC TTT TTa |
69 |
30 |
1015335863-95222-17207 |
 |
3 |
| B. angulatum |
F_angul_IS |
TGG TGG TTT GAG AAC TGG |
59 |
46 |
1015336044-12581-14600 |
117 п.о. |
4 |
 |
R_angul_IS |
ATA GTG TCG ACG AAC AAC |
59 |
32 |
1015336147-14351-29932 |
 |
5 |
 |
P_angul_IS |
AAT AAA CAA AAC A AAG GCC AAA GCC TC |
70 |
57 |
1015488648-557-2104 |
 |
6 |
| B. bifidum |
F_bif_IS |
GTT GAT TTC GCC GGA CTC |
60 |
52 |
1015336612-215666-12828 |
105 п.о. |
7 |
 |
R-bif_IS |
TTC GCA AGC CTA |
60 |
56 |
1015336668-22451-30731 |
 |
8 |
 |
P_bif_IS |
TCG CGC AAA AAC TCC GCT GGC AAC A |
70 |
56 |
1015336773-24053-3416 |
 |
9 |
| B. breve |
F_breve_IS |
GTG GTG GCT TGA GAA CTG |
59 |
52 |
1015243936-11550-20333 |
118 п.о. |
10 |
 |
R_breve_IS |
GAT AG CAA AAC GAT |
58 |
32 |
1015244110-13595-29514 |
 |
11 |
 |
P_breve_IS |
CGA AAC AAA CAC TAA A TGA TTC CTC GTT CTT GCT GT |
69 |
45 |
1015244238-15062-16853 |
 |
12 |
| B. catanulatum |
F_cate_IS |
GTG GAC GCG AGC AAT GC |
58 |
65 |
1015335268-99-20718 |
67 п.о. |
13 |
 |
R_cate_IS |
AAT AGA GCC TGG CCA AAT |
58 |
50 |
1015335364-157142175 |
 |
14 |
 |
P-CATE_IS |
CG AAG CAA ACG ATG ACA TCA |
68 |
39 |
1015335455-2899-17859 |
 |
15 |
| B. dentium |
F_dent_IS |
CCG CCA CCC ACA GTC T |
59 |
71 |
1015399643-15856-19947 |
150 п.о. |
16 |
 |
R_dent_IS |
AGC AAA GGG AAA CAC CAT |
59 |
41 |
1015399751-16991-11210 |
 |
17 |
 |
P_dent_IS |
GTTT ACGCGTCCA ACGGA |
70 |
64 |
1015399833-18158-5198 |
 |
18 |
| B. infantis |
F_inf_IS |
CGC GAG CAA AAC AAT GGT |
58 |
47 |
1037961234-06371-14364 |
76 п.о. |
19 |
 |
R_inf_IS |
Ta
AAC GAT CGA |
58 |
36 |
1037961263-06691-25461 |
 |
20 |
 |
P_inf_IS |
AAC GAA CAA TAG AGT T TTC GAA ATC AAC AGC AAA
Aa |
69 |
32 |
1037961294-06967-17477 |
 |
21 |
| B. longum |
F_long_IS |
TGG AAG ACG TCG TTG GCT |
59 |
50 |
1015323391-27595-22257 |
109 п.о. |
22 |
 |
R_long_IS |
TT
ATC GCG CGA |
58 |
56 |
1015323469-28673-23147 |
 |
23 |
 |
P_long_IS |
GGC AAA AA CGC ACC CAC CGC A |
68 |
77 |
1015488566-4529-13934 |
 |
24 |
| Все Bifidobacterium |
F_allbif_IS |
GGG ATG CTG
CTG TGG AAG |
60 |
57 |
1015399960-19603-31240 |
231 п.о.a |
25 |
 |
R.alIbif_JS |
AGA
TGC TCG CGT |
60 |
57 |
1015400076-20827-17418 |
 |
26 |
 |
P_allbif_IS |
CCA CTA TCC AGT
TCA AAC CAC CAC GCG CCA |
70 |
61 |
1015400166-21749-18424 |
 |
27 |
| а В этих случаях в основную методику были внесены некоторые коррективы (более 3 последовательных нуклеотидов или ампликон длиной более 150 п.о.), цель которых состояла в обнаружении соответствующего набора праймеров и зондов. |
Меченые препараты получали традиционными способами путем маркировки олигонуклеотида способным к обнаружению маркером. Для маркировки можно использовать маркеры, включающие радиоизотопы, флуоресцентные вещества, ферменты, биотин и гаптены.
Гибридизацию между меченым препаратом и образцом можно осуществлять известными методами, такими как дот-блоттинг и нозерн-блоттинг. Образование гибрида может быть подтверждено обнаружением меченого препарата с помощью известных методов, например, таких как авторадиография с использованием радиоизотопов, применение антител, меченных ферментом, где используют фермент или биотин и т.п.
Фрагменты ДНК из этих олигонулеотидов, представленные, как SEQ ID, выбранные из SEQ ID No 1, SEQ ID No 2, SEQ ID No 4, SEQ ID No 5, SEQ ID No 7, SEQ ID No 8, SEQ ID No 10, SEQ ID No 11, SEQ ID No 13, SEQ ID No 14, SEQ ID No 16, SEQ ID No 17, SEQ ID No 19, SEQ ID No 20, SEQ ID No 22, SEQ ID No 23, SEQ ID No 25, SEQ ID No 26, соответственно, могут использоваться в качестве праймера в методе PCR, предназначенном для идентификации видов. Более конкретно, микробные клетки, подлежащие идентификации, подвергают бактериолизу и любой из ДНК фрагментов SEQ ID, выбранный из SEQ ID No 1, SEQ ID No 4, SEQ ID No 7, SEQ ID No 10, SEQ ID No 13, SEQ ID No 16, SEQ ID No 19, SEQ ID No 22, SEQ ID No 25, а также SEQ ID, выбранной из SEQ ID No 2, SEQ ID No 5, SEQ ID No 8, SEQ ID No 11, SEQ ID No 14, SEQ ID No 17, SEQ ID No 20, SEQ ID No 23, SEQ ID No 26, добавляют в качестве праймера, затем проводят обработку ДНК полимеразой. Если с помощью электрофореза и т.п. наблюдалась амплификация ДНК, это означало, что клетки обладают частью гена, соответствующей используемому фрагменту ДНК, т.е. клетки идентифицируют как принадлежащие к тому же виду, что и праймер из фрагмента ДНК.
Таким образом, предусматриваются олигонуклеотиды, содержащие SEQ ID, выбранную из SEQ ID No 1, SEQ ID No 2, SEQ ID No 4, SEQ ID No 5, SEQ ID No 7, SEQ ID No 8, SEQ ID No 10, SEQ ID No 11, SEQ ID No 13, SEQ ID No 14, SEQ ID No 16, SEQ ID No 17, SEQ ID No 19, SEQ ID No 20, SEQ ID No 22, SEQ ID No 23, SEQ ID No 25, SEQ ID No 26, и соответствующие комплементарные последовательности.
Согласно изобретению также предусматривается олинуклеотидный зонд для обнаружения целевой последовательности нуклеиновых кислот, которая является характеристикой видов рода Bifidobacterium, где указанный зонд выбирают из:
1) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium adolescentis ДНК, представленной SEQ ID No 3, или соответствующей комплементарной последовательностью;
2) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium angulatum ДНК, представленной SEQ ID No 6, или соответствующей комплементарной последовательностью;
3) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium bifidum ДНК, представленной SEQ ID No 9, или соответствующей комплементарной последовательностью;
4) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium breve ДНК, представленной SEQ ID No 12, или соответствующей комплементарной последовательностью;
5) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium catenulatum ДНК, представленной SEQ ID No 15, или соответствующей комплементарной последовательностью;
6) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium dentium ДНК, представленной SEQ ID No 18, или соответствующей комплементарной последовательностью;
7) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium infantis ДНК, представленной SEQ ID No 21, или соответствующей комплементарной последовательностью;
8) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium longum ДНК, представленной SEQ ID No 24, или соответствующей комплементарной последовательностью;
9) меченого олигонуклеотида, который специфически гибридизован со всеми Bifidobacterium ДНК, представленной SEQ ID No 27, или соответствующей комплементарной последовательностью.
Кроме того, изобретение предусматривает способ видоспецифичной детекции видов рода Bifidobacterium, обнаруженного у людей, в особенности у детей, включающий следующие стадии:
(А) контактирование образца с олигонуклеотидным зондом в растворе для гибридизации, где указанный зонд выбирают из группы, состоящей из:
1) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium adolescentis ДНК, представленной SEQ ID No 3, или соответствующей комплементарной последовательностью;
2) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium angulatum ДНК, представленной SEQ ID No 6, или соответствующей комплементарной последовательностью;
3) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium bifidum ДНК, представленной SEQ ID No 9, или соответствующей комплементарной последовательностью;
4) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium breve ДНК, представленной SEQ ID No 12, или соответствующей комплементарной последовательностью;
5) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium catenulatum ДНК, представленной SEQ ID No 15, или соответствующей комплементарной последовательностью;
6) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium dentium ДНК, представленной SEQ ID No 18, или соответствующей комплементарной последовательностью;
7) меченого олигонуклеотида, который специфически гибридизован с Вifidobacterium infantis ДНК, представленной SEQ ID No 21, или соответствующей комплементарной последовательностью;
8) меченого олигонуклеотида, который специфически гибридизован с Bifidobacterium longum ДНК, представленной SEQ ID No 24, или соответствующей комплементарной последовательностью;
9) меченого олигонуклеотида, который специфически гибридизован со всеми Bifidobacterium ДНК, представленной SEQ ID No 27, или соответствующей комплементарной последовательностью, и
(В) установление факта гибридизации зонда с нуклеиновыми кислотами в указанном образце с целью обнаружения наличия в образце указанных видов рода.
Изобретение также включает способ видоспецифичной детекции видов рода Bifidobacterium, обнаруженного у людей, в особенности у детей, включающий следующие стадии:
а) амплификацию последовательности нуклеиновых кислот с использованием набора праймеров, включающего олигонуклеотидный праймер SEQ ID No, выбранной из SEQ ID No 1, SEQ ID No 4, SEQ ID No 7, SEQ ID No 10, SEQ ID No 13, SEQ ID No 16, SEQ ID No 19, SEQ ID No 22, SEQ ID No 23, SEQ ID No 25, а также нуклеотидный праймер SEQ ID, выбранной из SEQ ID No 2, SEQ ID No 5, SEQ ID No 8, SEQ ID No 11, SEQ ID No 14, SEQ ID No 17, SEQ ID No 20, SEQ ID No 23, SEQ ID No 26; и
b) установление факта гибридизации указанного выше олигонуклеотидного зонда с целевой последовательностью нуклеиновых кислот.
Описанный способ удобен для производства диагностического набора. Соответственно, изобретение предусматривает диагностический набор для детекции в образце видов Bifidobacterium, выбранных из Bifidobacterium adolescentis, B. angulatum, B. bifidum, B. breve, B. catenulatum, B. dentium,B. infantis и B. longum с помощью гибридизационного анализа, который содержит, по меньшей мере, упомянутый выше ДНК зонд, а также один или несколько дополнительных средств, требующихся для гибридизационного анализа, таких как денатурированная жидкость, среда гибридизации, промывная жидкость, твердый носитель, сосуд для гибридизации и меченые средства обнаружения.
Также предусматривается диагностический набор для обнаружения в образце указанных выше видов Bifidobacterium с помощью PCR анализа, включающий набор указанных выше ДНК праймеров, а также один или более дополнительных средств, требующихся для PCR анализа, таких как полимераза, полимеризационная среда, верхний масляный слой, реакционный сосуд и средства для обнаружения амплифицированной ДНК.
Пример 1. Аттестация разработанных зондов и праймеров для определения бифидобактерий
Бактериальные штаммы, используемые для подтверждения анализа, представляющего относительное количественное определение различных видов Bifidobacterium, перечислены в таблице 2.
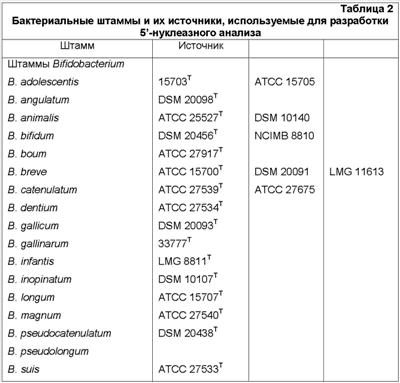
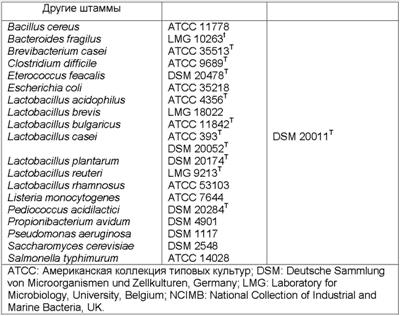
Все штаммы бифидобактерий культивировали в Mann Rogosa Sharp (MRS) бульонной (Oxoid Basingstoke, UK) среде при 37°С в течение 24 часов в анаэробных условиях. Ночные культуры хранили при -20°С до последующего использования.
ДНК экстрагировали из бактериальных культур размораживанием 5 мл замороженных ночных культур в смеси воды со льдом. Затем культуры центрифугировали в течение 20 минут при 4000 об/мин при 4°С (Sorvlall RT7, Du Pont, Stevenage, UK) для осаждения бактериальных клеток. Полученный осадок промывали 1 мл TES (50 мМ трис-HCl [pH 8,0], 5мМ EDTA; 50 мМ NaCl), с последующим центрифугированием при 4000 об/мин в течение 10 минут при 4°С. Супернатант удаляли и осадок повторно суспендировали в 1 мл THMS (30 мМ трис-HCl [pH 8,0], 3 мМ MgCl2, 25% (мас./об.) сахароза). После переноса суспензии в 2 мл пробирку Эппендорфа добавляли 200 мкл лизозима (0,1 г/мл; Sigma Aldrich Chemie, Stainheim; DE) и 40 мкл мутанолизина (1 мг/мл; Sigma Aldrich Chemie,; DE), и полученную смесь инкубировали в течение 30 минут при 37°С. Затем раствор центрифугировали в течение 5 минут при 10000 об/мин при 4°С (Sigma 1-15, Sigma Laborzentrifugen GmbH, Osterode am Harz, DE). Супернатант удаляли и осадок повторно суспендировали в 100 мкл THMS, затем добавляли 400 мкл TES (включая 0,5% SDS) и 7,5 мкл Proteinase K (20 мг/мл); Boehringer Mannhein GmbH, Mannhein, DE). Смесь встряхивали и инкубировали при 65°С в течение 30 минут. Затем проводили стандартную экстракцию смесью фенол/хлороформ с последующей обработкой 2,5 мкл RNase A (1 мг/мл; Roche Diagnostics, Mannhein, DE) в течение 30 минут при 37°С. После чего ДНК осаждали выдерживанием при -20°C в течение, по меньшей мере, 30 минут после добавления 2 объемов охлажденного льдом этанола (96%) и 0,1 объемом 0,3М раствора ацетата натрия (рН 5,2). Растворы, в которых образовался осадок, центрифугировали при 13000 об/мин в течение 20 минут при 4°С и супернатанты промывали 500 мкл 70% этанола с последующим центрифугированием при 13000 об/мин в течение 5 минут при 4°С. Супернатанты отбрасывали и осадок после центрифугирования сушили при комнатной температуре. ДНК ресуспендировали в 100 мкл стерильной милли-Q и хранили при -20°С.
Сначала тестировали специфичность каждого парного 5'-нуклеазного анализа, осуществляя амплификацию 25 мкл различных штаммов (см. таблицу 2). PCR реакции в объеме 25 мкл проводили с использованием 2,5 мкл матричной ДНК, 12,5 мкл TaqMan Universal Master Mix (Applied Biosystem), 900 нМ каждого из праймеров и 200 нМ каждого зонда с последующим осуществлением TaqMan Universal Temperature Profile, который состоял в нагревании при 50°С в течение 2 минут, выдерживании образца в течение 10 минут при 95°С с последующими 45 циклами продолжительностью в 15 секунд при 90°С и 60°С длительностью в 1 минуту с использованием ABI Prism 7700 (Applied Biosystem, Nieuwerker a/d IJssel, NL). Все 5'-нуклеазных анализов оказались специфичными относительно видов Bifidobacterium, для которых они были разработаны, и 5'-нуклеазного анализа, предназначенного для определения общего количества испытуемых видов Bifidobacterium, но не для других штаммов, таких как Propioni bacterium или Lactobacillus. Следует отметить, что 5'-нуклеазный анализ на B. catenulatum также позволяет детектировать B. pseudocatenulatum. Кроме того, образцы, обработанные ДНКазой и РНКазой, тестировали для подтверждения того, что в ходе анализа не детектировали загрязненную РНК. Также готовили смесь монокультур Bifidobacterium adolescentis, B. angulatum, B. breve,B. bifidum, B. catenulatum, B. dentium, B. infantis и B. longum с целью подтверждения того, что рассматриваемая смесь составляет примерно 100%. В этом случае можно исключить конкуренцию между различными видами Bifidobacterium, используемыми в качестве матрицы. Это соответствует случаю, представленному на фиг.1, который отображает установленные количества в смеси каждого из видов Bifidobacterium, а также общее количество видов Bifidobacterium, содержащихся в смеси.
В таблице 3 приведены значения CV для воспроизводимости и повторяемости различных 5'-нуклеазных анализов.
| Таблица 3 |
| Чувствительность 5'-нуклеазных анализов в сравнении с «традиционным» PCR, а также их воспроизводимость и повторяемость |
| Мишень |
Чувствительностьа
(х) |
Воспроизводимостьb
[CV (%)] |
Повторяемостьc
[CV (%)] |
| B. adolescentis |
10000 |
5,11 |
5,68 |
| B.angulatum |
1000 |
19,48 |
20,92 |
| B. bifidum |
100 |
11,65 |
11,20 |
| B. breve |
100 |
2,06 |
4,08 |
| B. catenulatum |
1000 |
9,42 |
14,83 |
| B. dentium |
100 |
12,65 |
11,35 |
| B. infantis |
1000 |
2,34 |
2,31 |
| B. longum |
10000 |
9,10 |
8,18 |
a во сколько раз чувствительность 5'-нуклеазного анализа выше, чем чувствительность «традиционного» PCR
b воспроизводимость определяли тестированием монокультур (100%), взятых в 10-кратном избытке, и расчетом CV (%) на базе полученных результатов
с повторяемость определяли трехкратным тестированием монокультур, взятых в четырехкратном избытке, и расчетом CV (%) на базе полученных результатов |
Разработанные 5'-нуклеазные анализы сравнивали с традиционной качественной видоспецифической PCR (проводимой с использованием праймеров, описанных Matsuki, T., K. Watanabe, R. Tanaka, M. Fukuda and H. Oyazu. 1999. Distribution of bifidobacterial species in human intestinal microflora examined with rRNA-gene-tergeted species-specific primers. Appl. Environ. Microbiol. 65:4506-4512) для определения чувствительности различных анализов, а также проверки на ложные положительные или отрицательные результаты. Результаты, представленные в таблице 3, свидетельствуют о том, что чувствительность 5'-нуклеазных анализов отличается от чувствительности традиционной видоспецифичной PCR. В таблице 4 приведены оптимальные концентрации праймера и зонда, используемых в дуплексных 5'-нуклеазных анализах.
| Таблица 4 |
| Оптимизированные конечные концентрации праймера и зонда, используемых в дуплексном 5'-нуклеазных анализах |
| Мишень |
5'-нуклеазный анализ |
Прямой праймер
(нM) |
Обратный праймер
(нM) |
Зонд
(нM) |
| B. adolescentis |
B. adolescentis
Все Bifidobacterium |
300
300 |
150
600 |
100
100 |
| B. angulatum |
B.angulatum
Все Bifidobacterium |
900
300 |
900
300 |
200
50 |
| B. bifidum |
B. bifidum
Все Bifidobacterium |
600
300 |
600
300 |
200
100 |
| B. breve |
B. breve
Все Bifidobacterium |
300
450 |
300
450 |
100
150 |
| B. catenulatum |
B. catenulatum
Все Bifidobacterium |
300
600 |
300
600 |
100
100 |
| B. dentium |
B. dentium
Все Bifidobacterium |
900
300 |
900
300 |
200
50 |
| B. infantis |
B. infantis
Все Bifidobacterium |
300
900 |
300
900 |
100
100 |
| B. longum |
B. longum
Все Bifidobacterium |
300
600 |
300
600 |
100
200 |
Все
Bifidobacterium |
Все Bifidobacterium
Все бактерии |
450
900 |
450
900 |
100
200 |
Пример 2. Клинические испытания
Исследование проводили двойным слепым, многоцентровым испытанием с контролем плацебо при использовании двух лечебных групп. Младенцев, получающих полноценное питание, в возрасте от 28 до 90 дней выбирали из четырех больниц в Германии. Дети участвовали в экспериментах в том случае, если их вес при рождении составлял 2600-4500 г и они питались полноценными молочными смесями в течение, по меньшей мере, четырех недель перед началом терапевтического воздействия. Из эксперимента исключались дети с пороками развития или с доказанной или подозреваемой аллергией на коровье молоко, дети, появившиеся в результате многоплодовых родов, дети, получавшие антибиотики менее чем за две недели до начала исследования, а также дети, питавшиеся смесями, содержащими про- или пребиотик, менее чем за месяц до начала исследования. После регистрации детей в произвольном порядке определяли в одну из двух экспериментальных групп: группу, получающую питание, дополненное 0,8 г/100 мл галактоолигосахаридов и фруктополисахаридов (GFSE-группа), и группу, получающую стандартное детское питание (SF-группа). Состав основных питательных компонентов в молочной смеси представлен в таблице 5.
| Таблица 5 |
| Состав экспериментальных смесей (в расчете на 100 мл готовой смеси) |
 |
Смесь, дополненная смесью углеводов
(Aptamil 1 с GOS/FOS, Milupa) |
Стандартная смесь
(Aptamil 1, Milupa) |
| Энергетическая ценность (ккал) |
72 |
72 |
| Белок (г) |
1,5 |
1,5 |
| Углеводы (г) |
8,5 |
8,5 |
| - лактоза (г) |
7,5 |
7,5 |
| - крахмал (г) |
1 |
1 |
| Неусваиваемые олигосахариды (г) |
0,8 |
0 |
| - галактоолигосахариды (г) |
0,72 |
0 |
| - фруктополисахариды (г) |
0,08 |
0 |
| Жир (г) |
3,6 |
3,6 |
Группу младенцев грудного вскармливания использовали в качестве эталонной группы (BF группа). Образцы кала собирали в течение трех дней после начала исследования, через 4 недели и в конце испытательного периода (6 недель). Проведение исследования было утверждено комитетом по медицинской этике четырех больниц. До начала исследования было получено письменное согласие от родителей.
Нуклеиновые кислоты выделяли из фекалий оттаиванием образцов в ледяной воде с последующим 10× (мас./об.) разбавлением в PBS (0,37 М NaCl, 2,7 мM KCl, 8,1 мM Na2HPO4 [pH 7,4]) и 10-минутной гомогенизацией с использованием устройства stomacher (IUL Instruments, Barcelona, Spain). Гомогенизированный кал хранили при -20°С до выделения ДНК. Экстракцию начинали оттаиванием 1 мл образца гомогенизированных фекалий в ледяной воде с последующим центрифугированием в течение 1 минуты при 1100 об/мин для удаления инородных веществ и крупных частиц. Супернатанты переносили в новую пробирку и центрифугировали в течение 5 минут при 10000 об/мин. Осадки после центрифугирования ресуспендировали в 1 мл TN150 (10 мM Трис-HCl [pH 8,0], 10 мM RDTA) и переносили в стерильные пробирки, содержащие 0,3 г циркониевых шариков (диаметр 0,1 мм, BioSpec Products, Bartlesville, US). В полученные суспензии добавляли 150 мкл ТЕ-забуференного фенола (рН±7,5) и образцы на 3 минуты помещали в битер с мини-шариками при 5000 об/мин (BioSpec Products, Bartlesville, US). После измельчения дробью образцы немедленно охлаждали на льду до добавления 150 мкл хлороформа. Образцы кратковременно встряхивали и центрифугировали в течение 5 минут при 10000 об/мин, верхней фазы переносили в чистые пробирки Эппендорфа емкостью 2 мл и приступали к экстракции смесью фенол/хлороформ. После фенол-хлороформной экстракции проводили осаждение ДНК охлаждением образцов при -20°С в течение, по меньшей мере, 30 минут после добавления 1 мл охлажденного льдом этанола (96%) и 50 мкл 3 М ацетата натрия (рН 5,2). Затем образцы центрифугировали в течение 20 минут при 13000 об/мин и промывали 150 мкл 70% этанола. После центрифугирования в течение 5 минут при 13000 об/мин супернатанты отбрасывали и осадки сушили на воздухе при комнатной температуре. ДНК ресуспендировали в 100 мкл стерильной милли-Q и хранили при -20°С.
Относительное определение различных видов Bifidobacterium в образцах кала проводили с помощью дуплексного 5'-нуклеазного анализа. Относительное количество каждого вида рассчитывали согласно Liu et al., 2002. Эффективность каждой кривой амплификации рассчитывали по отдельности по формуле Е=(пороговая величинаА/пороговая величинаВ)-(Сt1A-Ct1B)-1. С помощью рассчитанных значений эффективности рассчитывали начальное содержание ДНК (Ro) по формуле Ro=пороговое значение/(1+Е)Ct. Затем исходное количество ДНК вида Bifidobacterium может быть разделено на исходное количество ДНК во всех видах Bifidobacterium. Далее полученное соотношение может быть нормализовано на 100% с учетом количества монокультуры.
Общее количество Bifidobacterium также может быть определено с помощью указанного выше метода FISH (Langendijk, F. Shut, G.J. Jansen, G.R. Raangs, G.R. Kamphuis, M.H. Wilkison and G.W. Welling  Quantitative fluorescence in situ hybridization of Bifidobacterium spp. with genus-specific 16S rRNA-targeted probes and its application in fecal samples Quantitative fluorescence in situ hybridization of Bifidobacterium spp. with genus-specific 16S rRNA-targeted probes and its application in fecal samples Appl. Environ. Microbiol. 61 (8): 3069-75. (1995)). Appl. Environ. Microbiol. 61 (8): 3069-75. (1995)).
Процентное содержание рода Bifidobacterium в расчете на общее содержание бактерий составило 75, 47 и 68% в BF, SF и GFCF группе, соответственно, которое демонстрирует, что GFCF группа, получающая смесь неусваиваемых углеводов, обладает более бифидогенной флорой, как и в случае BF группы, по сравнению с SF группой.
В таблице 6 представлены данные, демонстрирующие преобладание каждого вида в различных группах в начале, а также в конце испытания. В таблице 7 приведены количества в процентах отдельных видов Bifidobacteria относительно общего количества Bifidobacteria.
| Таблица 6 |
| Преобладание (в %) видов Bifidobacteria в фекалиях детей через 6 недель питания материнским молоком (BF), детскими молочными смесями, содержащими пребитическую смесь (GFCF) или стандартной смесью (SF) |
| Вид |
BF |
GFSF |
SF |
| B. catenulatum |
80 |
67 |
75 |
| B. adolescentis |
20 |
11 |
50 |
| B. breve |
70 |
78 |
63 |
| B. longum |
50 |
56 |
63 |
| B. bifidum |
10 |
11 |
13 |
| B.angulatum |
30 |
11 |
13 |
| B. infantis |
100 |
100 |
100 |
| B. dentium |
20 |
11 |
13 |
| Таблица 7 |
| Процентное содержание отдельных видов Bifidobacteria относительного общего числа Bifidobacteria в фекалиях через 6 недель питания |
| Вид |
Грудное кормление
% (sd) |
GFSF-питание
% (sd) |
SF-питание
% (sd) |
| B. catenulatum |
1,9 (1,0) |
1,5 (3,0) |
9,8 (12,6) |
| B. adolescentis |
0,3 (0,9) |
0,1 (0,2) |
2,9 (6,0) |
| B. breve |
11,7 (9,6) |
5,4 (10,8) |
4,9 (10,7) |
| B. longum |
7,3 (13,9) |
5,4 (10,7) |
6,2 (9,4) |
| B. bifidum |
<0,1 (0,0) |
<0,1 (0,0) |
<0,1 (0,0) |
| B. angulatum |
<0,0 (0,0) |
<0,1 (0,2) |
<0,1 (0,0) |
| B. infantis |
32,0 (18,9) |
32,1 (20,0) |
37,8 (18,4) |
| B. dentium |
<0,1 (0,0) |
<0,1 (0,0) |
<0,1 (0,0) |
В трех различных группах присутствует большое число различных видов Bifidobacterium. Значительное уменьшение преобладания и количества B. adolescentis наблюдается у детей, получающих грудное кормление, и детей, получающих GFSF, в отличие от детей, питающихся стандартной смесью. Через 6 недель кормления превалирование и количество B. adolescentis значительно выше у детей, получающих SF, чем у детей, получающих GFSF или вскармливаемых грудью. Анализ образцов кала детей, получающих GFSF, обнаружил большое разнообразие в бифидобактериальной флоре, аналогично флоре детей, получающих грудное кормление, при этом не наблюдалась стимуляция только одного или нескольких видов. Помимо влияния на B. adolescentis профили детей, вскармливаемых грудью, и детей, получающих GFSF, также демонстрируют меньшее содержание B. сatenulatum (+B. pseudocatenulatum), чем профиль детей, питающихся стандартной смесью. B. infantis и B. longum, как оказалось, доминируют у детей, получающих грудное кормление, а также у детей, питающихся стандартными молочными смесями (SF) или стандартной смесью, дополненной пребиотиками (GFSF). B. breve доминируют во всех трех группах, однако в группе грудного вскармливания процент B. breve от общего количества бифидобактерий выше (11,7%), чем в SF (4,9%) и GFSF (5,4%) группе.
Пример 3. Эксперименты на аллергию у животных
Самцов BALB/c мышей, не содержащих специфических патогенов, получали от Charles River (Maastrict, the Nederlands). Пища и вода давались без ограничений и использовали мышей в возрасте 6-9 недель. Все эксперименты были одобрены комитетом по этике обращения с животными из University of Utrecht, the Netherlands.
Яичный альбумин (сорт V) и ацетил- -метилхолинхлорид (метахолин) приобретали у Sigma Chemical Co. (St. Lois, MO. USA). Гидроксид алюминия (AlumImject) приобретали у Pierce (Rockford, IL, USA). -метилхолинхлорид (метахолин) приобретали у Sigma Chemical Co. (St. Lois, MO. USA). Гидроксид алюминия (AlumImject) приобретали у Pierce (Rockford, IL, USA).
Мышей сенсибилизировали двумя i.p. инъекциями, содержащими 10 мкг яичного альбумина, нанесенного на 2,25 мг гидроксида алюминия в 100 мкл физиологического раствора, или только физиологическим раствором в день 0 и 7, от начала испытания. Мышей заражали на 35, 38 и 41 день путем вдыхания аэрозолей яичного альбумина при нахождении в плексигласовой камере в течение 20 минут. Аэрозоли получали распылением раствора яичного альбумина (10 мг/мл) в физиологическом растворе с использованием устройства Pari LC Star (Pari respiratory Equipment, Richmond, VA, USA).
Начиная с 28 дня и до конца эксперимента (т.е. 42 день) мышей ежедневно обрабатывали пероральным введением 1·109 (CFU) Bifidobacterium breve и 25 мг смеси галактоолигосахаридов и фруктополисахаридов (9:1) через зонд (0,2 мл, физиологический солевой раствор). В качестве контроля через зонд вводили 0,2 мл физиологического солевого раствора.
Дыхательную восприимчивость к распыленному метахолину определяли через 24 часа после заражения аэрозолем находящихся в сознании и свободном состоянии мышей с использованием плетизмографии всего организма (BUXCO, EMKA, Paris, France). Дыхательную реакцию выражали в виде увеличенной паузы (PenH).
Статистический анализ. Кривые дыхательной реакции на метахолин статистически анализировали с использованием общей линейной модели или повторных измерений с последующим post-hoc сравнением между группами. Подсчет клеток статистически анализировали с использованием Mann-Whitney теста (Siegel, S., Castellan Jr. N J, 1988  Nonparametric statistics for the behavioral sciences Nonparametric statistics for the behavioral sciences 2nd ed. McGrow Hill Book Company, New York, USA). Все другие анализы проводили с использованием критерия Стьюдента (Abramowitz, M., Stegun, I.A., 1972, 2nd ed. McGrow Hill Book Company, New York, USA). Все другие анализы проводили с использованием критерия Стьюдента (Abramowitz, M., Stegun, I.A., 1972,  Handbook of mathematical functions Handbook of mathematical functions Dover publications, Inc. New York, USA). Статистически значимой считалось значение вероятности р<0,05. Dover publications, Inc. New York, USA). Статистически значимой считалось значение вероятности р<0,05.
Результаты дыхательной гиперчувствительности. Результаты измерения дыхательной гиперчувствительности показали, что, по сравнению с контрольной группой, мыши, получающие B. breve+смесь галактоолигосахаридов и фруктополисахаридов, демонстрируют статистически значимое понижение дыхательной гиперчувствительности, что указывает на понижение астматической реакции.
На фиг.2 гиперчувствительность отображена графиком зависимости относительного значения PenH (увеличенная пауза) от концентрации метахолина для мышей, получающих комбинацию B. breve+смесь GOS/FOS, и контрольной группы мышей, получающих физиологический раствор. Представленные на графике относительные значения PenH получали вычитанием контрольных значений, полученных для мышей, несенсибилизированных яичным альбумином, и нормализацией значения, полученного для контрольной группы при самой высокой концентрации метахолина.
Как известно в данной области и из международных директив, композиции всех следующих примеров могут дополнительно содержать минералы, микроэлементы и витамины, холин, таурин, карнитин, и/или миоинозит или их смеси. Кроме того, в композиции могут необязательно присутствовать органические кислоты, вкусовые добавки и красители.
Пример 4
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 13,1 г порошка):
| 8% (энергетических) белка |
1,4 г (казеиновая сывороточная смесь) |
| 45% (энергетических) усваиваемых углеводов |
7,5 г |
| 47% (энергетических) жира |
3,5 г |
GOS (90% галактоолигосахаридов, Borculo
Domno NL)/полифруктоза (10% инулин, Raftilin HP, Orafti BE) |
0,4 г |
| B. breve |
1,3·108 cfu |
Пример 5
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 14 г порошка):
| 10% (энергетических) белка |
1,8 г (казеиновая сывороточная смесь) |
| 46% (энергетических) усваиваемых углеводов |
8,0 г |
| 44% (энергетических) жира |
3,4 г |
| GOS/полифруктоза (см. пример 4) |
0,4 г |
| B. breve |
1,4·108 cfu |
Пример 6
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 16,1 г порошка):
| 10% (энергетических) белка |
1,9 г (казеиновая сывороточная смесь) |
| 51% (энергетических) усваиваемых углеводов |
9,9 г |
| 39% (энергетических) жира |
3,3 г |
| FOS (Raftilin, Orafti/галактоманнан 9/1 |
0,4 г |
| B. breve |
1,6·108 cfu |
Пример 7
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 13 г порошка):
| 10% (энергетических) белкового эквивалента |
1,8 г (гидролизованный сывороточный белок молока) |
| 42% (энергетических) усваиваемых углеводов |
7,1 г |
| 48% (энергетических) жира |
3,6 г |
| Сиалильные олигосахариды, неусваиваемые мальтодекстрины 9/1 |
0,4 г |
| B. breve |
6,5·108 cfu/г |
Пример 8
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 15 г порошка):
| 10% (энергетических) белкового эквивалента |
1,8 г (гидролизованный сывороточный белок молока) |
| 42% (энергетических) усваиваемых углеводов |
8,6 г |
| 44% (энергетических) жира |
3,6 г |
| Фукоолигосахариды (из водорослевого фукоиндана), галактоманнан 8/2 |
0,4 г |
| B. breve |
7,5·108 cfu |
Пример 9
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 15,1 г порошка):
| 10% (энергетических) белкового эквивалента |
1,8 г (гидролизованный сывороточный белок молока) |
| 42% (энергетических) усваиваемых углеводов |
8,6 г |
| 44% (энергетических) жира |
3,6 г |
| Манноолигосахариды, арабиногалактан 9/1 |
0,4 г |
| B. breve |
1,5·108 cfu |
Пример 10
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 15,2 г порошка):
| 10% (энергетических) белка |
1,7 г (гидролизованный сывороточный белок молока) |
| 48% (энергетических) усваиваемых углеводов |
8,4 г |
| 42% (энергетических) жира |
3,3 г |
| GOS/галакторуновые олигосахариды/полифруктоза 7/2/1 |
1,0 г |
| B. breve |
7,5·108 cfu |
Пример 11
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 15,8 г порошка):
| 11% (энергетических) белка |
1,9 г (гидролизованный сывороточный белок молока) |
| 48% (энергетических) усваиваемых углеводов |
8,7 г |
| 41% (энергетических) жира |
3,3 г |
| Ксилоолигосахариды/галактан 9/1 |
0,8 г |
| B. breve |
8·108 cfu |
Пример 12
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 15 г порошка):
| 10% (энергетических) белка |
1,7 г (казеиновая сывороточная смесь) |
| 48% (энергетических) усваиваемых углеводов |
8,1 г |
| 42% (энергетических) жира |
3,1 г |
| GOS/полифруктоза 9/1 |
0,8г |
| Галактоманнан |
0,42 |
| B. breve |
1,5·108 cfu |
Пример 13
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 15,9 г порошка):
| 13% (энергетических) белка |
2,2 г (казеиновая сывороточная смесь) |
| 49% (энергетических) усваиваемых углеводов |
8,6 г |
| 37% (энергетических) жира |
3,0 г |
| GOS/полифруктоза 9/1 |
0,8 г |
| Галактоманнан |
0,4 г |
| B. breve |
1,6·108 cfu |
Пример 14
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 13,5 г порошка):
| 9% (энергетических) белкового эквивалента |
1,5 г (гидролизованный сывороточный белок молока) |
| 42% (энергетических) усваиваемых углеводов |
6,9 г |
| 49% (энергетических) жира |
3,6 г |
| GOS/полифруктоза/сиалиллактоза 7/2/1 |
0,8 г |
| B. breve |
1,4·108 cfu |
Пример 15
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 13,7 г порошка):
| 9% (энергетических) белкового эквивалента |
1,4 г (свободные аминокислоты)) |
| 44% (энергетических) усваиваемых углеводов |
7,1 г |
| 47% (энергетических) жира |
3,4 г |
| GOS/полифруктоза 6/4 |
0,8 г |
| B. breve |
1,4·108 cfu |
Пример 16
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 13,5 г порошка):
| 11% (энергетических) белка |
1,8 г (соевый белок) |
| 40% (энергетических) усваиваемых углеводов |
6,7 г |
| 49% (энергетических) жира |
3,6 г |
| GOS/галактоолигосахариды/полифруктоза 8/1/1 |
0,8 г |
| B. breve |
1,4·108 cfu |
Пример 17
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 15,1 г порошка):
| 12% (энергетических) белка |
2,2 г (соевый белок) |
| 43% (энергетических) усваиваемых углеводов |
7,7 г |
| 45% (энергетических) жира |
3,6 г |
| FOS/галактан 9/1 |
0,8 г |
| B. breve |
1,5·108 cfu |
Пример 18
Детская молочная смесь, содержащая в расчете на 100 мл конечного продукта (и на 16,5 г порошка):
| 13% (энергетических) белка |
2,0 г (гидролизованный сывороточный белок молока) |
| 57% (энергетических) усваиваемых углеводов |
8,6 г |
| 30% (энергетических) жира |
2,0 г |
| GOS/полифруктоза 9/1 |
1,0 г |
| Соевые полисахариды |
0,5 г |
| B. breve |
1,5·109 cfu |
Пример 19
Продукт на основе молока, содержащий в расчете на 100 мл:
| 14% (энергетических) белка |
2,5 г (белка коровьего молока) |
| 43% (энергетических) усваиваемых углеводов |
7,5 г |
| 43% (энергетических) жира |
3,4 г |
| GOS/полифруктоза 7/3 |
1,5 г |
| B. breve |
3·108 cfu |
Пример 20
Детская молочная смесь, содержащий в расчете на 100 мл (и на 15,4 г порошка):
| 11% (энергетических) белка |
2,0 г (гидролизованного коллагена и соевого белка) |
| 46% (энергетических) усваиваемых углеводов |
8,6 г |
| 43% (энергетических) жира |
3,6 г |
| GOS/полифруктоза 3/1 |
0,4 г |
| B. breve |
6·108 cfu |
Пример 21
Добавка: 3 г продукта, добавляемого в 100 мл молока, содержащая:
| 28% (энергетических) белка |
0,7 г (казеиновая сывороточная смесь) |
| 72% (энергетических) усваиваемых углеводов |
2,0 г |
| GOS/полифруктоза 65/35 |
0,3 г |
| B. breve |
3·109 cfu |
Пример 22
Добавка, содержащая: 0,4-0,8 г материала, добавляемого в 100 мл молока, в расчете на грамм:
| Галактоманнан |
0,26 г |
| Усваиваемые углеводы |
0,44 г |
| GOS/полифруктоза 85/15 |
0,3 г |
| B. breve |
1,0·109 cfu |
Пример 23
Добавка, содержащая в расчете на 100 мл:
| 100% (энергетических) усваиваемых углеводов |
2,2 г |
| Минералы |
K, Na, Cl |
| Осмотическая концентрация раствора |
261 mOsm/1 |
| GOS/полифруктоза 55/45 |
0,4 г |
| B. breve |
1·109 cfu |
Пример 24
Детское питание, содержащее в расчете на 100 г (85 г добавлено в 240 мл молока)
| 4% (энергетических) белка |
4,7 г (белок коровьего молока) |
| 53% (энергетических) усваиваемых углеводов |
68 г |
| 43% (энергетических) жира |
24,6 г |
| GOS/полифруктоза 9/1 |
0,8 г |
| B. breve |
1,2·109 cfu |
Пример 25
Детское питание в тюбиках в расчете на 100 мл
| 9% (энергетических) белка |
3,4 г (казеин) |
| 50% (энергетических) углеводов |
18,8 г |
| 41% (энергетических) жира |
8 г |
| GOS/полифруктоза 7/3 |
0,4 г |
| B. breve |
5·108 cfu |
Пример 26
Детское питание, содержащее в расчете на 100 мл продукта
| 11% (энергетических) белка |
2,8 г (казеин) |
| 49% (энергетических) углеводов |
12,3 г |
| 40% (энергетических) жира |
4,4 г |
| GOS/полифруктоза 85/15 |
0,8 г |
| B. breve |
5·108 cfu |
Пример 27
Детское питание, состоящее из рисовой муки, содержащей в расчете на 100 г сухого продукта (4-7 ложек добавляют в 200 мл теплой детской молочной смеси, содержащей молоко для ребенка, начинающего ходить, или коровье молоко)
| Белок (растительный) |
7,4 г |
| Углеводы |
83 г |
| Жир |
0,5 г |
| Клетчатка, включающая 1,5 г GOS/полифруктоза 9/1 |
3 г |
| B. breve |
1·1010 cfu |
Пример 28
Детское питание, состоящее из предварительно сваренных хлопьев (пшеница, рожь, рис, ячмень, овес, гречка), содержащее в расчете на 100 г сухого продукта (5-7 ложек добавляют в 250 мл теплой детской молочной смеси, содержащей молоко для начинающего ходить ребенка, или коровье молоко)
| Белок (растительный) |
9,5 г |
| Углеводы |
74 г |
| Жир |
2,0 г |
| Клетчатка, включающая 1,5 г GOS/полифрутоза 8/2 |
3 г |
| B. breve |
2·1010 cfu |
Пример 29
Детское питание, состоящее из гомогенизированных овощей или фруктов, содержащее в расчете на 100 мл
| GOS/полифруктоза 75/25 |
2,0 г |
| B. breve |
2·109 cfu |
Формула изобретения
1. Препарат для применения в качестве питания, содержащий Bifidobacterium breve в количестве 1·104-1·1010 cfu/г и смесь, по меньшей мере, двух неусваиваемых растворимых углеводных компонентов А и В, в котором
указанный углеводный компонент А отличается от указанного компонента В структурой моносахаридных звеньев углевода;
содержание указанного углеводного компонента А составляет 5-95 мас.% от суммарного содержания компонентов А и В;
по меньшей мере, 50% от общего количества неусваиваемых растворимых углеводов выбирают из углеводов от дисахаридов до эйкозасахаридов; и
углеводные компоненты А и В отличаются по числу моносахаридных звеньев, причем средняя длина цепи углеводного компонента А, по меньшей мере, на 5 моносахаридных звеньев меньше средней длинный цепи компонента В.
2. Препарат по п.1, в котором углеводный компонент А выбирают из неусваиваемых моносахаридов вплоть до гексасахаридов одинаковой углеводной структуры, и углеводный компонент В выбирают из неусваиваемых гептасахаридов и высших полисахаридов одинаковой углеводной структуры.
3. Препарат по п.1, в котором содержание углеводного компонента А составляет 95-60 мас.%, и содержание углевода В составляет 5-40 мас.%, причем А+В=100 мас.%.
4. Препарат по п.3, в котором, по меньшей мере, 60 мас.%, предпочтительно 80-100 мас.%, углеводного компонента А принадлежит к группе галактоолигосахаридов предпочтительно к группе транс-галактоолигосахаридов.
5. Препарат по п.1, в котором, по меньшей мере, 60 мас.%, предпочтительно 80-100 мас.%, углеводного компонента В принадлежит к группе фруктополисахаридов, включающей инулин.
6. Препарат по п.1, содержащий 105-1011 cfu Bifidobacterium breve в расчете на грамм суммарного содержания неусваиваемых растворимых углеводов.
7. Препарат по п.1 для применения в качестве добавки, содержащей пробиотический Bifidobacterium breve в количестве 1·102-1·1011 cfu/г в расчете на добавку.
8. Препарат по п.1 для применения в качестве детского питания, содержащего Bifidobacterium breve в количестве 1·102-1·1012 cfu/г детской пищевой добавки.
9. Добавка в питание детей, содержащая препарат по любому из пп.1-8 и дополнительно включающая усваиваемый углевод, источник липидов или источник белка, или их смесь.
10. Детское питание, содержащее препарат по любому из пп.1-8 и дополнительно включающее усваиваемый углевод, источник липидов и источник белка.
11. Применение препарата по любому из пп.1-8 для изготовления композиции для нормализации состава видов Bifidobacterium в желудочно-кишечном тракте детей, получающих искусственное или частично грудное питание, по сравнению с таким составом у детей, вскармливаемых грудью.
12. Применение препарата по любому из пп.1-8 для изготовления композиции для профилактики или лечения одного или нескольких нарушений иммунной системы.
13. Применение по п.12, где нарушения иммунной системы выбирают из аллергии, атопии, аллергического ринита, пищевой гиперчувствительности, атопического дерматита, экземы и астмы.
14. Применение по п.12, где нарушение иммунной системы выбирают из диареи и вирусной диареи.
15. Применение препарата по любому из пп.1-8 для изготовления композиции для профилактики и/или лечения недостаточного поглощения энергии.
16. Применение препарата по любому из пп.1-8 для изготовления композиции для ингибирования инфильтрации эозинофилов, нейтрофилов и одноядерных клеток при аллергических заболеваниях, ингибирования иммунной реакции Th2 типа и/или стимуляции Th1 опосредованной иммунной реакции.
|